
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гетерогенный катализ
Лекция №9
Здесь катализатор составляет отдельную фазу. Наиболее часто встречается катализ газофазных реакций на твердом катализаторе. Гетерогенно-каталитические реакции состоят из следующих основных стадий:
1) диффузия исходных веществ к поверхности катализатора;
2) адсорбция исходных веществ на поверхности катализатора;
3) взаимодействие адсорбированных веществ с получением адсорбированных продуктов;
4) десорбция продуктов;
5) диффузия продуктов от поверхности катализатора.
Увеличение скорости реакции при гетерогенном катализе, так же как и при гомогенном катализе,объясняется образованием промежуточных комплексов с участием катализатора, что приводит к снижению энергии активации.
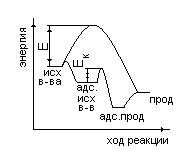
В зависимости от соотношения скоростей реакции и диффузии различают следующие области (режимы) протекания процесса.
1) Диффузионная область. 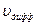 <<
<<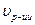
Различают внешнюю и внутреннюю диффузию. Скорость внешней диффузии зависит от скорости перемешивания или от скорости потока газа, скорость внутренней диффузии не зависит.
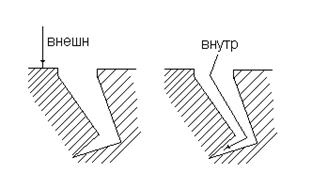
2) Кинетическая область. 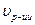 <<
<<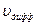
3) Переходная область. 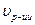
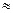
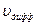
Рассмотрим кинетику мономолекулярной (одностадийной) реакции, протекающей на поверхности катализатора в кинетической области. Скоростью гетерогенной каталитической реакции называют величину равную 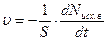 ,
,
здесь S – площадь поверхности катализатора; dN – количество исходных веществ, вступающих в реакцию за время dt.
Скорость поверхностной мономолекулярной реакции пропорциональна поверхностной концентрации адсорбированного вещества: 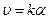 . Истинный порядок реакции - первый.
. Истинный порядок реакции - первый.
Поверхностную концентрацию адсорбированного вещества можно выразить через давление газа в объеме с помощью уравнения изотермы Ленгмюра:
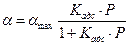 ;
;
тогда зависимость скорости реакции от давления газа в объеме выражается уравнением:
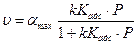 .
.
В частных случаях:
1) при малых давлениях реакционного газа 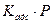 <<1;
<<1; 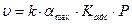 ;
;
кажущийся порядок реакции – первый;
2) при больших давлениях 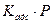 >>1;
>>1; 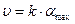 ;
;
кажущийся порядок - нулевой.
3) при средних давлениях адсорбцию приближенно можно описать уравнением Фрейндлиха: 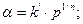
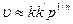 , кажущийся порядок реакции дробный
, кажущийся порядок реакции дробный
(от 0 до 1).
|
Дата добавления: 2014-01-05; Просмотров: 473; Нарушение авторских прав?; Мы поможем в написании вашей работы!