
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Поглощение почвой катионов. Поглощение почвой катионов осуществляется путем
|
|
|
|
Поглощение почвой катионов осуществляется путем
обменной ионной сорбции, необменной фиксации, химического и биологического поглощения.
Обменная сорбция — способность катионов диффузного слоя почвенных коллоидов обмениваться на эквивалентное количество катионов соприкасающегося с ними раствора.
Существенное значение имеет минералогический и химический состав почвенных коллоидов. Катионы кальция сильнее поглощаются гуминовыми кислотами и монтмориллонитом, аммоний — мусковитом.
Емкость поглощения у разных почв и содержание гумуса
| Содержание,% | Емкость поглощения катионов, мэкв/100 г почвы | Содержание поглощ. катионов, мэкв/100 г почвы | |||||
| Почва | гумуса | минеральных частиц диаметром | |||||
| 0.0002-25 мм | 0,00025-0,001 м | Са* + Мg* | Na | Н* | |||
| Дерново-подзолистая - | 2,5 | — | — | ||||
| Серая лесная | 3,0 | — | |||||
| Чернозем: | |||||||
| выщелочен ный - | 8,0 | — | |||||
| мощный | — | ||||||
| обыкновен ный - | 6.0 | ||||||
| южный | 4,5 | — | |||||
| Каштановая | 2.5 | — | |||||
| Серозем | 1,0 | — |
Необменное поглощение катионов (фиксация) происходит в почве постепенно и часть обменных катионов переходит в необменную форму (не вытесняется из почвы в раствор при действии нейтральных солей).
Наиболее интенсивно фиксируются ионы калия и аммония. Большинство исследователей считают, что основной причиной перехода катионов в необменное (фиксированное) состояние является защемление этих катионов в межплоскостных промежутках кристаллической решетки глинистых минералов с расширяющимся типом ее (монтмориллонит, вермикулит).
|
|
|
Химическое поглощение катионов. Катионы переходят в твердую фазу почвы в результате реакций солеобразования, при которых образуются нерастворимые в воде соединения. К таким катионам относятся Са2+, А13+, Fe3+ и отчасти Mg2+.
При взаимодействии с растворимыми в воде сульфатами, карбонатами и фосфатами эти катионы образуют нерастворимые соединения и выпадают в осадок в твердой фазе почвы:
[ППК-] Са2+ + Na2SO4->[ППK-] 2Na+ +CaSO4;
[ППК-] Са2+ + 2NaHCO3-^[ППK-]2Na+ + Ca(HCO3)2.
Ca(HCO3)2 — Н20- СаСО3 + СО2.
А1(ОН)3 + H3PO4-> AlPO4 + ЗН2О.
Биологическое поглощение катионов.
Некоторая часть катионов почвенного раствора поглощается в почве биологически вследствие усвоения их живыми организмами — растениями, микроорганизмами.
Биологическое поглощение носит избирательный характер, так как живые организмы поглощают в первую очередь катионы, необходимые для построения своих тканей.
К их числу относятся калий, аммоний, кальций, железо. Особенно велико значение этого вида поглощения для калия и аммония, которые физико-химически поглощаются слабо и не образуют в почве нерастворимых в воде соединений.
Поглощение анионов
Поглощение анионов почвами исследовано менее детально по сравнению с процессами поглощения катионов. Известно, что анионы поглощаются почвой в разной степени в зависимости от природы аниона, состава коллоидов и реакции среды.
Кислые почвы энергичнее поглощают анионы по сравнению с почвами, имеющими нейтральную или щелочную реакцию, в связи с повышенным содержанием подвижных форм полуторных окислов.
Основными видами поглощения анионов являются химическое и био-' логическое.
Широко распространенной реакцией при поглощении анионов следует признать солеобразование — реакцию взаимодействия растворимых солей, при которой образуется новая нерастворимая в воде соль, выпадающая в твердую фазу почвы. Таким путем поглощаются сульфаты, карбонаты и фосфаты.
|
|
|
Особенно велико значение реакций солеобразования для поглощения анионов фосфорной кислоты, которая образует с Са, А1 и Fe нерастворимые фосфаты.
Поглощение фосфатов почвой имеет положительное и отрицательное значение, так как приводит к накоплению фосфора в почве, но снижает степень его доступности растениям.
Общее содержание поглощенных катионов оснований (кроме Н+ и А13+) называют суммой обменных оснований.
На их долю в черноземах приходится до 80—90%; в дерново-подзолистых почвах и красноземах иногда 50% и более от ЕКО приходится на ионы водорода и алюминия.
В солонцах и солончаках наряду с кальцием и магнием в поглощенном состоянии присутствует натрий.
Сумма обменных оснований (S), выраженная в процентах от общей емкости катионного обмена (ЕКО), называется степенью насыщенности основаниями (V), которую определяют по формуле
V =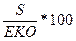 (%).
(%).
По этому показателю почвы делятся на насыщенные (V > 80%) и ненасыщенные (V 50—70%) основаниями.
Наилучшие условия для растений создаются при V в пределах 80—90% от ЕКО. При этом, однако, важны уровни насыщения ППК отдельными обменными катионами, особенно кальцием, магнием и калием. Уровни определяются так же, как и степень насыщенности основаниями. Например, степень насыщенности кальцием определяется по формуле Са=Са/ЕКО*100%
Таблица 3
Емкость поглощения и ее структура в дерново-подзолистой
легкосуглинистой почве при разном содержании гумуса,
мэкв/100 г почвы (А.И. Горбылева)
| Вариант опыта | Гумус, % | Емкость поглощения | ||
| Общая | минеральной части | органической части | ||
| Без удобрений Навоз + NPK Без удобрений Навоз + NPK | 1,4-1,8 3,5-4,0 | 15.0 16,6 31,3 34,6 | 10.6 11,2 13;0 11.2 | 4,4 5,4 18,3 23,4 |
4.Кислотность, щелочность, и буферность почвы
Таблица 4
| Значение рН реакции среды | |||||||||
| Концентрация Н ионов, г/л | 10-3 | 10-4 | 10-5 | 10-6 | 10-7 | 10-8 | 10-9 | 10-10 | 10-11 |
| рН | |||||||||
| Реакция среды | кислая | слабокислая | нейтральная | слабощелочная | щелочная |
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 534; Нарушение авторских прав?; Мы поможем в написании вашей работы!