
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Галогеналканы
|
|
|
|
Галогенопроизводные алканов (галогеналканы) имеют очень важное значение для синтеза многих соединений. Замена атомов водорода на галоген делает соединение химически активным, т.к. связь углерода с более электроотрицательным атомом галогена является полярной и довольно реакционноспособной в реакциях ионного типа. Полярность ковалентной связи, например С–Cl, приводит к смещению электронной плотности соседних связей в молекуле (индуктивный эффект).
Галогенопроизводные алканов широко применяются для синтеза алканов с заданным строением молекул. Для этого используется реакция взаимодействия их с активными металлами (реакция Вюрца):
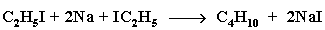
Если в реакции использовать разные галогенопроизводные, то получается смесь трех продуктов. Например:
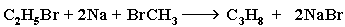
Кроме пропана C3H8 образуются бутан C4H10 (из 2-х молекул C2H5Br) и этан C2H6 (из 2-х молекул CH3Br).
Для галогенпроизводных характерно замещение галогена на другие группы атомов при действии воды, оснований и солей. Эти реакции протекают по механизму нуклеофильного замещения (SN), т.к. положительно заряженный углеродный атом, связанный с галогеном, является центром атаки нуклеофильными частицами (OH-, OR-, CN-, NH2- и др.).

Под действием нуклеофильного реагента (донора пары электронов) OH- происходит гетеролитический разрыв полярной связи С-Cl. Электронная пара этой связи отходит к более электроотрицательному атому Cl, который превращается в анион Cl- (анимация).
Нуклеофильное замещение в общем виде можно представить следующей схемой:
Y: + RX 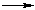 RY + X: (VRML-анимация)
RY + X: (VRML-анимация)
Механизмы нуклеофильного замещения в галогеналканах
Необходимо отметить, что галогеналканы являются представителями большого класса галогенопроизводных углеводородов (галогеноуглеводородов), к которому относятся также галогенозамещенные всех других углеводородов (алкенов, алкинов, циклоалканов, аренов и т.п.). Эти соединения играют важную роль в органическом синтезе и находят широкое практическое применение.
Для углубленного изучения данного класса органических веществ учащимся профильных колледжей и студентам младших курсов вузов мы предлагаем дистанционный курс " Галогеноуглеводороды ".
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 1075; Нарушение авторских прав?; Мы поможем в написании вашей работы!