
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Щявелево-янтарная К-ТА подвергается декарбоксилированию достаточно легко и не требует участия дополнительных ферментов - прямое декарбоксилирование
|
|
|
|
ИЗОЦИТРАТ подвергается далее ДЕГИДРИРОВАНИЮ под влиянием фермента -ИЗОЦИТРАТДЕГИДРОГЕНАЗЫ.


a-КГК подвергается реакции ОКИСЛИТЕЛЬНОГО ДЕКАРБОКСИЛИРОВАНИЯ, катализируемой комплексом ферментов (КЕТОГЛУТАРАТДЕГИДРОГЕНАЗНЫЙ комплекс), включающий 3 фермента и 5 КОФЕРМЕНТОВ.

СУКЦИНИЛ-КОА подвергается реакции субстратного ФОСФОРИЛИРОВАНИЯ.

ГТФ + АДФ = ГДФ + АТФ

Т.о. происходит распад АЦЕТИЛ-КОА до СО2 и восстановленного HSKOA.
ФУНКЦИИ ЦТК.
1.Катаболическая - распад АЦЕТИЛА.
2.Анаболическая. Компоненты ЦТК могут использоваться для синтеза др. соединений
ЩУК - синтез АСП, МАЛ AT - синтез глюкозы и т.д.
3.Интегративная. Взаимосвязь обмена БЖУ.
4.Энергетическая. Образование 1 молекулы АТФ. Если ЦТК работает вместе с дыхательной цепью, то образуется ещё 1 молекул АТФ.
5.ВОДОРОДГЕНЕРИРУЮЩАЯ - в результате ЦТК образуется 3 молекулы НАДН2 и 1 молекула ФАДН2, т.е. 4 пары молекул водорода. Они транспортируются в ЦТЭ.
Лекция № 8.
Образование воды как конечного продукта биологического окисления.
1.ИСТОРИЯ УЧЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ.
2.СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ.
3.КОМПОНЕНТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ.
4.ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ. ИСТОРИЯ УЧЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ.
Первые представления о биологическом окислении были высказаны ЛАВУАЗЬЕ, который говорил, что биологическое окисление - медленное горение. С химической точки зрения, горение - это взаимодействие углерода с кислородом с образованием СО2. Но в организме образование СО2 идёт путём ДЕКАРБОКСИЛИРОВАНИЯ, а биологическое окисление протекает при низкой температуре, не путём образования СО2, в присутствии воды и без образования пламени. Исходя из этого, были выдвинуты следующие настоящие представления о биологическом окислении в начале 20 в.:
|
|
|
1.Теория «активации» кислорода академика БАХА. Ведущей ролью в процессе биологического окисления он представлял образование ПЕРОКСИДОВ.


Эти взгляды поддержали ботаники, т.к. в растениях много ПЕРКСИДАЗ, а учёные, изучающие животные ткани, не поддержали эти взгляды, т.к. в них не обнаруживаются ПЕРОКСИДАЗЫ.
2.Теория активирования водорода академика ПАЛЛАДИНА. Он исходил из того, что в животных тканях много фермента - ДГ.

Конечным продуктом биологического окисления является вода. Взгляды БАХА и ПАЛЛАДИНА трансформировали. В настоящее время считается, что в биологическом окислении принимают участие ДГ и ОКСИДАЗЫ.
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О БИОЛОГИЧЕСКОМ ОКИСЛЕНИИ.
1. Биологическое окисление, как и окисление вообще, есть процесс переноса электронов. То вещество, что отдаёт электроны, окисляется, то, что принимает, восстанавливается. Если акцептором электронов является кислород, то такой процесс называется ТКАНЕВЫМ ДЫХАНИЕМ. Биологическое окисление предполагает ДЕГИДРИРОВАНИЕ с образованием воды.

Если водород взаимодействует с кислородом с образованием воды вне организма, то это сопровождается взрывом.
2. Биологическое окисление - это процесс многоступенчатый - многоступенчатая передача электронов с постепенным выделением энергии, что исключает взрыв.
3. Биологическое окисление - это процесс, требующий много ферментов. Т.о. биологическое окисление - это многоступенчатый процесс транспорта электронов, осуществляемый комплексов ферментов. Этот комплекс ферментов называется ЭЛЕКТРОН-ТРАНСПОРТНОЙ ЦЕПЬЮ (ЭТЦ), или ЦЕПЬЮ ПЕРЕНОСА ЭЛЕКТРОНОВ (ЦПЭ), или дыхательной цепью. ЭТЦ - это своеобразный КОНВЕЕР по переносу электронов и протонов от субстрата к кислороду.
КОМПОНЕНТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ.
1.НИКОТИНЗАВИСИМЫЕ ДГ, т.е. содержащие КОФЕРМЁНТЫ - НАД, НАДФ 2.ФЛАВИНЗАВИСИМЫЕ ДГ, т.е. содержащие КОФЕРМЁНТЫ - ФМН, ФАД.
|
|
|
З.УБИХИНОН (Ko-Q).
4.ЦИТОХРОМЫ: в, с, c1., а, а3.
Почти все эти компоненты, за исключением первого, встроены во внутреннюю мембрану МИТОХОНДРИЙ. В печени таких дыхательных цепей до 5000, а в сердце - до 20000.
СТРОЕНИЕ КОМПОНЕНТОВ ДЫХАТЕЛЬНОЙ ЦЕПИ.
1.В НАД и НАДФ рабочей частью является витамин РР - НИКОТИНАМИД.

НАД*2Н + 2е = НАДН+Н
2.В ФАД и ФМН рабочей частью является ФЛАВИИ (компонент витамина В2)

ФАД + 2Н + 2е = ФАДН2
3.УБИХИНОН легко переходит в восстановленную форму KOQ +2Н +2е =KOQ*H2
4.ЦИТОХРОМЫ - это ГЕТЕРОПРОТЕИНЫ. Их белковой частью является ГЕМ, структура которого представляет собой 4 ПИРРОЛЬНЫХ кольца и атом железа, который легко меняет валентность. Также могут включать медь.
ФЕРМЕНТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ.
1.ДГ субстратов находятся в цитоплазме клетки, могут быть в МАТРИКСЕ МИТОХОНДРИЙ.
2.НАДН-ДГ(ФМН).
3.KOQ
4.Q*H2 - ДГ (ЦИТОХРОМЫ в, с 1).
5.ЦИТОХРОМ с.
6.ЦИТОХРОМОКСИДАЗА участвует в передаче электронов на кислород (включает ЦИТОХРОМЫ а, а3).
ФУНКЦИОНИРОВАНИЕ ДЫХАТЕЛЬНОЙ ЦЕПИ.

Полная ЭТЦ - взаимодействие субстрата с НАД. Укороченная ЭТЦ - взаимодействие субстрата с ФАД и последующий транспорт электронов и протонов сразу на КОФЕРМЕНТ Q,
Порядок компонентов дыхательной цепи обусловлен величиной их red-ox потенциалов. Он изменяется от -0,32В до +0,81В
-0,32 характерно для НАДН2
+0,81 характерно для О2.
ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИИАНИЕ.
В дыхательной цепи создаются условия для синтеза АТФ, т.е. выделяется достаточное количество энергии. Процесс образования АТФ из АДФ и Н3РО4 за счёт энергии переноса электронов дыхательной цепи называется ОКИСЛИТЕЛЬНЫМ ФОСФОРИЛИРОВАНИЕМ.
СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ - это процесс образования АТФ из АДФ и Н3РО4 за счёт энергии распада какого-либо субстрата. В дыхательной цепи выделяются 3 пункта, где может образоваться АТФ:
1.НАД® KOQ
2.ЦИТ. в. ® ЦИТ. с
З.ЦИТ. а. ® ЦИТ. A3
НАДН2 — 3 АТФ
ФАДН2 — 2 АТФ
Процесс освобождения АТФ с транспортом электронов в дыхательной цепи называется
СОПРЯЖЕНИЕМ ОКИСЛЕНИЯ И ФОСФОРИЛИРОВАНИЯ. Но может быть разобщение
ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ (свободное окисление), т.е. окисление идёт, а
|
|
|
ФОСФОРИЛИРОВАНИЯ нет, вся энергия выделяется в виде тепла. Это обуславливает
ПИРОГЕННЫЙ эффект ряда лекарственных веществ.
Лекция № 9. Биологическое окисление (продолжение).
1.МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ.
2.АЛЬТЕРНАТИВНЫЕ ПУТИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ.
3.СВОБОДНО-РАДИКАЛЬНОЕ ОКИСЛЕНИЕ.
МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ.
Теория ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ выдвинута английским учёным П. МИТЧЕЛОМ в 1961 г. и названа ХЕМИООСМОТИЧЕСКОЙ ТЕОРИЕЙ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ. Он объяснил процесс синтеза АТФ с биохимической позиции, но его взгляды не получили признания. Однако в последующем его теория подтвердилась, и через 17 лет он был удостоен Нобелевской премии.
Основные положения теории:
1.Мембрана МИТОХОНДРИЙ не проницаема для протонов.
2.Образуется протонный потенциал в процессе транспорта электронов и протонов.
3.Обратный транспорт протонов в МАТРИКС сопряжен с образованием АТФ.
Процесс транспорта электронов происходит во внутренней мембране. Первые реакции окисления происходят в матрице. Протоны переносятся в межмембранное пространство, а электроны продвигаются по дыхательной цепи. В процессе работы дыхательной цепи внутренняя мембрана со стороны матрицы заряжается отрицательно, а со стороны межмембранного пространства положительно. Следовательно, возникает разность потенциалов, градиент концентрации ионов, и, соответственно, градиент РН. Т.о. РН со стороны матрицы будет менее кислая. Во время дыхания создаётся ЭЛЕКТРО-ХИМИЧЕСКИЙ градиент: концентрационный и разности потенциалов. Электрический и концентрационный градиент составляет ПРОТОНДВИЖУЩУЮ силу, которая даёт силу для синтеза АТФ. На определённых участках внутренней мембраны есть протонные каналы, образованные АТФ-СИНТЕТАЗОЙ. Протоны могут проходить обратно в матрицу, при этом образующаяся энергия идёт на синтез АТФ.
УСЛОВИЯ ОБРАЗОВАНИЯ АТФ.
1. Целостность мембраны - непроницаемость её для протонов.
2. Наличие специальных каналов.
3. Движение протонов в матрицу сопровождается выделением энергии, используемой для синтеза АТФ.
|
|
|
Вопрос о том, что позволяет протонам переходить в межмембранное пространство остаётся не вполне ясным.
Основные компоненты ЭТЦ представляют собой интегральные белки и фиксированные в мембране: 1.НАДН-ДГ.
2.QН2-ДГ.
3.ЦИТОХРОМОКСИДАЗА.
4.KOQ не связан с белками.
5.ЦИТОХРОМ с - не фиксирован к мембране.
Выдвигается теория Q-цикла транспорта протонов.
2Н + 2е + KOQ ® KOQ*H2
KOQ*H2 ® KOQ + 2Н + 2е - на наружной поверхности внутренней мембраны.
Т.о. в соответствии с ХЕМООСМОТИЧЕСКОЙ теорией МИТЧЕЛА окисление НАДН2 и ФАДН2 в дыхательной цепи создаёт сначала ЭЛЕКТРОНО-ХИМИЧЕСКИЙ протонный потенциал, градиент концентрации ионов на внутренней мембране, а обратный транспорт протонов через мембрану сопряжен с ФОСФОРИЛИРОВАНИЕМ, т.е. образованием АТФ.
АЛЬТЕРНАТИВНЫЕ ПУТИ БИОЛОГИЧЕСКОГО ОКИСЛЕНИЯ.
В организме возможен и ОКСИГЕНАЗНЫЙ путь биологического окисления. Он не относится к процессам, сопровождающимся выделением энергии, он не снабжает клетку энергией. Ферменты этого пути включают кислород и субстрат. Этот путь характерен для ДЕГИДРАТАЦИИ различных метаболитов, чаще всего чужеродных.
Стадии ОКСИГЕНАЗНОГО ПУТИ:
1.Связывание кислорода с активным центром фермента.
2.Восстановление кислорода и перенос его на субстрат.
Выделяют 2 типа ОКСИГЕНАЗ:
1.ДИОКСИГЕНАЗЫ - ферменты, включающие в субстрат молекулу кислорода.
А + О2 = АО2
В живых тканях этот процесс практически не встречается.
2.МОНООКСИГЕНАЗЫ - они катализируют включение в субстрат 1 атома кислорода, др. атом кислорода восстанавливается до воды. Для реакций катализируемых МОНООКСИГЕНАЗАМИ необходим КОСУБСТРАТ - донор электронов.
А-Н + О2 + ZH2 ® А-ОН + Z + Н2О
Где А-Н - субстрат
ZH2 - КОСУБСТРАТ
А-ОН - окисленный субстрат.
В организме есть несколько видов МОНООКСИГЕНАЗ и прежде всего МИКРОСОМАЛЬНЫЕ МОНООКСИГЕН АЗЫ, содержащие ЦИТОХРОМ Р-450.Т.к. образуется -ОН группа, то реакции называются ещё реакциями ГИДРОКСИЛИРОВАНИЯ. МИКРОСОМАЛЬНАЯ система участвует в деградации многих умеренно токсических соединений, лекарственных веществ. Восстановленным КОСУБСТРАТОМ в этих реакциях является НАДФ*Н2. Этот путь окисления иногда называют ГИДРОКСИЛАЗНЫМ ЦИКЛОМ.
СВОБОДНОЕ РАДИКАЛЬНОЕ ОКИСЛЕНИЕ.
Свободные радикалы - это молекулярные частицы, у которых на внешней оболочке имеется не спаренный электрон. Они могут образовываться: при окислении (отрывании атома водорода)
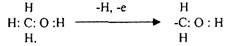
при восстановлении
О2 + е ® О2-
Атомарный кислород имеет на внешнем электронном уровне 2 неспареных электрона. Он
не слишком активный, но может образовывать высоко активные формы.
О2+4е + 4Н ® 2Н2О
Этот процесс, в тканях, идёт постепенно, с переносом 1е на каждом этапе.
О2 + е = 02- - СУПЕРОКСИДНЫЙ АНИОН
2-02 + 2е = 022- - ПЕРОКСИДНЫЙ АНИОН
НО, - ГИДРОКСИЛ РАДИКАЛ
Н2О2, О2-, О22-, ОН, - активные формы кислорода (АФК)
Они образуются в организме при различных физиологических и патологических процессах. Все свободные радикалы в организме классифицируют:
1. Первичные радикалы (О2, N,O). Они образуются в результате ферментативных реакций. Они являются физиологическими. Способствуют образованию РАДИКАЛОБРАЗНЫХ молекул, к которым относятся НООН, они вызывают образование вторичных радикалов.
2. Вторичные радикалы (ОН, ЛИПИДНЫЕ радикалы – L,, LO,, LOO,) Их образование происходит с участием железа (11). Это патологические продукты.
3. Третичные радикалы (АНТИОКСИДАНТЫ) - образуются под влиянием вторичных радикалов.
СУПЕРОКСИДНЫЙ АНИОН легко присоединяет Н+, е. Он хорошо растворяется в жирах, следовательно, следовательно, легко взаимодействует с ЛИПИДАМИ мембран, и особенно хорошо взаимодействует с ПОЛИНЕНАСЫЩЕННЫМИ ЖИРНЫМИ КИСЛОТАМИ, отнимая у них водород.


Этот процесс называется ПЕРЕКИСНЫМ ОКИСЛЕНИЕМ ЛИПИДОВ (ПОЛ). Это патологическое явление, приводящее к нарушению целостности мембран клеток. Процессы свободного радикального окисления идут в норме, но на низком уровне. Поэтому в организме есть система, которая предотвращает ПОЛ - АНТИОКИСЛИТЕЛЬНАЯ СИСТЕМА (АОС), препятствующая образованию свободных радикалов.
Она включает:
1.Фермент - СУПЕРОКСИДДИСМУТАЗА (СОД).
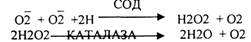
ГЛУТАТИОНПЕРОКСИДАЗА (восстановление Н2О2 за счет окисления ГЛУТАТИОНА).
2.Альфа- ТОКОФЕРРОЛ (вит. Е) - основной не ферментный АНТИОКСИДАНТ.
3.УБИХИНОН.
4.МОЧЕВАЯ К-ТА.
5.БИЛИРУБИН.
6.ГЛУТАТИОН.
7.КОМПЛЕКСОНЫ ЖЕЛЕЗА (связывают железо, потенцирующего образование свободных радикалов).
СЕНЕРГИСТЫ АНТИОКСИДАНТОВ соединения, которые восстанавливают АНТИОКСИДАНТЫ, способствуя возвращению их в активную форму. В организме основным источником свободных радикалов являются фагоциты. При встрече фагоцита с чужеродным субстратом, он прикрепляется к нему и начинает выделять АФК. Они активируют свободно-радикальный процесс ПОЛ, поражают мембрану чужеродного агента, вызывая его гибель. К активации свободных радикалов в организме приводят:
1. НЕДОСТАТОК БИООКСИДАНТОВ.
2. ВНЕШНИЕ ФАКТОРЫ.
3. ХРОНИЧЕСКИЙ СТРЕСС.
4. ГИПОДИНАМИЯ.
5. ИЗБЫТОК ЖИРНОЙ ПИЩИ.
6. МНОГИЕ ПАТОЛОГИЧЕСКИЕ СОСТОЯНИЯ.
Лекция № 10. Обмен углеводов.
1. ОСНОВНЫЕ УГЛЕВОДЫ ЖИВОТНОГО ОРГАНИЗМА, ИХ КЛАССИФИКАЦИЯ И БИОЛОГИЧЕСКАЯ РОЛЬ.
2. ПРЕВРАЩЕНИЕ УГЛЕВОДОВ В ОРГАНАХ ПИЩЕВАРИТЕЛЬНОЙ СИСТЕМЫ.
3. БИОСИНТЕЗ И РАСПАД ГЛИКОГЕНА.
4. ГЛИКОГЕНОВЫЕ БОЛЕЗНИ.
ОСНОВНЫЕ УГЛЕВОДЫ ЖИВОТНОГО ОРГАНИЗМА.
Углеводы - это ПОЛИОКСИКАРБОНИЛЬНЫЕ соединения и их производные.
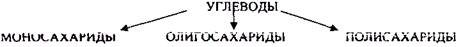
МОНОСАХАРИДЫ: ТРИОЗЫ (ГЛИЦЕРАЛЬДЕГИД, ДИОКСИАЦЕТОН), ТЕТРОЗЫ (ЭРИТРУЛОЗА), ПЕНТОЗЫ (РИБОЗА, ДЕЗОКСИРИБОЗА, КСИЛУЛОЗА), ГЕКСОЗЫ (ГЛЮКОЗА, ГАЛАКТОЗА, ФРУКТОЗА).
ОЛИГОСАХАРИДЫ (в состав молекулы входят 2-12 МОНОСАХАРИДОВ, соединённых между собой): МАЛЬТОЗА, ЛАКТОЗА, САХАРОЗА. ПОЛИСАХАРИДЫ делятся на ГОМОПОЛИСАХАРИДЫ и ГЕТЕРОПОЛИСАХАРИДЫ. ГОМОПОЛИСАХАРИДЫ - КРАХМАЛ, ГЛИКОГЕН. ГЕТЕРОПОЛИСАХАРИДЫ ХОНРОЭТИНСЕРНАЯ К-ТА, ГИАЛУРОНОВАЯ К-ТА, НЕЙРАМИНОВАЯ К-ТА, ГЕПАРИН.
БИОЛОГИЧЕСКАЯ РОЛЬ УВ.
1. ЭНЕРГЕТИЧЕСКАЯ. При окислении 1 гр. УВ до конечных продуктов (СО2 и Н2О) выделяется 4,1-ккал-60-70 % всей калорийности пищи. Суточная потребность в УВ для взрослого человека с массой 60-70 кг составляет около 400-500 гр.
2. Структурная. УВ используется как строительный материал для образования структурных компонентов клеток (ГЛИКОЛИПИДЫ, ГЛИКОПРОТЕИНЫ, ГЕТЕРОПОЛИСАХАРИДЫ межклеточного вещества).
3.Резервная. УВ в виде гликогена могут откладываться в запас.
4. Защитная. ГЛИКОПРОТЕИНЫ принимают участие в образовании антител. ГИАЛУРОНОВАЯ К-ТА препятствует проникновению чужеродных веществ. ГЕТЕРОПОЛИСАХАРИДЫ участвуют в образовании слизи слизистых оболочек дыхательных путей, ЖКТ.
5. Регуляторная. Некоторые гормоны являются ГЛИКОПРОТЕИНАМИ (ТИРИОГЛОБУЛИН)
6.Участвуют в процессах распознавания клеток (СИАЛОВАЯ и НЕЙРОЛИНОВАЯ К-ТЫ).
7 Входя в состав оболочек эритроцитов, определяют группы крови.
8. Участвуют в процессах свёртывания крови, входя в состав ФИБРИНОГЕНА и ПРОТРОМБИНА. Препятствуют свёртыванию крови, входя в состав ГЕПАРИНА.
ПРЕВРАЩЕНИЕ УГЛЕВОДОВ В ОРГАНАХ ПИЩЕВАРИТЕЛЬНОЙ СИСТЕМЫ.
Основными УВ для организма человека являются УВ пищи: крахмал, сахароза, лактоза.
Поступивший с пищей крахмал в ротовой полости будет подвергаться гидролизу под действием альфа -АМИЛАЗЫ слюны. Она расщепляет альфа (1,4)-ГЛИКОЗИДНЫЕ связи. РН оптимум в слабощелочной среде (6,8). Поскольку пища в ротовой полости задерживается недолго, то крахмал здесь переваривается лишь частично. Гидролиз крахмала завершается образованием АМИЛОДЕКСТРИНОВ (с йодом дают фиолетовое окрашивание). Далее пища поступает в желудок. Слизистой оболочкой желудка ГЛИКОЗИДАЗЫ не вырабатываются. В желудке среда резко кислая, поэтому действие альфа -АМИЛАЗЫ прекращается. Однако в более глубоких слоях действие фермента продолжается (пищевой комок полностью желудочным соком не пропитывается), крахмал проходит следующую стадию гидролиза- ЭРИТРОДЕКСТРИНОВ (с йодом дают красное окрашивание). Основным местом переваривания крахмала служит тонкий отдел кишечника. Здесь наиболее важная фаза гидролиза крахмала. В 12 п.к. открываются протоки ПЖЖ. Под действием фермента в её секрете будет идти гидролиз крахмала. Выделяющийся панкреатический сок содержит БИКАРБОНАТЫ, которые нейтрализуют желудочное кислое содержимое. Образующийся при этом Н2СОЗ распадается. СО2 «вспенивает» пищевой комок, способствуя его перемешиванию. Создаётся слабощелочная среда. Катионы натрия и калия способствуют активации панкреатических ГЛИКОЗИДАЗ: альфа -АМИЛАЗЫ, АМИЛО-1,6-ГЛИКОЗИДАЗЫ, ОЛИГО-1,6-ГЛИКОЗИДАЗЫ. Эти ферменты завершают гидролитический разрыв внутренних ГЛИКОЗИДНЫХ связей. ЭРИТРОДЕКСТРИНЫ переходят в ОХРОДЕКСТРИНЫ (с йодом жёлтое окрашивание).
Альфа -АМИЛАЗА завершает разрыв внутренних альфа(1,4)-ГЛИКОЗИДНЫХ связей с образованием ДИСАХАРИДОВ (МАЛЬТОЗ). Альфа(1,6)-ГЛИКОЗИДНЫЕ связи в точках ветвления крахмала гидролитически расщепляются под действием АМИЛО-(1,6)-ГЛИКОЗИДАЗЫ и ОЛИГО-(1,6)-ГЛИКОЗИДАЗЫ, которая является терминальной в этом процессе. Т.о. 3 панкреатических фермента завершают гидролиз крахмала в кишечнике с образованием МАЛЬТОЗ. Образованная МАЛЬТОЗА - временный продукт гидролиза, т.к. она в клетках кишечника быстро гидролизуется под действием МАЛЬТАЗ. Из тех же остатков, которые в молекулах крахмала были соединены альфа(1,6)-ГЛИКОЗИДНЫМИ связями, образуются ДИСАХАРИДЫ -ИЗОМАЛЬТОЗЫ. Они будут гидролизоваться ИЗОМАЛЬТАЗАМИ. В составе пищи в организм человека поступают и ДИСАХАРИДЫ: лактозы и сахарозы, которые подвергаются гидролизу только в тонком кишечнике. В ЭНТЕРОЦИТАХ синтезируются ЛАКТАЗЫ и САХАРАЗЫ, которые осуществляют гидролиз с образованием глюкозы, галактозы, фруктозы.
Продукты полного гидролиза - МОНОСАХАРИДЫ - всасываются в кровь. На этом завершается начальный этап пищеварения. С пищей в организм человека поступает клетчатка, которая в ЖКТ не переваривается, поскольку отсутствуют бета -ГЛИКОЗИДАЗЫ. Однако биологическая роль клетчатки велика: 1.формирование пищевого комка,
2.она раздражает слизистую оболочку ЖКТ, усиливая секрецию желёз.
3.усиливает сокращение кишечника,
4.в толстом кишечнике под действием ферментов условно-патогенной микрофлоры клетчатка подвергается брожению с образованием глюкозы, лактозы и газообразных веществ.
БИОСИНТЕЗ ГЛИКОГЕНА.
Было установлено, что гликоген может синтезироваться практически во всех органах и тканях. Однако наибольшая его концентрация обнаружена в печени (2-6%) и мышцах (0,5-2%). Т.к. мышечная масса велика, то большая часть гликогена содержится в мышцах. Глюкоза из крови легко проникает в клетки органов и тканей, проходя через биологические мембраны клеток. Как только глюкоза заходит в клетку, она запирается в ней в результате первой метаболической реакции - ФОСФОРИЛИРОВАНИЕ в присутствии АТФ и фермента -ГЕКСОКИНАЗЫ. Глюкоза превращается в глюкозо-6-фосфат. Теперь он будет использоваться в АНАБОЛИЧЕСКИХ и КАТАБОЛИЧЕСКИХ реакциях. Глюкоза из клетки может выйти, если в реакции гидролиза при участии глюкозо-6-фосфатазы освободится от остатка фосфорной кислоты. Этот фермент находится в печени, почках, эпителии кишечника. В других органах его нет. Проникновение глюкозы в клетки этих органов и тканей необратимы. Процесс биосинтеза протекает в 4 стадии:


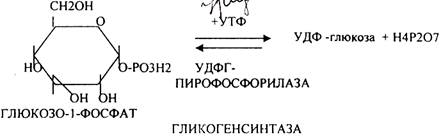


ГЛИКОГЕНСИНТАЗА - ТРАНСФЕРАЗА, которая переносит остатки глюкозы, входящие в УДФ- глюкозу, на ГЛИКОЗИДНУЮ связь остаточного в клетке гликогена, при этом образуется альфа(1,4)-ГЛИКОЗИДНЫЕ связи. Образование альфа(1,6)-ГЛИКОЗИДНЫХ связей в точках ветвления гликогена катализирует специальный ГЛИКОГЕН-ВЕТВЯЩИЙ фермент. Образовавшийся в последней реакции УДФ, превращается в УТФ, при этом поглощается I молекула АТФ. На каждую молекулу глюкозы, включающуюся в структуру гликогена, расходуется 2 молекулы АТФ.Гликогену клетках накапливается во время пищеварения и рассматривается как резервная форма глюкозы, которая используется клетками в промежутках между приёмами пищи.
РАСПАД ГЛИКОГЕНА. Может идти 2 путями:
1. ОСНОВНОЙ ФОСФОРОЛИТИЧЕСКИЙ ПУТЬ
Он протекает в печени, почках, эпителии кишечника. Схематично можно записать в виде 3 реакций.

2.НЕОСНОВНОЙ АМИЛОЛИТИЧЕСКИЙ.
Его доля мала и незначительна. Протекает в печени при участии 3 ферментов: альфа -
АМИЛАЗА, АМИЛО-1,6-ГЛИКОЗИДАЗА, гамма -АМИЛАЗА.
ГЛИКОГЕНОВЫЕ БОЛЕЗНИ.
Это наследственное нарушение обмена гликогена, которое связано с недостатком какого-либо из ферментов, участвующих в синтезе или распаде гликогена. Как правило эта недостаточность выражается либо в снижении активности, либо в полном отсутствии какого либо фермента. ГЛИКОГЕНОЗЫ - болезни, связанные с нарушением процессов распада гликогена, при этом в клетках печени, почек, мышц гликоген накапливается в большом количестве. Клинически проявляются увеличением печени, мышечной слабостью, ГИПОГЛЮКОЗЭМИЕЙ натощак. В норме уровень глюкозы в крови равен 3,3 - 5,5 ммоль/л. Смерть наступает в раннем детском возрасте. Наиболее часто встречаются:
1.болезнь ФЕРСА - ФОСФОРИЛАЗА ПЕЧЕНИ.
2.Болезнь МАК-АРДЛЯ - ФОСФОРИЛАЗА МЫШЦ.
3.Болезнь ПОМПЕ- альфа- 1,4-ГЛИКОЗИДАЗА.
4.Болезнь КОРИ - АМИЛО-1.6-ГЛИКОЗИДАЗА.
5.Болезнь ГИРКЕ - ГЛЮКОЗО-6-ФОСФОТАЗА.
АГЛИКОГЕНОЗЫ характеризуются признаками нарушения синтеза. Клинически проявляются резкой ГИПОГЛЮКОЗЭМИЕЙ натощак, рвотой, судорогами, потерей сознания, углеводное голодание клеток, следовательно, отставание психо-физического развития, смерть в раннем детском возрасте. Наиболее часто встречаются:
1. болезнь ЛЬЮИСА - ГЛИКОГЕНСИНТЕТАЗА.
2. Болезнь АНДЕРСЕНА - ГЛИКОГЕН-ВЕТВЯЩИЙ фермент.
Лекция №11. Обмен углеводов (продолжение).
1. АНАЭРОБНЫЙ ГЛИКОЛИЗ, ХИМИЗМ РЕАКЦИИ И БИОЛОГИЧЕСКАЯ РОЛЬ.
2.АЭРОБНЫЙ ГЛИКОЛИЗ, (ГЕКСОЗОДИФОСФАТНЫЙ ПУТЬ), ХИМИЗМ РЕАКЦИИ И БИОЛОГИЧЕСКАЯ РОЛЬ.
В зависимости от функционального состояния организма, клетки органов и тканей могут находиться в условиях достаточного снабжения кислородом, так и испытывать кислородное голодание. Т.о. катоболизм глюкозы или глюкозного остатка гликогена может рассматриваться с двух позиций:
1.В АНАЭРОБНЫХ УСЛОВИЯХ
2.В АЭРОБНЫХ УСЛОВИЯХ.
АНАЭРОБНЫЙ ГЛИКОЛИЗ протекает в цитоплазме клеток. Окисление глюкозы или глюкозного остатка гликогена всегда завершается образованием конечного продукта этого процесса- молочной кислоты.
Окисление глюкозы и глюкозного остатка гликогена в тканях отличается начальных стадиях превращения, до образования глюкозо-6-фосфата. Дальнейшее окисление с этого этапа в тканях как в АНА-, так и в АЭРОБНЫХ условиях полностью совпадает до стадии образования ПИРУВАТА.
Процесс АНАЭРОБНОГО ГЛИКОЛИЗА сложный и многоступенчатый. Условно его можно
разделить на 2 стадии:
-первая стадия заканчивается образованием из ГЕКСОЗЫ двух ТРИОЗ -ДИОКСИАЦЕТОНФОСФАТА и ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА.
-Вторая стадия наиболее важная. Её называют стадией ГЛИКОЛИТИЧЕСКОЙ ОКСИДОРЕДУКЦИИ. Она сопряжена с образованием АТФ за счёт реакций СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ, окислением ГЛИЦРАЛЬДЕГИД -3-ФОСФАТА, восстановлением ПИРУВАТА до ЛАКТАТА.

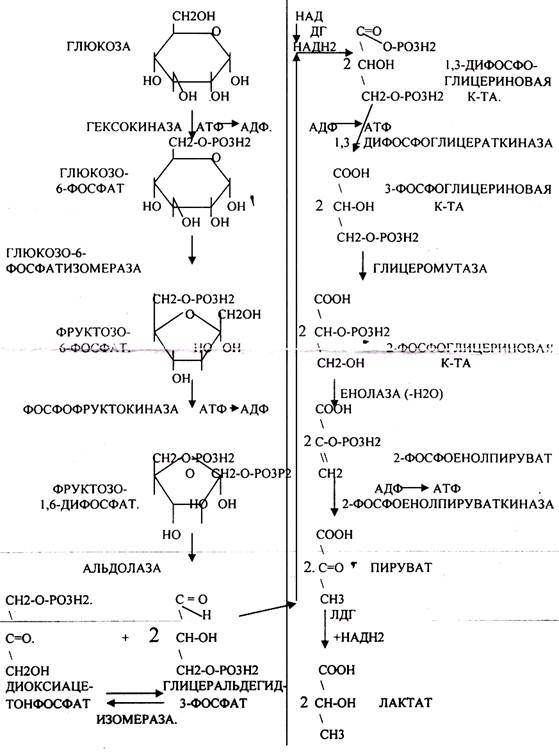
Т.о. окислительный процесс в без кислородных условиях завершается образованием ЛАКТАТА. В процессе превращения глюкозы было израсходовано 2 молекулы АТФ (ГЕКСОКИНАЗНАЯ и ФОСФОФРУКТОКИНАЗНАЯ реакции). С этапа образования ТРИОЗ идёт одновременное их окисление. В результате этих реакций образуется энергия в виде АТФ за счёт реакций СУБСТРАТНОГО ФОСФОРИЛИРОВАНИЯ (ГЛИЦЕРАТКИНАЗНАЯ и ПИРУВАТКИНАЗНАЯ).
На этапе ГЛИКОЛИТИЧЕСКОЙ ОКСИДОРЕДУКЦИИ идёт окисление ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА в присутствии НЗРО4 и НАД- зависимой ДГ. которая на этом этапе восстанавливается до НАДН2. МИТОХОНДРИИ в АНАЭРОБНЫХ условиях блокированы, поэтому НАДН2 находится в среде до тех пор, пока не образуется субстрат, способный принять его. ПВК, принимая НАДН2, восстанавливается с образованием ЛАКТАТА, завершая тем самым внутренний-окислительно-восстановительный этап ГЛИКОЛИЗА. НАД окисленный выделяется и может участвовать в окислительном процессе, выполняя роль переносчиков водорода.
3 реакции ГЛИКОЛИЗА являются необратимыми:
1.ГЕКСОКИНАЗНАЯ.
2.ФОСФОФРУКТОКИНАЗНАЯ.
3.ПИРУВАТКИНАЗНАЯ.
Энергетический эффект глюкозы и глюкозного остатка гликогена:
АТФ = (2*2)-2 = 2 глюкоза
АТФ = (2*2)-1 =3 гликоген
Биологическая роль АНАЭРОБНОГО ГЛИКОЛИЗА энергетическая. АНАЭРОБНЫЙ ГЛИКОЛИЗ является единственным процессом продуцирующим энергию в форме АТФ в клетке в бес кислородных условиях в кризисных ситуациях. А в эритроцитах ГЛИКОЛИЗ является единственным процессом поддерживающим биоэнергетику, для сохранения их функции и целостности.
ГЕКСОЗОДИФОСФАТНЫЙ ПУТЬ - это аэробное превращение глюкозы в тканях. При поступлении кислорода в клетки происходит подавление анаэробного ГЛИКОЛИЗА. При этом понижается потребление глюкозы, блокируется образование ЛАКТАТА. Эффект торможения анаэробного гликолиза дыханием получил название эффекта ПАСТСРА. Процесс окисления начинается в цитоплазме до стадии образования ПИРУВАТА. Затем ПВК поступает в МИТОХОНДРИИ, где в матрице подвергается ОКИСЛИТЕЛЬНОМУ ДЕКАРБОКСИЛИРОВАНИЮ. Образующийся АЦЕТИЛ-КОА поступает для дальнейшего окисления в основной метаболический ЦТК КРЕБСА. С участием ферментов ЦТК и сопряженных с ним ферментов дыхательной цепи происходит образование конечных продуктов (СО2 иН2О) и выделяется 38 АТФ, а при окислении глюкозного остатка гликогена - 39 АТФ. Н2О образуется на этапе превращения:
1. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТ
2. 2-ФОСФОГЛИЦЕРИНОВАЯ К-ТА
3. ПИРУВАТА
4. Альфа- КЕТОГЛУТАРОВАЯ К-ТА
5. СУКЦИНАТ
4. ИЗОЦИТРАТ
7. МАЛАТ
СО2 образуется на этапе превращения:
1. ПИРУВAT
2. ОКСАЛОСУКЦИНАТ
3. Альфа - КЕТОГЛУТАРОВАЯ К-ТА. АТФ образуется:
А. За счёт реакций субстратного ФОСФОРИЛИРОВАНИЯ на этапе превращения:
1. 1,3-ДИФОСФОГЛИЦЕРИНОВАЯ К-ТА
2. 2-ФОСФОЕНОЛПИРУВАТ
3. СУКЦИНИЛ-КОА
В. За счёт реакций ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ на этапе превращения:
1. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТ
2. ПИРУВАТ
3. ИЗОЦИТРАТ
4. альфа -КГК
5. СУКЦИНАТ
6. МАЛАТ.
Энергетический эффект окисления глюкозы и глюкозного остатка гликогена в аэробных условиях:
АТФ = 2*(3+1 +1 +3+12) - 2 = 38 глюкоза
АТФ = 2*(3+1+ 1 +3+12) - 1 =39 гликоген
Лекция № 12.
Обмен углеводов (продолжение).
1.ГЕКСОЗОМОНОФОСФАТНЫЙ ПУТЬ ПРЕВРАЩЕНИЯ УГЛЕВОДОВ В ТКАНЯХ. ХИМИЗМ РЕАКЦИЙ, БИОЛОГИЧЕСКАЯ РОЛЬ.
2.ОСНОВНЫЕ ИСТОЧНИКИ ГЛЮКОЗЫ ДЛЯ ОРГАНИЗМА ЧЕЛОВЕКА, ГЛЮКОНЕОГЕНЕЗ И ЕГО БИОЛОГИЧЕСКАЯ РОЛЬ.
3.ПАТОЛОГИЯ УГЛЕВОДНОГО ОБМЕНА.
ГЕКСОЗОМОНОФОСФАТНЫЙ ПУТЬ (ПЕНТОЗНЫЙ, АПОТОМИЧЕСКИЙ) протекает в цитоплазме клетки и представлен 2 ветвями: окислительной и неокислительной. Особенно активно этот путь протекает в тех органах и тканях, в которых активно синтезируются жиры (печень, почки, жировая и эмбриональная ткань, молочные железы). Биологическая роль этого пути окисления глюкозы связывается прежде всего с производством двух веществ:
1.НАДФ*Н2, который в отличии от НАДН2 не используется вдыхательной цепи МИТОХОНДРИЙ, а поступает клетке для реакций синтеза и восстановления веществ.
2.РИБОЗО-5-ФОСФАТА и др. ПЕНТОЗ, которые используются в клетке для синтеза важнейших биологических молекул: ДНК, РНК, НТФ (АТФ, ГТФ, ЦТФ, ТТФ),Н5КОА, НАД, ФАД).
Следовательно, основная биологическая роль - АНАБОЛИЧЕСКАЯ. Неокислительная стадия ПЕНТОЗНОГО ПУТИ окисления глюкозы даёт субстраты, которые в анаэробных условиях поддерживают ГЛИКОЛИЗ (ФРУКТОЗО-6-ФОСФАТ, ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТ). Т.о. поддерживается биоэнергетика клетки в ГИПОКСИЧЕСКИХ ситуациях. Окислительная стадия представляет 5 реакций и предусматривает образование ПЕНТОЗ. ГЕКСОЗОМОНОФОСФАТНЫЙ путь отличается от ГЕКСОЗОДИФОСФАТНОГО пути с этапа превращения глюкозо-6-фосфата.

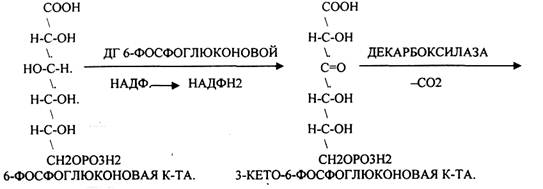
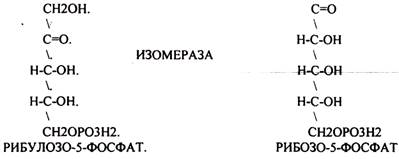
При определенных условиях на этом заканчивается окислительная стадия. Между ПЕНТОЗАМИ устанавливается подвижное равновесие.

Неокислительная стадия ГЕКСОЗОМОНОФОСФАТНОГО пути представлена двумя ТРАНСКЕТЛАЗНЫМИ реакциями и одной ТРАНСАЛЬДОЛАЗНОЙ. Особенно активно эти реакции протекают в анаэробных условиях. В результате этих реакций образуются субстраты для ГЛИКОЛИЗА, а также вещества характерные для ПЕНТОЗНОГО пути.
1. ТРАНСКЕТОЛАЗНЫЕ реакции:
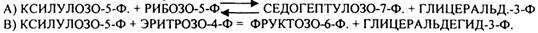
2. ТРАНСАЛЬДОЛАЗНАЯ реакция:
А) СЕДОГЕПТУЛОЗО-7-Ф + ГЛИЦЕРАЛЬД-3-Ф = ФРУКТОЗО-6-Ф + ЭРИТРОЗО-4-Ф.
Было установлено, что за счёт ГЕКСОЗОМОНОФОСФАТНОГО пути клетки на 100% обеспечиваются ПЕНТОЗАМИ, на 50% - молекулами НАДФ*Н2. Баланс окислительной и неокислительной стадий ПЕНТОЗНОГО пути превращения ПЕНТОЗЫ можно записать в виде суммарного уравнение:

Основные источники глюкозы для организма человека:
1. УВ пищи,
2. гликоген тканей
3. ГЛЮКОНЕОГЕНЕЗ.
ГЛЮКОНЕОГЕНЕЗ - это биосинтез глюкозы из не углеводных предшественников, главными из которых являются ПИРУВАТ, ЛАКТАТ, ГЛИЦЕРИН, ряд АК (АСП, ФЕН, АЛА, ТИР, ТРИ, ВАЛ, ЛЕЙ, ИЛЕ, МЕТ, ПРО, ГИС, АРГ), тем или иным путем превращающиеся в метаболит ЦТК - ФУМАРАТ, который в дальнейшем превращается в ЩУК. Другие АК превращаются в ПИРУВАТ –субстрат ГЛЮЮКОНЕОГЕНЕЗА, ГЛЮКОНЕОГЕНЕЗ возможен не во всех тканях. Главным местом синтеза глюкозы является печень, в меньшей степени процесс идёт в почках и слизистой кишечника. ГЛЮКОНЕОГЕНЕЗ обеспечивает синтез глюкозы, а также возврат ЛАКТАТ А, образованного в реакциях анаэробного ГЛИКОЛИЗА, в клеточный фонд углеводов. За счет этого процесса поддерживается уровень глюкозы при углеводном голодании, сахарном диабете. Большинство реакций ГЛЮКОНЕОГЕНЕЗА представляют собой обратные реакции ГЛИКОЛИЗУ, за исключением трёх (ГЕКСОКИНАЗНОЙ, ФОСФОФРУКТОКИНАЗНОЙ, ПИРУВАТКИНАЗНОЙ), которые при ГЛКЖОНЕОГЕНЕЗЕ имеют обходные пути. Первая обходная реакция ГЛЮКОНЕОГЕНЕЗА связана с образованием 2-ФОСФОЕНОЛ ПВК и протекает в две стадии:


Вторая обходная реакция связана с образованием фруктозо-6-фосфата.

Образовавшаяся глюкоза может вновь использоваться клетками как пластический и энергетический материал, откладываться про запас в виде гликогена. В организме взрослого человека за сутки может быть образованно 80 гр. глюкозы.
ПАТОЛОГИЯ УГЛЕВОДНОГО ОБМЕНА.
Глюкоза является основным углеводом пищи, который используется всеми тканями для метаболизма. Концентрация глюкозы в крови для взрослого человека с массой 70 кг. составляет 3,3-5,5 ммоль/л.
Концентрация глюкозы в крови поддерживается за счёт УВ пищи, гликогена тканей и ГЛЮКОНЕОГЕНЕЗА и зависит от содержания УВ в пище, частоты приёма пищи и интенсивности затрат энергии. Нарушение углеводного обмена может быть на различных этапах. Объективными показателями этих нарушений является нарушение доступных биологических сред на содержание глюкозы. ГИПО-, ГИПЕРГЛЮКОЗЭМИЯ, ГЛЮКОЗУРИЯ является показателями углеводного иомена. ГЛЮКОЗУРИЯ возможна в том случае, если превышается величина почечного порога больше 10 ммоль/л.
Наиболее часто нарушения углеводного обмена возможны на следующих этапах:
1.на этапе поступления углеводов с пищей. Причины, которые могут вести к АЛИМЕНТАРНОМУ ОЖИРЕНИЮ, связаны прежде всего с употреблением пищи богатой углеводами и малоподвижным образом жизни, когда интенсивность окисления понижается. Большая нагрузка углеводов ведёт к переполнению резервом гликогена клеток печени, мышц, развитию ГИПЕРГЛЮКОЗЕМИИ, ГЛЮКОЗУРИИ, усиленному биосинтезу жира, развитию ожирения.
2.При поражении слизистых оболочек ЖКТ. При поражении слизистой желудка нарушается выработка соляной кислоты. Она обладает антибактериальным действием. Поступающие с пищей углеводы при недостатке соляной кислоты под действием ферментов микрофлоры сбраживаются с образованием ЛАКТАТА, что создаёт благоприятные условия для развития анаэробной микрофлоры и расстройства пищеварения в целом. При поражении слизистой оболочки тонкого отдела кишечника нарушается всасывание и гидролиз ДИСАХАРИДОВ пищи: переваривание МАЛЬТОЗ, ЛАКТОЗ, САХАРОЗ, а также транспорт глюкозы, галактозы, фруктозы через БИОМЕМБРАНУ ЭНТЕРОЦИТОВ в капиллярную сеть. При поражении ПЖЖ нарушается переваривание гликогена, крахмала пищи под влиянием ферментов.
Наиболее грозным заболеванием, ведущим к нарушению углеводного обмена, является сахарный диабет. В ПЖЖ в В -клетках синтезируется белок - инсулин, который обеспечивает транспорт глюкозы из крови в ткани. В случае недостаточной выработки инсулина развивается ГИПЕРГЛЮКОЗЕМИЯ, ГЛЮКОЗУРИЯ, КЕТОНУРИЯ. В клетках развивается энергетический голод, который компенсируется за счёт процессов ГЛЮКОНЕОГЕНЕЗА и усиления процессов окисления белков и жиров, что сопровождается избыточной продукцией АЦЕТИЛ-КОА, NH3. NH3 токсичный продукт, для связывания которого откликаются основные КЕТОКИСЛОТЫ цикла КРЕБСА, а это в свою очередь понижает интенсивность окислительных процессов и создаёт предпосылки для конденсации АЦЕТИЛ-КОА и образования кетоновых тел (АЦЕТОУКСУСНАЯ К-ТА, АЦЕТОН, бета -ГИДРОКСИМАСЛЯНАЯ К-ТА).
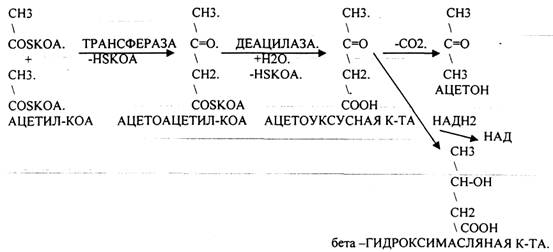
При поражении печени нарушается процесс биосинтеза и распада гликогена. Наследственные заболевания наблюдаются при генетических дефектах ферментов, участвующих в метаболизме углеводов. Наиболее часто встречаются ГЛИКОГЕНОЗЫ (ГИРКЕ, ПОМПЕ) и АГЛИКОГЕНОЗЫ (ЛЬЮИСА, АНДЕРСЕНА), которые связаны с недостаточной активностью или полным отсутствием ферментов, участвующих в распаде или синтезе гликогена. У детей встречается АЛАКТОЗИЯ - непереносимость лактозы в виду генетического дефекта ЛАКТАЗЫ ЭНТЕРОЦИТОВ. Наблюдается вздутие живота, обезвоживание, резкое похудание. Лечение заключается в замене лактозы на другие сахара.
Лекция.№ 13. Обмен ЛИПИДОВ.
1.ЛИПИДЫ, ИХ КЛАССИФИКАЦИЯ И БИОЛОГИЧЕСКАЯ РОЛЬ.
2.ПРЕВРАЩЕНИЕ ЛИПИДОВ В ОРГАНАХ ПИЩЕВАРЕНИЯ.
З.ЖЕЛЧНЫЕ КИСЛОТЫ, ИХ БИОЛОГИЧЕСКАЯ РОЛЬ. РЕСИНТЕЗ ЖИРА В СТЕНКАХ
КИШЕЧНИКА.
ЛИПИДАМИ называются сложные органические вещества биологической природы нерастворимые в воде, но растворимые в органических растворителях. ЛИПИДЫ являются основным продуктом питания. Они поступают в организм с продуктами растительного и животного происхождения. Суточная потребность в ЛИПИДАХ для взрослого человека составляет 80-100 гр.

Воска - это сложные эфиры одно- или двухатомных спиртов с количеством углеводных звеньев в цепи 16-35 и ВЖК. Они входят в состав ЛИПИДОВ, покрывающих листья и плоды растений, шерсть животных, перья птиц. К природным воскам относятся пчелиный воск, спермацет, ланолин. В организме человека ЛИПИДЫ представлены:
1.структурными липидами.
2.резервными липидами.
3.свободными липидами. — хиломикроны,
- липопротеины низкой плотности (лпнп),
- липопротеины очень низкой плотности (лпонп),
- липопротеины высокой плотности (лпвп).
ЛИПИДЫ - трудно растворимые в воде вещества, поэтому для транспорта их кровью нужны —специальные-транспортные частицы. Ими являются ЛИПОПРОТЕИНЫ крови, где роль стабилизатора выполняют белки. ЛИПОПРОТЕИНЫ осуществляют транспорт ЛИПИДОВ от органов и тканей, где они синтезируются к местам их потребления. С их помощью осуществляется транспорт ВЖК и жирорастворимых витаминов A, D, Е, К..
БИОЛОГИЧЕСКАЯ РОЛЬ ЛИПИДОВ.
1.Структурная. ЛИПИДЫ являются обязательным структурным компонентом биологических мембран клеток.
2.Резервная. ЛИПИДЫ могут откладываться в запас.
3.Энергетическая. Было установлено, что при окислении 1 гр. ЛИПИДОВ до конечных продуктов выделяется 9,3 ккал энергии.
4.Механическая. ЛИПИДЫ подкожной жировой клетчатки, соединительной ткани предохраняют внутренние органы от механических повреждений.
5.Теплоизолирующая. Защищают организм от переохлаждения и перегревания.
6.Транспортная. ЛИПИДЫ мембран клеток участвуют в транспорте катионов.
7.Регуляторная. Некоторые гормоны являются СТЕРОИДАМИ (АНДРОГЕНЫ, ЭСТРОГЕНЫ, ГЛЮКО- и МИНЕРАЛОКОРТИКОИДЫ), «Местные» гормоны - ПРОСТАГЛАНДИНЫ, ПРОСТАЦИКЛИНЫ, тромбоксаны, лейкотриены образуются в организме из ПОЛИНЕНАСЫЩЕННЫХ ВЖК, входящих в состав ЛИПИДОВ.
8.Участвуют в передаче нервного импульса.
9.Являются источником эндогенной воды. При окислении 100 гр. ЛИПИДОВ выделяется 107гр эндогенной воды.
10.Растворяющая роль. В ЛИПИДАХ растворяются витамины A, D, E, К.
11.Питательная. С пищей в организм поступают незаменимые ВЖК, которые имеют 2 и более связи (ЛИНОЛЕВАЯ, ЛИНОЛЕНОВАЯ, АРАХИДОНОВАЯ).
БИОЛОГИЧЕСКАЯ РОЛЬ ПОЛИНЕНАСЫЩЕННЫХ ВЖК:
1. Они являются обязательным структурным компонентом мембран клеток.
2. Являются источником гормон подобных веществ.
3. Стимулируют синтез желчных кислот в печени.
4. Предупреждают развитие атеросклероза, ограничивая всасывание холестерина пищи в кишечнике, тормозя образование АТЕРОГЕННОЙ фракции ЛИПОПРОТЕИНОВ.
5. Понижают свёртываемость крови и уменьшают возможность тромб образования.
6. Повышают защитные силы организма.
ПЕРЕВАРИВАНИЕ ЛИПИДОВ.
Поступающие с пищей ЛИПИДЫ в ротовой полости подвергаются только механической переработке. ЛИПОЛИТИЧЕСКИЕ ферменты - ЭСТЕРАЗЫ - в ротовой полости не образуются. Переваривание жиров у взрослого человека будет происходить в кишечнике, где для этого имеются все условия:
1. Наличие желчных кислот.
2. Наличие ферментов.
3. Оптимальная рН среды.
У детей до 1 года в кишечнике выделяется ЛИПАЗА, рН оптимум которой = 5-5,5. Под влиянием этого фермента расщепляются только жиры молока. У взрослого человека она не активна, т.к. рН желудочного содержимого =1,5 - 2,5. Следовательно, переваривание жиров в желудке не происходит (в норме).
Переваривание ЛИПИДОВ пищи в кишечнике происходит при наличии желчных кислот, образованных печенью, и ЛИПОЛИТИЧЕСКИХ ферментов ПЖЖ. При поступлении пищи из желудка в двенадцатиперстную кишку в слизистой оболочке тонкой кишки начинают выделяться регуляторы: СЕКРЕТИН, ХОЛЕЦИСТОКИНИН, ХИМОДЕНИН, ИНТЕРОКЛИИН. Они обеспечивают:
-образование желчи в печени,
-сокращение желчного пузыря,
-выделение панкреатического сока,
-секрецию желез тонкого отдела кишечника. Всё это в целом обеспечивает быстрое переваривание пищи.
Особую роль в переваривании играют желчные кислоты. Все они образуются в печени и являются конечным продуктом окисления холестерина в организме. В основе их строения лежит структура ЦИКЛОПЕНТАНПЕРГИДРОФЕНАНТРЕН.

По своей химической природе все желчные кислоты являются производными ХОЛЕВОЙ К-ТЫ, у которой в 3, 7, 12 положениях имеются ОКСИГРУППЫ. Если у ХОЛЕВОЙ кислоты присутствует две группы в 3 и 7 положениях, то её называют ХЕНОДЕЗОКСИХОЛЕВОЙ. Если присутствует две группы в 3 и 12 положении, то она называется ДЕЗОКСИХОЛЕВОЙ. Если одна группа в 3 положении, кислота называется ЛИТОХОЛЕВАЯ.
БИОЛОГИЧЕСКАЯ РОЛЬ ЖЕЛЧНЫХ КИСЛОТ:
1. Эмульгируют пищевые жиры.
2. Активируют ЛИПОЛИТИЧЕСКИЕ ферменты.
3. Выполняют роль переносчиков трудно растворимых в воде продуктов гидролиза жира и жирорастворимых витаминов A, D, Е, К.
При ЭМУЛЬГИРОВАНИИ жир дробится на мелкие частички. Желчные кислоты адсорбируются на поверхности жира, значительно уменьшает поверхностное натяжение, при этом жир дробится на частички, которые вновь обволакиваются желчными кислотами, препятствуя их слиянию. В результате происходит стабилизация жира и значительно увеличивается поверхность контактов с ЛИПОЛИТИЧЕСКИМИ ферментами. Стабилизированная эмульсия жира далее подвергается гидролизу под влиянием панкреатических ферментов (ЛИПАЗ, ФОСФОЛИПАЗ, ХОЛЕСТЕРОЛЭСТЕРАЗ).
В переваривании жира принимает участие и КОЛИПАЗЫ кишечника. Помогают гидролизу жира ионы кальция, которые образуют комплексы со свободными ВЖК.

Т.о. в результате гидролиза пищевого жира образуются глицерины, холестерины, ВЖК, фосфаты, азотистые основания. Необходимо отметить, что в расщеплении жиров принимают участие и кишечные ЛИПАЗЫ, но их активность невысока, к тому же они расщепляют только МОНОГЛИЦЕРИДЫ и не действуют на ДИ- и ТРИГЛИЦЕРИДЫ. Установлено, что всасывание продуктов гидролиза жира имеет свою особенность. Легко всасываются слизистой кишечника спирты, фосфаты, АК, коротко цепочные ВЖК, азотистые основания. Трудно растворимые в воде продукты гидролиза (холестерин, ВЖК, МОНОГЛИЦЕРИДЫ), жирорастворимые витамины всасываются только в комплексе с желчными кислотами. Эти комплексы называются ХОЛЕИНОВЫМИ. В таком виде трудно растворимые в воде соединения проходят через мембраны ЭНТЕРОЦИТОВ. В этих клетках ворсинок кишечника происходит их распад. При этом желчные кислоты сразу же поступают в ток крови и через систему воротной вены доставляются в печень. Оттуда они в составе желчи вновь попадают в кишечник и могут участвовать в новом акте переваривания жира, либо удаляются из организма в составе каловых масс – КОПРОСТЕРИН. Установлено, что обязательный фонд желчных кислот у взрослого человека составляет 2,8 -3,5гр., при этом они совершают 5-6 оборотов в сутки за счёт печёночно-кишечной циркуляции. После того как продукты гидролиза жира поступили в ЭНТЕРОЦИТЫ, в стенке кишечника начинают синтезироваться жиры, специфические для данного организма, которые по своему строению отличаются от пищевого жира. Механизм синтеза жира в стенке кишечника сводится к следующему: Сначала происходит активация глицерина и ВЖК затем последовательно будет происходить АЦИЛИРОВАНИЕ альфа -ГЛИЦЕРОФОСФАТА с образованием МОНО- и ДИГЛИЦЕРИДОВ. Активная форма ДИГЛИЦЕРИДА - ФОСФАТИДНАЯ К-ТА занимает центральное место в синтезе жира к стенке кишечника. Из неё после активации в присутствии ЦТФ образуется ЦДФ -ДИАЦИЛГЛИЦЕРИД, который даёт начало сложным жирам.

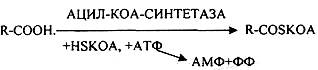

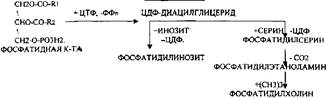
При укусе змей повышается активность ФОСФОРИЛАЗЫ А2. При этом в положении С2 у ФОСФАТИДИЛХОЛИНОВ и ФОСФАТИДИЛЭТАНОЛАМИНОВ отщепляется ПОЛИНЕНАСЫЩЕНЫЕ ВЖК и образуются токсические соединения -ЛИЗОФОСФОЛИПИДЫ, обладающие ГЕМОЛИТИЧЕСКИМ действием.
Лекция № 14. Обмен ЛИПИДОВ (продолжение).
1.ТРАНСПОРТНЫЕ ЛИПОПРОТЕИНЫ КРОВИ. СОСТАВ И БИОЛОГИЧЕСКАЯ РОЛЬ. 2.ПРОСТАГЛАНДИНЫ, ПРОСТАЦИКЛИНЫ, ТРОМБОКСАНЫ, ЛЕЙКОТРИЕНЫ. МЕХАНИЗМ ИХ ОБРАЗОВАНИЯ И БИОЛОГИЧЕСКАЯ РОЛЬ.
3.ОКИСЛЕНИЕ ГЛИЦЕРИНА И ВЖК В ТКАНЯХ.
ЛИПИДЫ являются нерастворимыми в воде соединениями, поэтому для их переноса кровью необходимы специальные переносчики, которые растворимы в воде. Такими транспортными формами являются ЛИПОПРОТЕИНЫ. Они относятся к свободным ЛИПИДАМ. Синтезированный жир в стенке кишечника, либо жир синтезированный в других тканях органах может быть транспортирован кровью лишь после включения в состав ЛИПОПРОТЕИНОВ, где роль стабилизатора играют белки.
По своему строению мицеллы ЛИПОПРОТЕИНЫ имеют наружный слой и ядро. Наружный слой формируется из БЕЛКОВ, ФОСФОЛИПИДОВ и ХОЛЕСТЕРИНА, которые имеют гидрофильные полярные группы и проявляют сродство к воде. Ядро состоит из ТРИГЛИЦЕРИДОВ, ЭФИРОВ ХОЛЕСТЕРИНА, ВЖК, витаминов A, D, Е, К. Т.о. нерастворимые жиры легко транспортируются по всему организму после синтеза в стенке кишечника, а также синтеза в других тканях между клетками, которые их синтезируют и используют.
Выделяют 4 класса ЛИПОПРОТЕИНОВ крови, которые отличаются друг от друга по своему химическому состоянию, размерам мицелл и транспортируемым жирам. Поскольку они имеют различную скорость оседания в растворе поваренной соли, их разделяют на:
1. ХИЛОМИКРОНЫ. Образуются в стенке кишечника и имеют самый крупный размер частиц.
2. ЛПОНП. Синтезируются в стенке кишечника и печени.
3. ЛПНП. Образуются в эндотелии капилляров из ЛПОНП.
4. ЛПВП. Образуются в стенке кишечника и печени.
Т.о. транспортные ЛП крови синтезируются двумя видами клеток - ЭНТЕРОЦИТАМИ и
ГЕПАТОЦИТАМИ. Было установлено, что ЛП крови при электрофорезе белков движутся в зоне
альфа и бета -ГЛОБУЛИНОВ, поэтому их по электрофоретической подвижности ещё
обозначают как:
Пре бета- ЛП - ЛПОНП,
Бета-ЛП-ЛПНП,
Альфа-ЛП-ЛПВП.
ХИЛОМИКРОНЫ как самые крупные частицы при электрофорезе остаются на старте.
Максимальная их концентрация достигается к 4 - 6 часам после приёма пищи. Расщепляются они
под действием фермента - ЛИПОПРОТЕИДЛИПАЗЫ, которая образуется в печени, легких,
эндотелии сосудов, жировой ткани.
Принято считать, что ХИЛОМИКРОНЫ отсутствуют в крови натощак и появляются только
после приёма пищи. В основном они транспортируют ТРИГЛИЦЕРИДЫ (83 - 85 %).
ЛПОНП и ЛПНП в основном транспортируют холестерин и его эфиры в клетки органов и
тканей. Эти фракции относятся к АТЕРОГЕННЫМ. ЛПВП в основном осуществляют транспорт ФОСФОЛИПИДОВ и ХОЛЕСТЕРИНА. Холестерин транспортируется в печень для последующего окисления с образованием желчных кислот и выделяется из организма в виде КОПРОСТЕРИНОВ. Эту фракцию называются АНТИАТЕРОГЕННОЙ.
Распадаются ЛИПОПРОТЕИНЫ крови:
ХИЛОМИКРОНЫ - под действием ЛИПОПРОТЕИДЛИПАЗЫ печени, жировой ткани, эндотелия капилляров. Продукты гидролиза вовлекаются в клеточный метаболизм. ЛПНП и ЛПВП путём эндоцитоза поглощаются клетками печени, почек, надпочечников, жировой ткани и кишечника, разрушаются в ЛИЗОСОМАХ и МИКРОСОМАХ.
ПРОСТАГЛАНДИНЫ, ПРОСТАЦИКЛИНЫ, ТР0МБОКСАНЫ, относящиеся к ПРОСТАНОИДАМ, а также ЛЕЙКОТРИЕНЫ являются гормон подобными веществами, которые в организме человека образуются из ЭССЕНЦИАЛЬНЫХ ВЖК. Главным их предшественником являются АРАХИДОНОВАЯ кислота (С19Н31СООН). Она не может существовать в клетке в свободном виде. Она очень активная и как только, выделяется в результате гидролиза, сразу же включается в клеточный метаболизм - образование гормон подобных веществ.
В настоящее время установлено, что они могут образовываться практически во всех клетках организма, за исключением эритроцитов. Образуются они в микро-количествах и по мере необходимости. Свой биологический эффект они оказывают в клетках тех органов и тканей, в которых образуются. Они выполняют роль местных гормонов, которые координируют функцию соседних клеток или удалённых на незначительные расстояния друг от друга органов. Все эти
вещества коротко живущие, т.е. они имеют период полураспада от нескольких секунд
(ТРОМБОКСАНЫ) до 20 минут (ПРОСТАГЛАНДИНЫ). Выполнив свою роль, они инактивируются и выводятся из организма с мочой. Биосинтез этих соединений начинается с того момента, когда из ФОСФОЛИПИДА под действием ФОСФОЛИПАЗЫ А2 высвобождается АРАХИДОНОВАЯ кислота. Центральные реакции метаболизма кислоты катализирует фермент: ЦИКЛООКСИГЕНАЗА. а в лейкоцитах ЛИПООКСИГЕНАЗА. В результате реакции синтеза в структуру АРАИДОНОВОЙ кислоты включается молекула кислорода. В случае образования ПРОСТАНОИДОВ происходит циклизация. ПРОСТАГЛАНДИНЫ и ПРОСТАЦИКЛИНЫ представляют собой пяти-членные циклы, ТРОМБОКСАНЫ - шести членные циклы, ЛЕЙКОТРИЕНЫ - ненасыщенные производные, ациклические соединения АРАХИДОНОВОЙ К-ТЫ.
Биологическая роль:
1.ПРОСТАГЛАНДИНЫ:
A) В эндокринных железах стимулируют образование гормонов (щитовидная железа, ПЖЖ, надпочечники).
Б) В жировой ткани тормозят ЛИПОЛИЗ.
B) Регулируют сокращение гладких мышц кишечника, бронхов, матки. Г) Оказывают влияние на сокращение миокарда.
Д) Регулируют кровоток в почках, контролируют выведение электролитов и воды с мочой.
Е) Регулируют тромб-образование и проницаемость капилляров.
Ж) В ЦНС раздражают центры терморегуляции, вызывая повышение температуры тела -
лихорадку.
3) Повышая чувствительность нервных окончаний к ГИСТАМИНУ, они вызывают боль.
2.ПРОСТАЦИКЛИНЫ образуются в сердце и сосудах. Препятствуют образованию тромбов,
способствуют расширению сосудов, понижению артериального давления.
3.ТРОМБОКСАНЫ образуются из тучных клеток и тромбоцитов. Они запускают механизм
тромб образования, способствуя слипанию тромбоцитов.
4.ЛЕЙКОТРИЕНЫ. Их биологическая роль связывается с воспалительными реакциями,
аллергическими реакциями и иммунитетом. Они способствуют прилипанию лейкоцитов к стенке
сосудов в местах воспаления. Они способствуют сокращению гладкой мускулатуры дыхательных
путей, ЖКТ. Регулируя тонус сосудов, они вызывают их сужение, повышение АД, стимулируют сокращение
коронарных сосудов.

Основную массу ЛИПИДОВ организма человека составляют нейтральные жиры, которые в клетках находятся в виде включений. Период обновления ТРИГЛИЦЕРИДОВ в разных тканях составляет от 2 до 18 суток. В клетках постоянно идут процессы распада и синтеза жиров. Распад жиров в клетках происходит в лизосомах, меньше в микросомах и цитоплазме при участии тканевых ЭСТЕРАЗ. В результате гидролиза жира образуются общие метаболиты: глицерины и ВЖК, окисление которых сопровождается образованием конечных продуктов -воды и углекислого газа -и выделением энергии в форме АТФ. Окисление глицеринов в тканях тесно связано с ГЛИКОЛИЗОМ, в который вовлекаются метаболиты обмена глицерина по следующей схеме:

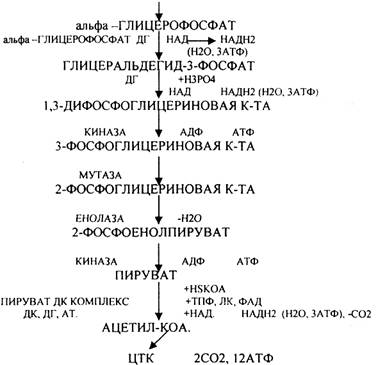
Т.о. при окислении глицерина образовались конечные продукты:
Н2О на этапе превращения:
1. альфа -ГЛИЦЕРОФОСФАТА
2. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА
3. 2-ФОСФОГЛИЦЕРИНОВОЙ К-ТЫ
4. ПВК
5. ИЗОЦИТРАТА
6. Альфа-КЕТОГЛУТАРАТА
7. СУКЦИНАТА
8. МАЛАТА
СО2 на этапе превращения:
1. ПВК
2. ОКСАЛОСУКЦИНАТА
3. Альфа-КЕТОГЛУТАРАТА АТФ на этапе превращения:
1. альфа -ГЛИЦЕРОФОСФАТА
2. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА
3. 1,3-ДИФОСФОГЛИЦЕРИНОВОЙ К-ТЫ (СУБСТРАТНОЕФОСФОРИЛИРОВАНИЕ)
4. 2-ФОСФОЕНОЛПИРУВАТА (СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ)
6. ИЗОЦИТРАТА
7. Альфа-КЕТОГЛУТАРАТА
8. СУКЦИНИЛ-КОА (СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ)
9. СУКЦИНАТА
10. МАЛАТА
АТФ = (3+3+1 + 1+3+12) -1 =22
Окисление ВЖК в тканях изучалось Ф. КНООПОМ (1904г.), который назвал окисление ВЖК бета- окислением. Он показал, что процесс этот циклический, что все ВЖК, имеющие чётное количество углеродных звеньев в цепи обязательно проходят окисление, когда цепь периодически укорачивается на 2 углеродных звена. Последняя стадия окисления - стадия превращения масляной кислоты имеет свои особенности, когда в результате 1 цикла окисления образуется 2 молекулы АЦЕТИЛ-КОА. Одна проходит окисление с выделением 5 АТФ, а другая нет.
В 1949г. А. ЛЕНИНДЖЕР установил, что бета-окисление ВЖК происходит в МИТОХОНДРИЯХ. Д. ЛИНЕН (1954г.) детально описал все стадии бета-окисления.
В настоящее время бета-окисление называют ЦИКЛОМ КНООПА - ЛИНЕНА. Установлено, что процесс бета -окисления начинается в цитоплазме клеток с активации ВЖК. Мембрана МИТОХОНДРИЙ для ВЖК не проницаема. Транспорт ВЖК внутрь возможно только при участии азотистого основания - КАРНИТИНА. АЦИТИЛ-КОА в цитоплазме соединяется с КАРНИТИНОМ при участии фермента АЦЕТИЛ-КОА-КАРНИТИНТРАНСФЕРАЗЫ. Образуется комплекс, который легко проникает через мембрану. В межмембранном пространстве уже при участии МИТОХОНДРИАЛЬНОЙ ТРАНСФЕРАЗЫ комплекс распадается. КАРНИТИН возвращается в цитоплазму, а ВЖК в матрице подвергается окислению.

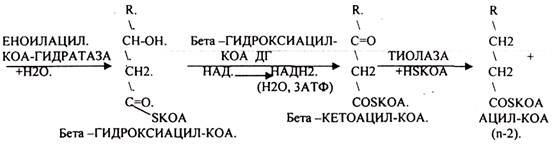

Т.о. завершая 1 цикл бега -окисления ВЖК, в результате которого ВЖК укоротилось на 2 углеродных звена. При бета -окислении выделилось 5АТФ и 12АТФ выделилось при окислении АЦЕИЛ-КОА в ЦТК и сопряженных с ним ферментов дыхательной цепи. Окисление ВЖК будет происходить циклически одинаково, но только до последней стадии - стадии превращения масляной кислоты (БУТИРИЛ-КОА), которая имеет свои особенности. Их надо учитывать при подсчёте энергетического эффекта окисления ВЖК, когда в результате одного цикла образуется 2 молекулы АЦЕТИЛ-КОА, одна из них проходила бета -окисление с выделением 5АТФ, а другая нет.


Энергетический эффект окисления ВЖК: АТФ = n/2 * 17 - 6, где n - число углеродных звеньев в цепи ВЖК, 17 - количество молекул АТФ, которые выделяются в результате окисления 2 углеродных звеньев цепи до конечных продуктов 5АТФ+12АТФ, 6 - то количество АТФ, которое не выделяется, поскольку 1 АТФ тратится на активацию ВЖК, а 5 АТФ не выделяются на последнем этапе - превращения молочной кислоты.
ВЖК, имеющие нечётное количество углеродных звеньев, поступают в организм человека в составе пищи. Окисление таких ВЖК происходит также как и ВЖК, имеющих чётное количество углеродных звеньев в цепи, но только до последней стадии - стадии превращения ПРОПИОНИЛ-КОА. которая имеет свои особенности:
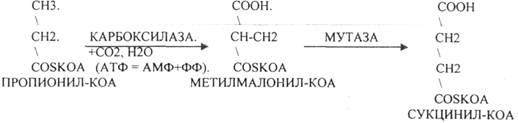
Т.о. образованная молекула СУКЦИНИЛ-КОА, которая для дальнейшего окисления в МИТОХОНДРИЯХ поступает в ЦТК КРЕБСА, одним из основных субстратов которого она является.
Лекция № 15.
Обмен ЛИПИДОВ (продолжение).
1.БИОСИНТЕЗ ВЖК В ТКАНЯХ, ХИМИЗМ РЕАКЦИЙ, БИОЛОГИЧЕСКАЯ РОЛЬ. 2.ХОЛЕСТЕРИН, БИОЛОГИЧЕСКАЯ РОЛЬ, БИОСИНТЕЗ, ОКИСЛЕНИЕ. 3.ПАТОЛОГИЯ ЛИПИДНОГО ОБМЕНА.
Биосинтез ВЖК протекает в ЭПС клеток. Исходным материалом для синтеза заменимых ВЖК является АЦЁТИЛ-КОА, который поступает для биосинтеза при распаде белков, жиров и углеводов.
Условия для биосинтеза ВЖК:
1.Наличие АТФ, СО2, Н2О, НАДФ*Н2, поступающий из ГЕКСОЗОМОНОФОСФАТНОГО пути превращения глюкозы.
2.Наличие специальных белков-переносчиков (HS -АПБ). 3.Наличие специальных ферментов синтеза.
Процесс биосинтеза циклический. Каждый цикл включает в себя 6 этапов. АЦЕТИЛ-КОА используется на первом этапе, как «затравка» синтеза.
Первый этап. Этап образования 3-углеродного соединения - МАЛОНИЛ-КОА.
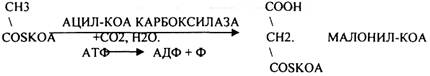
Второй этап. Этап переноса МАЛОНИЛА и АЦЕТИЛА на специальные белки - HS-АПБ.

Третий этап. Этап конденсации МАЛОНИЛА-АПБ и АЦЕТИЛА-АПБ с участием ТРАНСФЕР АЗЫ - СИНТАЗЫ.
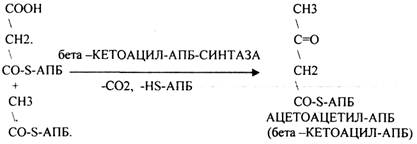
Четвёртый этап. Этап восстановления бета -КЕТОАЦИЛ-АПБ.
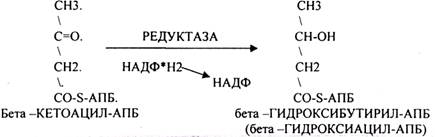
Пятый этап. Этап ДЕГИДРАТАЦИИ бета-ГИДРОКСИАЦИЛ-АПБ.

Шестой этап. Этап восстановления ЕНОИЛАЦИЛ-АПБ.
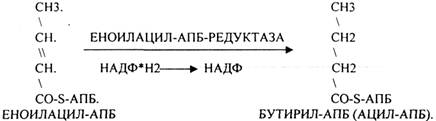
Т.о. завершается 1 цикл синтеза ВЖК образованием масляной кислоты (БУТИРИЛ-АПБ). В дальнейшем последовательно и циклично к 4-углеродному фрагменту будут присоединяться молекулы МАЛОНИЛ-КОА. Для подсчёта количества циклов синтеза ВЖК, подсчёта молекул АТФ, МАЛОНИЛ-КОА можно пользоваться формулой: N/2 - 1, где N-это число углеродных звеньев в молекуле ВЖК. Завершается биосинтез любой ВЖК в тканях ДЕАЦИЛАЗНОЙ реакцией.
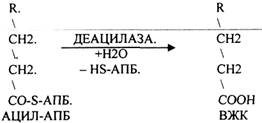
Так в организме человека происходит синтез всех заменимых ВЖК - всех предельных и непредельных ВЖК, имеющих одну двойную связь.

Холестерин является одноатомным циклическим спиртом, который в тканях легко образует ХОЛЕСТЕРИДЫ (в положении 3). В организм человека поступает в составе пищи и синтезируется г.о. в печени, тонком отделе кишечника и коже.
Биологическая роль холестерина:
1.Структурная. Свободный холестерин является, обязательным структурным компонентом мембран клеток.
2.Метаболическая. Холестерин является предшественником биологически активных веществ: витамина D3
СТЕРОИДНЫХ гормонов (АНДРОГЕНОВ, ЭСТРОГЕНОВ, КОРТИКОИДОВ) При окислении холестерина в печени при участии ЦИТОХРОМА Р-450 образуются желчные кислоты, которые принимают участие в переваривании жиров пищи. Наиболее богаты холестерином плазматические мембраны ГЕПАТОЦИТОВ, где на его долю приходится 30% всех мембранных липидов. Содержание холестерина в миелине составляет 20%. В свободном виде холестерин транспортируется по организму с помощью транспортных ЛИПОПРОТЕИНОВ крови.
Источники холестерина:
1. Пища. За сутки в организм взрослого человека поступает 0,3гр. холестерина.
2. У человека в среднем с массой 65-70кг за сутки синтезируется 3.5 -4,2гр. холестерина. Печень занимает главное место в синтезе холестерина (85%), в меньшей степени холестерин синтезируется в кишечнике (10%) и коже (5%). На экспорт холестерин синтезируется только в печени и кишечнике.
Процесс биосинтеза сложен и многоступенчат. Он включает в себя 35 реакций. Схематично его можно представить следующим образом:

Образовавшийся в результате распада мембранных ЛИПИДОВ, а также излишки холестерина с помощью ЛПВП доставляется для окисления в печень, и в составе желчных кислот удаляется из организма с каловыми массами в виде КОПРОСТЕРИНОВ.
ПАТОЛОГИЯ ЛИПИДНОГО ОБМЕНА.
1.На этапе поступления жиров с пищей:
A. Обильная жирная пища на фоне ГИПОДИНАМИИ приводит к развитию АЛИМЕНТАРНОГО ОЖИРЕНИЯ.
B. Недостаточное поступление жиров или их отсутствие приводит к ГИПО- и АВИТАМИНОЗАМ A, D. Е, К. Могут развиваться ДЕРМАТИТЫ, СКЛЕРОЗ сосудов, когда с пищей не поступают ЭССЕНЦИАЛЬНЫЕ ВЖК. Также нарушается процесс синтеза ПРОСТАГЛАНДИНОВ, ПРОСТАЦИКЛИНОВ, ТРОМБОКСАНОВ и ЛЕЙКОТРИЕНОВ местных гормонов.
C. Недостаточное поступление с пищей ЛИПОТРОПНЫХ веществ приводит к развитию жировой инфильтрации тканей. К ЛИПОТРОПНЫМ веществам относятся:
ХОЛИН, ИНОЗИТ, СЕРИИ вещества, принимающие участие в синтезе
ФОСФОЛИПИДОВ. Витамин В6 (ПЕРИДОКСАЛЬФОСФАТ), входящий в состав ДК СЕРИНА. МЕТИОНИН поставщик МЕТИЛЬНЫХ групп при биосинтезе ХОЛИНА из ЭТАНОЛАМИНА.
Витамин BI2 и ФОЛИЕВАЯ К-ТА, которые являются КОФЕРМЕНТАМИ МЕТИЛТРАНСФЕРАЗ.
2.На этапе пищеварения.
A. При поражении печени и кишечника нарушается образование и транспорт ЛП крови.
B. При поражении печени и желчевыводяицих путей нарушается образование и экскреция желчных кислот, участвующих в переваривании жиров пищи. В случае нарушения оттока желчи происходит насыщение её холестерином, что ведёт в этих условиях к застою и образованию холестериновых камней, центрами образования которых служат слущивающиеся клетки эпителия. Развивается ЖЕЛЧЕКАМЕННАЯ БОЛЕЗНЬ. В крови отмечается ГИПЕРХОЛЕСТЕРИНЕМИЯ.
C. Если поражается слизистая оболочка кишечника и нарушается выработка и поступление ферментов ПЖЖ, содержание жира в кале увеличивается. Если содержание жира будет превышать 50%, развивается СТЕАТОРЕЯ. Кал становится бесцветным.
D. Наиболее часто в последнее время среди населения встречается поражение бета -клеток ПЖЖ, что ведйт к развитию сахарного диабета, который сопровождается интенсивным окислением в клетках белков и жиров. В крови у таких больных отмечается ГИПЕРКЕТОНЕМИЯ, ГИПЕРХОЛЕСТЕРИНЕМИЯ. Кетоновые тела и холестерин синтезируются из АЦЕТИЛ-КОА.
3.На этапе обмена холестерина наиболее ча
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 1050; Нарушение авторских прав?; Мы поможем в написании вашей работы!