
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Окислительно-восстановительные электроды
Амальгамные электроды
Газовые электроды
Газовый электрод состоит из инертного металла (обычно платины), контактирующего одновременно с газом и раствором, содержащим ионы этого газообразного вещества.
Примером газовых электродов могут служить водородный, кислородный и хлорный электроды:
Н+ ½ H2, Pt.
Амальгамный электрод состоит из амальгамы данного металла (раствор металла в ртути) в контакте с раствором, содержащим ионы этого металла:
МеZ+ ½ Me, Hg.
Окислительно-восстановительный электрод состоит из инертного металла, погруженного в раствор, содержащий окисленную и восстановленную форму вещества:
Fe2+, Fe3+ ½ Pt.
ВОДОРОДНЫЙ ЭЛЕКТРОД
Этот электрод состоит обычно из платинированной платиновой пластинки опущенной в раствор, содержащий ионы водорода, и омываемый током газообразного водорода. (Платинированием называется покрытие поверхности слоем платиновой черни, т.е. слоем высокодисперсной платины, получаемой обычно электролитическим путем непосредственно на самой пластинке).
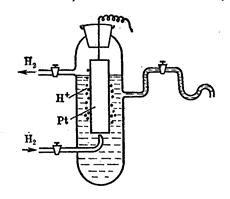
В водородном электроде происходит реакция
1/2Н2 = Н+ + е,
вполне аналогичная реакциям, протекающим на поверхности металлических электродов, обратимых относительно катиона. Платина здесь играет роль только инертного проводника и может быть заменена палладием, иридием, золотом и некоторыми другими металлами.
Электродный потенциал такого электрода зависит от концентрации ионов водорода в растворе, от давления водорода в газовой фазе и от температуры.
jН+ = j0Н+ + (lnaH+ - lnPH2),
для РН2 = 1 атм;
jН+ = lnaH+;
jH+ = 1,984×10-4 T lgaH+;
jH+ = - 1,984× 10-4 T (pH).
Водородный электрод весьма чувствителен к условиям работы. Для получения вполне правильных и устойчивых результатов существенны, в частности, высокая степень чистоты водорода и состояние поверхности платины. При правильной работе, водородный электрод дает очень точные результаты, воспроизводимые до 0,00001 в. Но чувствительность его к условиям процесса сильно усложняет работу с ним. Поэтому обычно пользуются другими электродами, для которых потенциал по отношению к такому электроду известен и которые вместе с тем не так капризны в работе
|
|
Дата добавления: 2014-01-05; Просмотров: 785; Нарушение авторских прав?; Мы поможем в написании вашей работы!