
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Водородный показатель
ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ.
Лекция 4
Вода, очищенная от посторонних примесей обладает электрической проводимостью, заметно возрастающей с повышением температуры (при 273К удельная электрическая проводимость воды составляет ρ =1,5 · 10 -8 Ом-1 · см-1, при 289 К ρ= 6,2 · 10 -8 Ом-1 · см-1).
Наличие электрической проводимости объясняется тем, что молекулы воды частично распадаются на ионы, т. е. Н2О является слабым электролитом.
Процесс диссоциации воды происходит по уравнению:
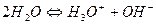
Свободных ионов Н+ в воде не существует, в связи с их гидратацией образуется ион гидроксония 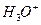 .
.
Для простоты запишем уравнение диссоциации:
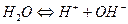

Константа диссоциации 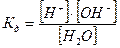 =
= 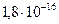
Молекулярная масса воды 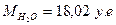 ,
,
Число молей воды в 1 литре раствора 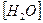 =
= 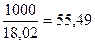
Ионное произведение воды Кw = const при постоянной температуре t=const
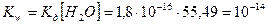
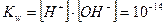
В чистой воде в нейтральном растворе концентрация ионов водорода равна концентрации ионов гидроксила: 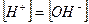 , тогда
, тогда
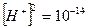 ;
; 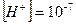 ;
; 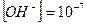
В кислой среде [H+]>10-7
В щелочной среде [H+]<10-7
Для удобства пользуются значением отрицательного логарифма концентрации ионов водорода:
pH = - lg [H+]=7
pOH = - lg [OH-]=7
Процесс диссоциации воды – эндотермический, происходит с поглощением тепла по реакции:
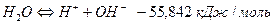
При повышении температуры Кд увеличивается, и степень диссоциации увеличивается; при t=500С 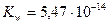
рН = 6,63, рН изменилась, а среда осталась нейтральной
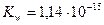 при 00С, рН = 7,97.
при 00С, рН = 7,97.
В соответствии с теорией электролитической диссоциации, ионы Н+
являются носителями кислотных свойств, а ионы ОН- носителями основных свойств раствора.
Водородный показатель определяет характер реакции раствора. Значение рН = 7 соответствует нейтральному раствору только при 2950К
Водородный показатель имеет важное значение для понимания большинства процессов, протекающих в жидкой фазе, так как ионы Н+ и ОН- непосредственно участвуют во многих из этих процессов. Кроме того, эти ионы являются гомогенными катализаторами многих реакций.
|
|
Дата добавления: 2014-01-05; Просмотров: 342; Нарушение авторских прав?; Мы поможем в написании вашей работы!