
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Строение коллоидной частицы
|
|
|
|
Рассмотрим процесс образования золя и строение его дисперсных частиц на примере гидрозоля хлорида серебра.
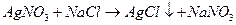 , избыток AgNO3
, избыток AgNO3
Этот гидрозоль образуется при медленном приливании водного раствора NaCl к водному раствору AgNO3, взятому в избытке.
При постепенном введении NaCl в системе образуются кристаллические агрегаты (AgCl)n из ионов Ag+ и Cl-, расположенных в том же порядке, что и в кристаллической решетке AgCl.
Агрегаты (AgCl)n адсорбируют на своей поверхности те ионы, которые составляют кристаллическую решетку и находятся в растворе в избытке.
Этим условиям отвечают ионы Ag+.
В результате адсорбции ионов Ag+ кристаллические агрегаты (AgCl)n приобретают положительный заряд.
Ионы, адсорбирующиеся на поверхности кристаллического агрегата, называются потенциал-определяющими. Наличие одноименных зарядов на агрегатах препятствует их объединению и росту кристаллов AgCl, т.о. агрегаты AgCl с адсорбированными на их поверхности ионами Ag+ приобретают состояние агрегативной устойчивости.
Кристаллический агрегат с потенциалопределяющими ионами Ag+ составляет ядро. К заряженному ядру притягиваются ионы противоположного заряда – противоионы, в данном случае 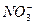 .
.
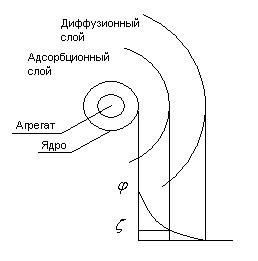
Противоионы, непосредственно примыкающие к ядру образуют адсорбционный слой противоионов.
За этим слоем следует диффузионный слой тех же противоионов. Концентрация противоионов диффузного слоя постепенно снижается по мере удаления от ядра. Между противоионами адсорбционного и диффузного слоев устанавливается подвижное равновесие.
Противоионы подвижного слоя ориентируют полярные молекулы растворителя, создавая дополнительную сольватную оболочку.
Ядро вместе с противоионами адсорбционного слоя составляет коллоидную частицу или гранулу.
|
|
|
Коллоидная частица совместно с противоионами диффузного слоя называется мицеллой.
Коллоидная частица всегда заряжена, знак заряда соответствует знаку заряда агрегата, мицелла – электронейтральна.
При снижении или полном уничтожении заряда коллоидных частиц, диффузионный слой разрушается, что приводит к снижению устойчивости коллоидной системы.
Процесс разрушения укрупнения коллоидных частиц под действием внешних сил приводит к образованию осадка, называется коагуляцией.
Осаждение частиц дисперсной фазы под действием силы тяжести, называется седиментацией.
Двойной электрический слой состоит из потенциалопределяющих ионов фиксированных на поверхности твердой фазы и противоположно заряженных ионов (противоионов) находящихся в жидкой фазе. В результате чего между твердыми и жидкими фазами возникает разность потенциалов – поверхностный потенциал 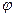 .
.
При относительном перемещении фаз происходит разрыв двойного электрического слоя обычно по диффузионному слою и дисперсная фаза, и дисперсная среда становятся противоположно заряженными.
В результате на границе разрыва возникает разность потенциалов, называется электрокинетическим потенциалом 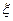 - потенциал;
- потенциал; 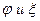 - важные характеристики устойчивости системы.
- важные характеристики устойчивости системы.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 546; Нарушение авторских прав?; Мы поможем в написании вашей работы!