
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Правила электрофильного замещения в ароматическом ядре
|
|
|
|
В бензоле все шесть атомов углерода равноценны, поэтому вступление первого заместителя возможно в любое положение, но, если в молекуле бензола один из атомов Н уже замещен, то вторичное замещение будет происходить в определенное положение по отношению к первому заместителю.
По характеру влияния на ароматическое ядро имеющиеся в нем заместители можно разделить на 2 вида:
Заместители 1 рода: -OH, OR, RCOO-, SH, SR, NHR, NR2, NHCOR, -N=N-, -NH2, Alk-, Hal-. Находясь в ядре, эти заместители ориентируют электрофильный реагент Х+ в положения орто- или пара-.
Заместители 2 рода: NO2-, SO3H, -COOH, -C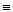 N, -NH3+, NR3+, COR, COOR, CCl3, CHal3, -C=O
N, -NH3+, NR3+, COR, COOR, CCl3, CHal3, -C=O
H
Находясь в ядре, эти заместители ориентируют вступающий электрофильный реагент Х+ в положение мета-.
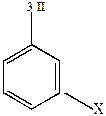
Заместители 1 рода являются группировками электроно-донорными (за исключением галогенов), т.к. все они имеют у атома, связанного с ядром, избыток электронной плотности, который могут отдать ядру. Это приводит к повышению электронной плотности в орто- и пара-положениях по отношению к заместителю.
Влияние заместителей на ядро передается как индукционным путем (прямые стрелки), так и за счет эффекта сопряжения (изогнутые стрелки). Например,
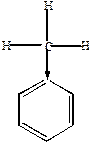
| При наличии алкила наблюдается положительное индукционное влияние (+I) и 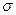 - -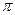 сопряжение (+М) совпадают по направлению. сопряжение (+М) совпадают по направлению.
|

| При наличии группы –ОН наблюдается отрицательное индукционное влияние (-I) и p-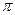 сопряжение (+М), которые не совпадают по направлению, но +M>-I. сопряжение (+М), которые не совпадают по направлению, но +M>-I.
|
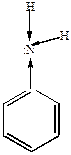
| То же самое наблюдается при наличии группы –NH2, где +М>-I |
Во всех этих случаях повышена электронная плотность в орто- и пара-положениях, поэтому реакции электрофильного замещения идут в этих положениях и протекают легче, чем в замещенном бензоле.
|
|
|
При наличии в качестве заместителя галогена, в статистическом состоянии молекулы наблюдается более сильное индукционное влияние –I>+M. В результате ароматическое ядро обедняется электронами в целом, и реакционноспособность кольца хлорбензола меньше, чем бензола.
Однако, с учетом динамических факторов, преобладающее влияние оказывает все же эффект p-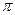 -сопряжения, и реакция замещения идет преимущественно в орто- или пара-положении, но труднее, чем при наличии других заместителей 1 рода.
-сопряжения, и реакция замещения идет преимущественно в орто- или пара-положении, но труднее, чем при наличии других заместителей 1 рода.
Динамические факторы связаны, в основном, с устойчивостью 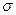 -комплексов, образующихся в процессе реакции.
-комплексов, образующихся в процессе реакции.

|

| 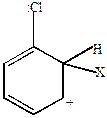
|
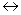
| 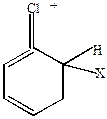
| |
|
 + X+ + X+
|  2 2
| 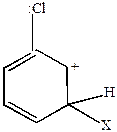
| ||
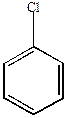
| Хлорбензол |

| 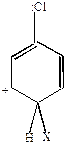
|
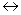
| 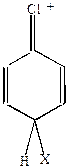
|
В случаях (1) и (3) наблюдается включение в цепь сопряжения положительного заряда, что приводит к его делокализации и повышению устойчивости 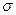 -комплекса. В случае (2) делокализация положительного заряда с участием р-электронов хлора невозможна. Возможно образование граничных структур
-комплекса. В случае (2) делокализация положительного заряда с участием р-электронов хлора невозможна. Возможно образование граничных структур 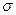 -комплексов, когда неподеленная пара электронов хлора переходит к положительно заряженному атому углерода. Поэтому реакции идут в основном в положение орто- или пара-.
-комплексов, когда неподеленная пара электронов хлора переходит к положительно заряженному атому углерода. Поэтому реакции идут в основном в положение орто- или пара-.
Заместители 2 рода обладают электронно-акцепторным характером, т.е. имеют на атоме, связанном с ядром, положительный заряд и оттягивают на себя 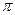 -электронное облако кольца. Например, бензойная кислота
-электронное облако кольца. Например, бензойная кислота
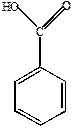
Направление индукционного влияния (-I) в этом случае совпадает с направлением эффекта сопряжения (-М). Поэтому ядро обеднено электронами, и особенно сильно в положении орто- и пара-. Менее обеднены электронами атомы углерода в мета-положении, к ним и присоединяется электрофильный реагент. Так как заместители 2 рода понижают электронную плотность ядра, то электрофильное замещение у этих соединений идет труднее, чем у бензола.
Рассмотрим конкретные примеры реакций электрофильного замещения в ароматических углеводородах.
|
|
|
1.Галоидирование
а) замещения в ядре.
Реакции хлорирования и бромирования в ароматическом ядре обязательно требуют присутствия электрофильных катализаторов (FeCl3, AlCl3) и могут идти даже без нагревания. Катализатор обеспечивает электрофильный механизм реакции.
FeCl3 + Cl2 : Cl 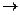 [FeCl4]-Cl+
[FeCl4]-Cl+ 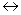 FeCl4- + Cl+
FeCl4- + Cl+
Галоидирование гомологов бензола может происходить в 2-х направлениях:
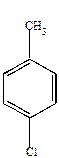
1) галоидирование ядра.
Механизм реакций электрофильный.

|
 + Cl+
(Cl2 + FeCl3)
+ Cl+
(Cl2 + FeCl3)
| 
| +H+ | |

| 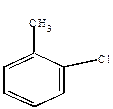
|
2) замещение в боковой цепи.
Механизм реакции свободно-радикальный.
h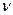
Cl2 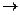 2Cl.
2Cl.
| Cl. + | 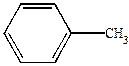
|
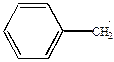
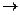 HCl + HCl +
| 
|
+Cl2
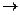
| 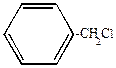
| +Cl. |
Необходимо отметить, что при наличии в боковой цепи нескольких атомов углерода реакция галоидирования идет преимущественно в 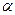 -положении к ядру, что обусловливается большой устойчивостью образующегося при этой реакции радикала.
-положении к ядру, что обусловливается большой устойчивостью образующегося при этой реакции радикала.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 879; Нарушение авторских прав?; Мы поможем в написании вашей работы!