
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ВОДНЕВИЙ ЗВ’ЯЗОК
|
|
|
|
Крім вандерваальсових сил міжмолекулярної взаємодії між деякими молекулами або певними групами у складних молекулах може виникати водневий зв’язок.
Водневий зв’язок виникає як особливий тип взаємодії між молекулами або функціональними групами у складних молекулах, до складу яких входять атоми водню, ковалентно сполучені з найбільш електронегативними атомами — найчастіше киснем, азотом і фтором. Він має складну природу внаслідок значного внеску електростатичної і певною мірою донорно-акцепторної взаємодії. Подібно до ковалентного зв’язку водневий зв’язок характеризується насиченістю і просторовою напрямленістю.
З урахуванням цього водневий зв’язок утворюється немовби за рахунок побічної валентності атома водню.
Механізм його виникнення можна пояснити так. У сполуках типу Х –Н узагальнена електронна пара зміщена до найбільш електронегативного атома. Позитивно поляризований атом водню можна уявити як частково оголене ядро, що має надзвичайно малий розмір і внаслідок цього — високу напруженість позитивного електричного поля. Це зумовлює його енергійний вплив на електронну оболонку атома Y сусідньої молекули (групи), яка має негативний заряд. Схематично утворення водневого зв’язку можна подати так:
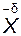 –
– 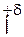 +
+ 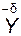 –
– 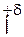 ® X – H ××× Y – H
® X – H ××× Y – H
Водневий зв’язок позначають трьома крапками.
Атом водню зазвичай міцніше зв’язаний з тим із двох атомів, з яким утворює ковалентний зв’язок.
Енергія водневого зв’язку становить 8–40 кДж/моль. За міцністю він перевищує вандерваальсову взаємодію, але здебільшого слабкіший від ковалентного зв’язку.
Водневий зв’язок дуже поширений і відіграє важливу роль у структурі багатьох неорганічних та органічних сполук.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 530; Нарушение авторских прав?; Мы поможем в написании вашей работы!