
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Сущность процесса производства стали
|
|
|
|
Содержание углерода и примесей в стали значительно ниже, чем в чугуне (табл. 5).
Состав передельного чугуна и низкоуглеродистой стали, % Таблица 5
| Материал | С | Si | Мп | Р | S | ||
| Передельный чугун | 4. | …..4,4 | 0,56. | …. 1,26 | До 1,75 | 0,10... 0,3 | 0,03...0,07 |
| Сталь низкоуглеродистая | 0,12 | ......0,25 | 0,12. | ……0,3 | 0,3... 0,9 | 0,05 | 0,050 |
Сущностью любого металлургического передела чугуна в сталь является снижение содержания углерода и примесей путем их избирательного окисления и перевода в шлак и газы в процессе плавки.
Основными материалами для производства стали являются передельный чугун и стальной лом (скрап).
В процессе плавки стали происходит взаимодействие между металлической [ ], шлаковой () и газовой фазами и футеровкой плавильного агрегата (основной или кислой), различными по агрегатному состоянию и химическому составу. В результате этого взаимодействия осуществляется переход химических элементов из одной фазы в другую. Обменные процессы сопровождаются химическими превращениями, главным образом на границе металлической фазы со шлаком. Металлическая фаза состоит из расплава химических элементов, шлаковая - из расплава оксидов и их соединений. Поэтому переход элемента из одной фазы в другую возможен только при протекании химической реакции образования или восстановления оксида. Так как примеси по своим физико-химическим свойствам различны, то для их удаления в плавильном агрегате создают определенные условия, используя основные законы физической химии.
В соответствии с законом действующих масс скорость химических реакций пропорциональна концентрации реагирующих веществ. Поскольку в наибольшем количестве в чугуне содержится железо, то оно окисляется в первую очередь при взаимодействии чугуна с кислородом в сталеплавильной печи:
|
|
|
Fe + 1/2О2 = FeO + Q кДж. (1)
Одновременно с железом окисляются Si, P, С, Мп и др.
Образующийся оксид железа при высоких температурах отдает свой кислород более активным элементам - примесям в чугуне, окисляя их:
2FeO + Si = SiO2 + 2Fe + Q, кДж; (2)
5FeO + 2P = P2O5 + 5Fe + Q2 кДж; (3)
FeO + Mn = MnO + Fe + Q3 кДж; (4)
FeO + С = CO + Fe - Q4 кДж. (5)
Чем больше оксида железа содержится в жидком металле, тем активнее окисляются примеси. Для ускорения окисления примесей в сталеплавильную ванну добавляют железную руду, окалину, содержащие много оксидов железа. Таким образом, основное количество примесей окисляется за счет кислорода оксида железа.
После расплавления шихты в сталеплавильной печи образуются две несмешивающиеся среды: жидкий металл и шлак.
Нерастворимые соединения в зависимости от плотности будут переходить либо в шлак, либо в металл. Изменяя состав шлака, можно менять соотношение между количеством примесей в металле и шлаке так, что нежелательные примеси будут удаляться из металла в шлак. Убирая шлак с поверхности металла и наводя новый путем подачи флюса требуемого состава, можно удалять вредные примеси (серу, фосфор) из металла. Поэтому регулирование состава шлака с помощью флюсов является одним из основных путей управления металлургическими процессами.
Используя изложенные законы, процессы выплавки стали осуществляют в несколько этапов.
Первый этап - расплавление шихты и нагрев ванны жидкого металла. На этом этапе температура металла невысока; интенсивно происходят окисление железа, образование оксида железа и окисление им примесей Si, P, Мп по реакциям (1) - (4). Фосфор удаляется благодаря присутствию шлаков с большим содержанием СаО и FeO, интенсивному перемещению металла и шлака при сравнительно невысоких температурах. Принято компонент, находящийся в растворе металла, обозначать в прямых скобках [Р], а находящийся в растворе шлака - в круглых скобках (СаО).
|
|
|
2[Р] + 5(FeO) + 4(CaO) ß>(4CaOP2O5)+5[Fe]. (6)
Второй этап - "кипение" металлической ванны - начинается по мере ее прогрева до более высоких, чем на первом этапе, температур.
Образующийся в металле оксид железа реагирует с углеродом по реакции (5), а пузырьки оксида углерода СО выделяются из жидкого металла, вызывая "кипение" ванны (рис.32). При "кипении" уменьшается содержание углерода в металле до требуемого, выравнивается температура по объему ванны, частично удаляются неметаллические включения, прилипающие к всплывающим пузырькам СО, а также газы, проникающие в пузырьки СО. Все это способствует повышению качества металла. Поэтому этап "кипения" ванны является основным в процессе выплавки стали.
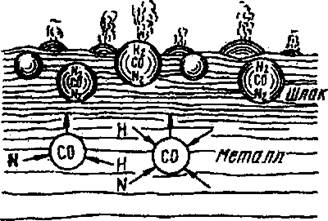
Рис. 32. Схема удаления газов из жидкого металла в процессе кипения
В этот же период создаются условия для удаления серы из металла. Сера в стали находится в виде сульфида [FeS], который растворяется также в основном шлаке (FeS). Чем выше температура, тем большее количество FeS растворяется в шлаке, т.е. больше серы переходит из металла в шлак. Сульфид железа, растворенный в шлаке, взаимодействует с оксидом кальция, также растворенным в шлаке: (FeS) + (СаО) = (CaS) + (FeO). (7)
Эта же реакция протекает на границе металл - шлак между сульфидом железа в стали [FeS] и (СаО) в шлаке: [FeS] + (СаО) = (CaS) + (FeO). (8)
Образующееся соединение (CaS) растворимо в шлаке, но не растворяется в железе, поэтому сера удаляется в шлак.
Третий этап (завершающий) - раскисление стали - заключается в восстановлении оксида железа, растворенного в жидком металле. При плавке повышение содержания кислорода в металле необходимо для окисления примесей, но в готовой стали кислород - вредная примесь, так как понижает механические свойства стали, особенно при высоких температурах.
Легирование стали осуществляют введением ферросплавов или чистых металлов в необходимом количестве в расплав. Легирующие элементы (Ni, Co, Мо, Си), сродство к кислороду у которых меньше, чем у железа, при плавке и разливке практически не окисляются, и поэтому их вводят в печь в любое время плавки (обычно вместе с остальной шихтой). Легирующие элементы, у которых сродство к кислороду больше, чем у железа (Si, Mn, Al, Cr, V, Ti и др.), вводят в металл после раскисления или одновременно с ним в конце плавки, а иногда непосредственно в ковш.
|
|
|
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 897; Нарушение авторских прав?; Мы поможем в написании вашей работы!