
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Електролітична дисоціація. Електроліз
|
|
|
|
План
Електричний струм у розчинах і розплавах електролітів. Закони електролізу. Застосування електролізу.
Запитання для самоперевірки
1.Чому електричне поле заряджених частинок не здатне підтримувати постійний електричний струм в колі?
2. Що називають сторонніми силами?
3. Що називають ЕРС джерела струму? Який фізичний зміст ЕРС? У яких одиницях її виражають?
4. Що розуміють під внутрішньою і зовнішньою частинами кола?
5. Що показує вольтметр, приєднаний до полюсів джерела струму, у разі розімкненої зовнішньої ділянки кола? Замкненої зовнішньої ділянки кола?
6. Виведіть формулу закону Ома для повного кола. Як формулюється цей закон?
7. Напишіть формулу для визначення роботи постійного струму.
8. Доведіть, що робота струму виміряється в джоулях.
9. Як записується закон Джоуля-Ленца?
10.Як залежить кількість теплоти, що виділяється під час проходження струму у провідниках, від опору цих провідників у разі їх послідовного і паралельного з'єднання?
11. Запишіть формулу потужності постійного струму.
12. Доведіть, що потужність струму виражається у ватах.
13. Яким приладом вимірюють потужність постійного струму?
14. Нарисуйте схеми ввімкнення в коло постійного струму амперметра і вольтметра.
15. Що вимірюють у кіловат-годинах?
1.Електролітична дисоціація. Електроліз
2.Закони електролізу. Застосування електролізу
Рідини, як і тверді тіла, можуть бути діелектриками, провідниками і напівпровідниками. Діелектриком є також дистильована вода. До провідників належать розплави і розчини електролітів: кислот, лугів і солей. Рідкими напівпровідниками є розплавлений селен, розплави сульфідів та ін.
Під час розчинення електролітів під впливом електричного поля полярних молекул води відбувається розпад молекул електролітів на іони. Цей процес називають електролітичною дисоціацією, в результаті якої нейтральні молекули розпадаються на позитивні та негативні іони. В електроліті з'являються вільні носії зарядів і він починає проводити струм. Оскільки заряд у водних розчинах чи розплавах електролітів переноситься іонами, то таку провідність називають іонною. За іонної провідності проходження струму пов'язано із перенесенням речовини. На електродах відбувається виділення речовин, які входять до складу електроліту. На аноді негативно заряджені частинки віддають свої зайві електрони (окиснювальна реакція), а на катоді позитивні іони отримують електрони (реакція відновлення). Процес виділення на електроді речовини, пов'язаний із окиснювально-відновлювальними реакціями, називають електролізом.
|
|
|
Розглянемо явище електролізу на прикладі мідного купоросу. В результаті електролітичної дисоціації CuSO4 = Cu2 + + SO4 2 +. Позитивно заряджені іони міді під дією електричного струму будуть переміщуватися до катода, де отримають електрони і виділяться на ньому у вигляді нейтральних атомів міді (рис. 4.3.4). Негативно заряджені іони під дією електричного поля перемістяться до анода, де віддадуть вільні електрони і також виділяться на ньому.

Нехай за час t через електроліт буде перенесено заряд. Кількість іонів, які досягли електрода, дорівнюватиме: 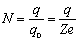 , де q 0 = Ze - заряд іона; Z - валентність іона; e - елементарний заряд.
, де q 0 = Ze - заряд іона; Z - валентність іона; e - елементарний заряд.
Кількість іонів N дорівнює кількості атомів речовини, що виділиться на електроді, а маса виділеної речовини
 , (4.3.3) де m 0 - маса одного атома,
, (4.3.3) де m 0 - маса одного атома, 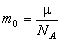 ; m - молярна маса речовини.
; m - молярна маса речовини.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1527; Нарушение авторских прав?; Мы поможем в написании вашей работы!