
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электропроводность полупроводников
|
|
|
|
Цоколёвочные мастики
Применяются для крепления цоколя к стеклу (неразъёмные соединения). По переходу из одной фазы (пастообразные, жидкие) в твёрдую мастики делятся на: 1) плавящиеся; 2) схватывающиеся (присоединение кристаллизационной Н2О); 3) реакционные (постепенное протекание химических реакций между компонентами); 4) конституционные (отверждение в результате водоотщепления).
Соединение осуществляется: 1) путём адгезии (прилипания); 2) охватывание скреплённых деталей (фасонное крепление). Неприятное свойство некоторых мастик – водопоглощение и набухание (отвал цоколя или нарушение изоляции, если токовводы касаются мастики. Поверхности перед цоколеванием необходимо очищать от жирных и масляных пятен, ухудшающих адгезию. Для крепления пластмассовых цоколей (деталей) используются мастики с малой температурой отверждения (< 150оС).
Плавящиеся мастики: 1) пицеин; 2) известково-саратная; 2) новолаковая; 4) шеллачно-фарфоровая.
Схватывающиеся мастики: 5) ГИПС; 6) мраморный цемент; 7) портландский цемент; 8) силикат калия – окись магния; 9) силикат калия - отмученный мел.
Реакционные мастики: 10) свинцовый глёт –глицерин; 11) розовая мастика; 12) каолин и бура.
Конституционные мастики: 13) шеллачная; 14) бакелитовая (резолевая); 15), 16) силиконосмоляные.
Составы, режимы (временные и температурные) всех мастик можно найти в [1, т. 3, табл. 19-1], там же (табл. 19-4) – электропроводяшая мастика.
Б. ХИМИЯ МАТЕРИАЛОВ ДЛЯ СВЕТОДИОДОВ
И ПОЛУПРОВОДНИКОВЫХ ПРИБОРОВ
Рассмотрим возможные типы проводимости на примере чистого и легированного кремния.
Электроводность п/п i - типа проводимости


 а) а) чистый п/п (Si) (низкие температуры), 1 чёрточка соответствует 1 электрону
а) а) чистый п/п (Si) (низкие температуры), 1 чёрточка соответствует 1 электрону
|
|
|
 б) б) чистый п/п (Si) при температуре 200оС:
б) б) чистый п/п (Si) при температуре 200оС: 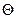 - 1 электрон покидает своё место под воздействием теплового излучения;
- 1 электрон покидает своё место под воздействием теплового излучения;  - на месте электрона образуется дырка, квазичастица, аналогичная электрону, но имеющая положи- тельный заряд
- на месте электрона образуется дырка, квазичастица, аналогичная электрону, но имеющая положи- тельный заряд
 в) в) чистый п/п (Si) при приложении электрического поля, электрон перемещается против поля, дырка - в направлении поля. Электропроводность чистого п/п определяется формулой:
в) в) чистый п/п (Si) при приложении электрического поля, электрон перемещается против поля, дырка - в направлении поля. Электропроводность чистого п/п определяется формулой:
σi = enμn + epμp,
где е - заряд электрона, n - концентрация электронов, p - концентрация дырок, μn и μp - подвижности электронов и дырок (скорости перемещения частиц, имеющих единичный электрический заряд, в электрическом поле единичной напряженности).
Электропроводность п/п n-типа проводимости
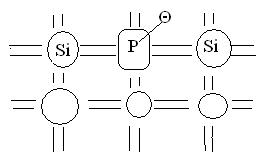 Если в чистый п/п ввести атомы примеси из группы на единицу больше, чем группа самого п/п (для Si это элемент 5 группы, Р), то 4 валентных электрона Р образуют прочные электронные пары с Si, а избыточный 5-й электрон
Если в чистый п/п ввести атомы примеси из группы на единицу больше, чем группа самого п/п (для Si это элемент 5 группы, Р), то 4 валентных электрона Р образуют прочные электронные пары с Si, а избыточный 5-й электрон
имеет слабую связь с ядром Р. Даже при комнатной температуре этот электрон становится свободным. При приложении электрического поля (Е) происходит ток (перемещение электронов, дырок при этом не образуется.
Проводимость такого п/п: σn = enμn - это проводник с электронным типом проводимости (обозначения см. выше).
Электропроводность п/п р-типа проводимости
 Если в чистый п/п ввести атомы примеси из группы на единицу меньше, чем группа самого п/п (для Si это элемент 3 группы бор, В), то 3 валентных электрона атома В образуют прочные связи с соседними атомами Si, а 4-ая пара остаётся не заполненной, т.е. образуется дырка, при этом свободных электронов нет. При при ложении к такому п/п электрического поля (Е) происходит перемещение дырок, а его электропроводсть называется дырочной (р-типа) и определяется формулой: σр = eрμр (обозначения см. выше).
Если в чистый п/п ввести атомы примеси из группы на единицу меньше, чем группа самого п/п (для Si это элемент 3 группы бор, В), то 3 валентных электрона атома В образуют прочные связи с соседними атомами Si, а 4-ая пара остаётся не заполненной, т.е. образуется дырка, при этом свободных электронов нет. При при ложении к такому п/п электрического поля (Е) происходит перемещение дырок, а его электропроводсть называется дырочной (р-типа) и определяется формулой: σр = eрμр (обозначения см. выше).
Зонные диаграммы для различных пипов п/п
|
|
|
Собственный п/п Примесные п/п
i-тип n-тип р-тип


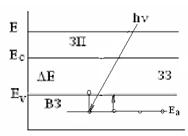
ЗП – зона проводимости, ЗЗ – запрещённая зона, ВЗ – валентная зона
ΔЕ – ширина ЗЗ, Ес - дно зоны проводимости, Еv - потолок валент- ной зоны, Ед - донорный уровень, Ед «∆Е, Еа - акцепторный уровень, Еа «∆Е.
16. Полупроводники (общие сведения и классификация) [26].
По значению удельного электрического сопротивления (ρ) п/п занимают промежуточное положение между диэлектриками и проводниками (ρ = 10-6÷109 Ом см). Отличия от проводников: 1) при увеличении температуры ρп/п уменьшается (отрицательный температурный коэффициент удельного электрического сопротивления); 2) ρп/п резко изменяется при введении в п/п ничтожного количества примесей; 3) п/п чувствительны к различного типа внешним воздействиям – свету, ядерному излучению, электрическому и магнитному полям, давлению и др.
Свойствами п/п обладают целый ряд материалов – природных и синтетических, органических и неорганических, простых и сложных по химическому составу.
Простые п/п: Ge, Si, Se, Te, B, C, P, S, Sb, As, серое Sn, J.
Сложные п/п: 1) бинарные (двойные) соединения: AIBVII (CuCl, AgBr и др.); AIBVI (Cu2O, CuS и др.); AIBV (KSb, K3Sb и др.); AIIBVII (ZnCl2, CdCl2 и др.); AIIBVI (ZnO, ZnS, CdS и др.); AIIBV (ZnSb, Mg3Sb2 и др.); AIIBIV (Mg2Sn, CaSi и др.); AIIIBVI (GaS, In2Fe3 и др.); AIIIBV (GaP, GaAs, InSb и др.); AIVBVI (GeO2, PbS и др.); AIVBIV(SiC); AVBVI (Sb2Te3, Bi2S3 и др.); AVIBVI (MoO3, WO3 и др.); AVIIBVI (Fe2O3, NiO); 2) тройные соединения: AIBIIIB2VI (CuAlS2, CuInS2 и др.); AIBVB2VI (CuSbS2, CuAsS2 и др.); AIBVIIIB2VI (CuFeS2 и др.); AII BIVB2V (ZnSiAs2, ZnGeAs2); AIVBVB2VI (PbSiSe); 3) твёрдые растворы: GeSi,GaAs1-xPx; InxAl1-xSb и др.
К органическим п/п относятся фталоцианин, антрацин, нафталин, коронел и др.
Германий, Ge: IV группа периодической системы элементов, №32, ат.вес – 72,59, Тпл = 937оС, ΔЕ = 0,65 эВ (300 К), ρ = 0,47Ом·м (20оС), ТКЛР = 6 10-3 град-1 (0÷100оС), уд. плотн. = 5,3 г/см3.
Получают из германийсодержащей руды путём химической переработки сырья с помощью концентрированной НCl в виде GeCl4 (тетрахлорида Ge) – летучая жидкость, которая подвергается глубокой очистке методами экстракции и ректификации. После гидролизации водой получают диоксид Ge (GeO2) – порошок белого цвета. Восстанавливают при 650оС в токе очищенного Н2 – получают серый порошок Ge. Затем травят в смеси кислот и сплавляют в слитки, которые используются как сырьё для получения особо чистого Ge методом зонной плавки или же непосредственного получения монокристаллов методом вытягивания из расплава.
|
|
|
Кристаллический Ge химически устойчив в воздухе при комнатной температуре, размельчённый в порошок при 700оС в воздухе образует GeO2. Слабо растворим в Н2О и практически не растворим в HCl и разбавленной H2SO4. Активные растворители: смесь HNO3 и HF, раствор Н2О2. При нагревании активно взаимодействует с галогенами, серой и сернокислыми соединениями.
Маркировка ГДГ075/05: Г – германий, Д – дырочная электропроводность, Г – легирующая примесь галлий (Ga), 075 – удельное сопротивление (0,75Ом·см), 05 – диффузионная длина неосновных носителей заряда (0,5 мм), tприб = -60÷70оС.
Применяется для изготовления диодов, транзисторов, датчиков Холла, тензодатчиков, фотодиодов, фототранзисторов, модуляторов света, оптических фильтров, датчиков ядерных частиц.
Кремний, Si: IV группа периодической системы элементов, №14, ат.вес – 28,86, Тпл = 1412оС, ΔЕ = 1,12эВ (300К), ρ = 20Ом·м (20оС), ТКЛР = 4,2 10-3 град-1 (0-100оС), уд. плотн. = 2,3г/см3– один из самых распространённых элементов в земной коре (~ 29%), имеется только в соединениях в виде окислов и солей Si-кислот: монокристаллы кварца – чистота 99,9%; песок (в специальных месторождениях) – чистота 99,8÷99,9%.
Технический Si получают восстановлением кремнезёма (SiO2) в электрической дуге с графитовым электродом, примеси при этом составляют около 1%. Такой Si не может использоваться как полупроводник (примеси должны составлять 10-6%), он используется как сырьё для п/п Si.
Технология получения п/п Si: 1) превращение технического Si в легколетучее соединение, которое после очистки может быть легко восстановлено; 2) очистка соединения физическими и химическими методами; 3) восстановление соединения с выделением чистого Si; 4) конечная очистка Si методом бестигельной зонной плавки; 5) выращивание монокристаллов.
Метод водородного восстановления трихлорсилана (SiHCl3): технический Si обрабатывают сухим паром HCl (300÷400оС) по реакции Si + 3HCl ↔ SiHCl3 + H2 – получается жидкость с tкип= 32оС, которая легко очищается методами экстракции, адсорбции и ректификации.
|
|
|
Основная очистка Si от примесей осуществляется химическими методами. Кристаллизационные методы имеют цель превратить полукристаллический Si, полученный химическим путём, в монокристаллический Si с определёнными электрофизическими свойствами. Объёмные кристаллы Si выращивают методами выращивания из расплава (крупные монокристаллы с ρ < 2,5Ом·м) и бестигельной зонной плавки (для получения высокоомных монокристаллов с малым содержанием примесей).
Si более сложный материал в технологическом плане (tпл=1412оС) и в расплавленном состоянии весьма химически активен – вступает в реакцию со всеми тигельными материалами. Для выращивания монокристаллов Si метод вытягивания из расплава имеет недостаток: загрязнение монокристалла кислородом (источник – кварцевый тигель SiO2(тв) + Si(ж) → 2SiO), также при этом вводятся и другие примеси.
Методом вертикальной бестигельной плавки делают монокристаллы Si диаметром до 100мм. Si n-типа или р- типа проводимости получают введением при выращивании соответствующей примеси (Р или В), соответственно, марки КЭФ (кремний, электронная проводимость, фосфор) или КДБ(кремний, дырочная проводимость, бор).
Si п/п – основной материал п/п техники для создания микросхем и дискретных п/п приборов: низко- и высокочастотных, маломощных и мощных, полевых транзисторов, стабилитронов, тиристоров, фотодиодов, фототранзисторов, фотоэлементов солнечных батарей, датчиков Холла, тензодатчиков, детекторов ядерного излучения.
Карбид кремния, SiC: ΔЕ = 2,8÷3,1эВ, применяется в п/п приборах, работающих при температурах до 700оС.
Технический SiC изготавливается в электрических печах путём восстановления SiO2 (кварцевого стекла) углеродом: SiO2 +3C → SiC + 2CO. В печах образуются сросшиеся кристаллы SiC, называемые друзами (некоторые до 1,5÷2 см2), которые дробят до порошка SiC. Кристаллы SiC п/п чистоты получают методом возгонки в печах с графитовыми нагревателями и экранами. Процесс кристаллизации проводят в атмосфере Ar при 2400÷2600оС – получаются кристаллы пластинчатой формы с поперечным размером ~ 1см. SiC – очень твёрдый материал, не окисляющийся до температуры 1400оС, при комнатной температуре не взаимодействует ни с какими кислотами. При нагревании растворяется в расплавах щелочей, а также взаимодействует с ортофосфорной кислотой и смесью азотной и плавиковой кислот.
SiC применяется для выпуска вариаторов (нелинейных резисторов), светодиодов, а также высокотемпературных диодов, транзисторов, тензорезисторов, счётчиков частиц высоких энергий.
Бинарные соединения. Практическое применение находят соединения AIIIBV, AIIBVI, AIVBIV. Соединения AIIIBV являются ближайшими аналогами Si и Ge: III гр (B, Al, Ga, In) + V гр (N, P, As, Sb) – они классифицируются по металлоидному типу (нитриды, фосфиды, арсениды, антимониды). Получают из расплава, содержащего элементы в равных концентрациях, или из растворов соединений, имеющих в избытке элементы III группы, а также из газовой фазы.
Некоторые сведения из истории развития светодиодов (СД) [27]: 1) в 60-70-е годы 20 века были созданы СД, излучающие в ИК- области спектра (850÷930нм, ΔЕ = 1,3÷1,6эВ), которые с применением антистоксовых люминофоров, излучающих в зеленой области спектра, имели световую отдачу 1÷2 лм/Вт (кристаллы на основе GaAs); 2) в 1975-1976г.г. Алфёров Ж.И. сделал первый шаг к созданию эффективных СД – его школой разработана концепция многопроходных двойных гетероструктур (МДГС) в системе GaAlAs, получаемых методом жидкостной эпитаксии; 3) в1991г. для СД, излучающих в красной области спектра (650÷680 нм, ΔЕ = 1,6÷2эВ) получена световая отдача 10лм/Вт; 4) с 2000г. световая отдача СД увеличилась до 30÷40лм/Вт (на AlGaInP/GaAs), до 60лм/Вт (на InGaN), 100 лм/Вт (на AlGaInP/GaP), ожидается её рост до 150÷200лм/Вт с применением метода металлоорганического химического вакуумного напыления (диффузии) – метода MOCVD.
Кристаллы GaAs, InAs, InSb обычно выращивают из расплава вытягиванием на затравку из под инертного флюса, находящемся под давлением инертного газа, они требуют очистки, как для Si и Ge.
Для СД нового поколения применяются многослойные гетероструктуры на основе нитридных соединений (GaN, AlN, InN, InGaN) – это прямозонные широкозонные полупроводники с ΔЕ > 2,16эВ для СД зелёного, синего, фиолетового и ультрафиолетового излучения, для InGaN ΔЕ =2,4÷ ÷4эВ. Для структуры AlGaInP/GaP характерно красно-оранжевое излучение (ΔЕ = 1,7÷2,3эВ). СД белого света получается путём преобразования части синего излучения (структура InGaN) с помощью люминофора, излучающего в зелёно-оранжево-красной области спектра. Таким люминофором является алюмоиттриевый гранат, активированный церием, в котором добавкой галлия корректируется спектр излучения Се: Y3(Al,Ga)5O12:Ce.
Структура кристалла InGaNСтруктура кристалла AlGaInP/GaP

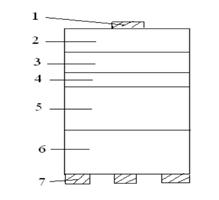
1. Ni – Au 1. Au-Zn
2. p-GaN:Mg (0,15мкм) 2. p-GaP
3. p-AlGaN (60нм) 3. p-AlGaInP (~1мкм)
4. Активная область – 4. Активная область-
структура квантовых ям структура квантовых ям
5. n-GaN:Si (5 мкм) 5. n-AlGaInP (~1мкм)
6. GaN- буферный слой(30нм) 6. n-GaAs или n-GaP
7. Сапфировая подложка 7. Au-Ge
8. Ti-Al
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 436; Нарушение авторских прав?; Мы поможем в написании вашей работы!