
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные типы фотохимических реакций
|
|
|
|
Это уравнение объединяет все законы фотохимии и является общим выражением для скорости фотохимической реакции.
Скорость фотохимической реакции зависит от интенсивности излучения 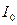 и не зависти от температуры
и не зависти от температуры  .
.
Все фотохимические реакции можно разбить по величинам 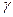 на четыре группы:
на четыре группы:
1) реакции, в которых квантовый выход  (образование бромциклогексана, перекиси водорода, нитрозометана);
(образование бромциклогексана, перекиси водорода, нитрозометана);
2) реакции, в которых  (разложение аммиака, ацетона)
(разложение аммиака, ацетона)
3) реакции, в которых  (образование озона, разложение двуокиси азота, бромистого водорода);
(образование озона, разложение двуокиси азота, бромистого водорода);
4) реакции, в которых квантовый выход  (реакция взаимодействия хлора с водородом и окисью углерода)
(реакция взаимодействия хлора с водородом и окисью углерода)
· реакции с  . Каждому поглощённому кванту соответствует одна прореагировавшая частица. Это истинно фотохимические процессы, подчиняющиеся закону квантовой эквивалентности Штарка-Эйнштейна. Отклонение
. Каждому поглощённому кванту соответствует одна прореагировавшая частица. Это истинно фотохимические процессы, подчиняющиеся закону квантовой эквивалентности Штарка-Эйнштейна. Отклонение 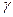 от единицы связано с тем, что фотохимический процесс состоит из трех основных стадий:
от единицы связано с тем, что фотохимический процесс состоит из трех основных стадий:
1) начальный акт поглощения света (приводит к образованию электроновозбужденной молекулы)
A + hv → A*
Это истинно фотохимический процесс, подчиняющийся закону квантовой эквивалентности Штарка-Эйнштейна. Квантовый выход такого процесса γ=1.
2) первичный фотохимический процесс (когда электроновозбужденная частица превращается в различного вида продукты реакции)
A* → неактивные частицы, γ<1
 – активные частицы, γ=1
– активные частицы, γ=1
3) вторичные процессы (идут без поглощения света и связаны с процессами дезактивации активных частиц, образующихся при поглощении кванта света в первичной реакции)
 , γ≠1
, γ≠1
· реакции с  . Характерно для двух типов реакций.
. Характерно для двух типов реакций.
1) реакции в растворах. Для всех них γ<1 за счет протекания первичных процессов:
|
|
|
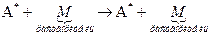 ,
,
а также за счет протекания вторичных процессов:
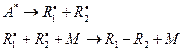
2) реакции в газовой фазе, протекающие при низких давлениях. Электроновозбужденные частицы испускают квант света до того, как сталкиваются с реагирующими молекулами.
Пример: разложение аммиака
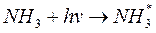 (начальный акт поглощения света)
(начальный акт поглощения света)
 (первичный процесс)
(первичный процесс)

| (вторичные процессы) |
По реакции (в) часть активных продуктов фотолиза возвращается в исходное состояние, что приводит к уменьшению 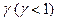 .
.
· реакции с  . При этом поглощение молекулой одного кванта приводит к появлению активной частицы, вызывающей развитие цепи. Часто
. При этом поглощение молекулой одного кванта приводит к появлению активной частицы, вызывающей развитие цепи. Часто 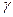 равен 2 или 3.
равен 2 или 3.
Пример:
а) разложение йодистого водорода:
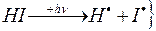 (первичный процесс)
(первичный процесс)

| (вторичные процессы) |
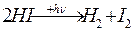
Таким образом, квантовый выход  , так как поглощение одного кванта вызывает реакцию двух молекул йодоводорода
, так как поглощение одного кванта вызывает реакцию двух молекул йодоводорода  .
.
б) образование озона из 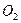 :
:


Таким образом, 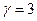 , так как поглощение одного
, так как поглощение одного 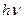 вызывает превращение трёх молекул
вызывает превращение трёх молекул 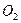 .
.
· реакции с  . Примером такой реакции является реакция
. Примером такой реакции является реакция 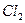 и
и 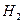 на свету.
на свету.  , то есть одному поглощённому кванту света соответствует около ста тысяч превращающихся молекул
, то есть одному поглощённому кванту света соответствует около ста тысяч превращающихся молекул 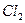 и
и 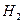 .
.
Различия между фотохимическими и обычными темновыми реакциями можно рассмотреть на примере образования 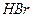 .
.
Темновая реакция: 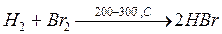
Состоит из следующих стадий:
| Темновая реакция | Фотохимическая реакция |
Первичный процесс: термическая реакция

|  (фотолиз)
Первичный процесс: (фотолиз)
Первичный процесс:

|
| Вторичные процессы: | |
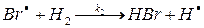 (2) (2)
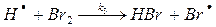 (3) (3)
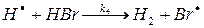 (4) (4)
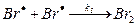 (5) (5)
|
Фотохимическая реакция зависит от интенсивности света и при комнатной темпаратуре идет в 500 раз быстрее темновой реакции. Таким образом, отличие фотохимической реакции от темновой только в первичном процессе, а вторичные процессы идентичны в обоих случаях.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1633; Нарушение авторских прав?; Мы поможем в написании вашей работы!