
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Характеристика тепловых процессов
|
|
|
|
Процессом называют переход тела из одного состояния в другое. Рассмотренные процессы в газах (изотермический, изобарический, изохорический, адиабатический) характерны тем, что при их осуществлении в окружающих телах никаких изменений не происходит, энергия системы не передается другим телам. Поэтому возможно и осуществление обратного перехода через последовательность тех же промежуточных состояний. Такие процессы называют обратимыми. Обратимые тепловые процессы всегда являются идеализацией в той или иной степени. Они возможны лишь при условии, что изменение параметров состояния происходит очень медленно и сама система каждый раз находится в состоянии равновесия, т.е. когда параметры всюду одинаковы. Лишь при этом возможен обратный процесс, когда система проходит ту же последовательность промежуточных состояний, что и в прямом процессе. Процесс, состоящий из ряда равновесных состояний, называют равновесный. Таким образом, все обратимые процессы - равновесные. Они изображаются графически плавной линией (АВ, рис. 10.1). Рассмотрим работу расширения и сжатия при обратимом и необратимом процессах. При быстром расширении процесс не будет обратимым и изобразится ступенчатой линией АаВ, аналогично при быстром сжатии ВвА. Таким образом, как видно из рис. 10.1,
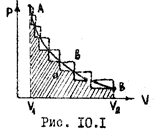
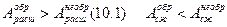
В равновесном состоянии в системе самопроизвольно никакие процессы не возникают. Если же ее вывести из этого состояния, то она в течение некоторого времени будет возвращаться в равновесное состояние. Причем из-за хаотичного движения молекул такой процесс будет необратимым. Таким образом, все самопроизвольные процессы протекают в направлении приближения системы к равновесному состоянию. Количественная формулировка этого положения составляет содержание второго начала термодинамики.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 529; Нарушение авторских прав?; Мы поможем в написании вашей работы!