
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Потенциал металлического электрода
При погружении металла в раствор собственных ионов устанавливается следующее равновесие:
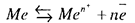
При равновесии растворение металла равно скорости разряда его ионов.
Потенциал, который устанавливается на электроде при равновесии, называется равновесным потенциалом. Для его измерения необходим гальванический элемент следующего вида:
H2, Рt | H+ | | Men+ | Me,
в котором токообразующая реакция будет реакцией следующего типа:
Men+ + n/2Н2→Me + nH+.
ЭДС этого элемента будет равна потенциалу электрода по водородной шкале:
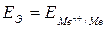 .
.
Поскольку [Н+]= 1, р(H2) = 1, то
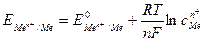 . (62)
. (62)
Уравнение (62 ) называется уравнением Нернста. Переходя от натурального логарифма к десятичному и подставляя во второе слагаемое температуру Т=298К и соответствующие значения R и F, получим расчетную форму уравнения Нернста:
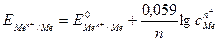 .
.
Для разбавленных растворов активность заменяется на концентрацию.
Стандартный электродный потенциал металла указывает на меру восстановительной способности его атомов и меру окислительной способности ионов металла. Чем более отрицательное значение имеет потенциал металла, тем более сильной восстановительной способностью он характеризуется. Чем более положителен потенциал металлического электрода, тем более сильной окислительной способностью обладают его ионы.
|
|
Дата добавления: 2014-01-06; Просмотров: 580; Нарушение авторских прав?; Мы поможем в написании вашей работы!