
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Формулы для расчета эквивалентов
|
|
|
|
Основные стехиометрические законы.
ЗАКОН СОХРАНЕНИЯ МАССЫ.
Массы веществ, вступающих в реакцию, равны массе веществ, получающихся в результате реакции.
ЗАКОН ПОСТОЯНСТВА СОСТАВА.
Каждое сложное вещество, независимо от способа его получения, имеет постоянный качественный и количественный состав. Следовательно, химические вещества взаимодействуют друг с другом в строго определенных (эквивалентных) соотношениях.
Эквивалент - это реальная или условная частица вещества, которая может присоединять, замещать, высвобождать один ион водорода в кислотно-основных и ионообменных реакциях или один электрон в окислительно-восстановительных реакциях.
Молярная масса эквивалентов - это масса одного моль эквивалентов, содержащая 6,02×1023 эквивалентов (Э).
[Э] = [г / моль×экв]
Эквивалент зависит от условий протекания реакций, а молярная масса - постоянна.
Э оксида = М оксида / число атомов элемента × валентность элемента
Э кислоты = М кислоты / основность кислоты
Основность кислоты определяется числом атомов водорода, которое кислота отдает, реагируя с основанием.
Э основания = М основания / кислотность основания Кислотность основания - количество ионов гидроксила, которые замещаются при взаимодействии с кислотой.
Э соли = М соли / число атомов Ме × валентность Ме, где (Ме - металл)
ЗАКОН ЭКВИВАЛЕНТОВ
Вещества взаимодействуют друг с другом в количествах, прямо пропорциональных их эквивалентам.
Массы (объемы) реагирующих веществ, прямо пропорциональны молярным массам (объемам) их эквивалентов.
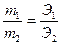
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 2311; Нарушение авторских прав?; Мы поможем в написании вашей работы!