
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамический процесс
|
|
|
|
Термодинамический процесс – изменение состояния термодинамической системы во времени.
Пример: при перемещении поршня в цилиндре объем, а с ним давление и температура находящегося внутри газа будут изменятся, будет совершаться процесс расширения или сжатия.
Как уже было сказано, система, выведенная из состояния равновесия, и предоставленная при постоянных параметрах окружающей среды самой себе, через некоторое время вновь придет в равновесное состояние, соответствующее этим параметрам. Самопроизвольное возвращение системы в состояние равновесия называется релаксацией. Время, в течение которого система возвращается в состояние равновесия, называется временем релаксации. Для разных процессов время релаксации различно.
Например, для установления равновесного давления в газе требуется всего 10-16 с, а для выравнивания температуры в объеме того же газа нужны десятки минут. Для твердых тел выравнивание температур иногда требует нескольких часов.
Равновесный термодинамический процесс – если все параметры системы при его протекании меняются достаточно медленно по сравнению с соответствующим процессом релаксации. В этом случае система фактически все время находится в состоянии равновесия с окружающей средой, чем и определяется название процесса.
Чтобы процесс был равновесным скорость изменения параметров системы 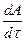 должна удовлетворять соотношению
должна удовлетворять соотношению
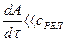
где А – параметр, наиболее быстро изменяющийся в рассматриваемом процессе;
сРЕЛ – скорость изменения этого параметра в релаксационном процессе.
Например, рассмотрим процесс сжатия газа в цилиндре. Если время смещения поршня от одного положения до другого существенно превышает время релаксации, то в процессе перемещения поршня давление и температура успеют выравняться по всему объему цилиндра. Это выравнивание обеспечивается непрерывным столкновением молекул, в результате чего подводимая от поршня к газу энергия достаточно быстро и равномерно распределяется между ними. Если последующие смещения поршня будут происходить аналогичным образом, то состояние системы в каждый момент времени будет практически равновесным.
|
|
|
Таким образом, равновесный процесс состоит из непрерывного ряда последовательных состояний равновесия. Соответственно в каждой его точке состояние термодинамической системы можно описать уравнением состояния данного рабочего тела. Классическая термодинамика в своих исследованиях оперирует только равновесными процессами. Они являются удобной идеализацией реальных процессов, позволяющей во многих случаях существенно упростить решение задачи. Такая идеализация вполне обоснована, так как условие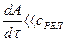 выполняется на практике достаточно часто. Поскольку механические возмущения распространяются в газах со скоростью звука, процесс сжатия газа в цилиндре будет равновесным, если скорость перемещения поршня много меньше скорости звука.
выполняется на практике достаточно часто. Поскольку механические возмущения распространяются в газах со скоростью звука, процесс сжатия газа в цилиндре будет равновесным, если скорость перемещения поршня много меньше скорости звука.
Процессы, не удовлетворяющие условию 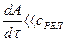 , протекают с нарушением равновесия, т.е. являются неравновесными.
, протекают с нарушением равновесия, т.е. являются неравновесными.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 200; Нарушение авторских прав?; Мы поможем в написании вашей работы!