
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ионная связь. Ионную связь можно рассматривать как предельный случай ковалентнорй полярной связи
|
|
|
|
Ионную связь можно рассматривать как предельный случай ковалентнорй полярной связи. В общем случае это связь, образующаяся в результате электростатического притяжения разноименных ионов. В отличии от ковалентной связи ионная не обладает насыщенностью и направленностью. Причина этого равномерное распределение электрического поля вокруг каждого иона. Однако ионная связь имеет ряд особенностей: поляризация и поляризуем ость
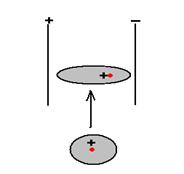 Поляризация – смещение электронной плотности иона в электрическом поле.
Поляризация – смещение электронной плотности иона в электрическом поле.
Сам ион способен создавать вокруг себя электрическое поле, которое деформирует близлежащую заряженную частицу. Однако, при действии одного и того же электрического поля, поляризуемость различных ионов неодинакова. Чем слабее связаны внешние электроны с ядром, т.е. чем больше атомный радиус, тем сильнее он деформируется. Превращение атома в положительно заряженный ион всегда приводит к уменьшению его размеров. Кроме того, избыточный положительный заряд катиона затрудняет деформацию его внешних электронных облаков. Напротив отрицательно заряженные ионы всегда имеют большие размеры, чем нейтральные атомы, а избыточный отрицательный заряд приводит здесь к отталкиванию электронов, и следовательно ослаблению их силы связывания с ядром. Поляризующая способность ионов, т.е. их способность оказывать деформирующее действие на другие ионы также зависит от их размеров.
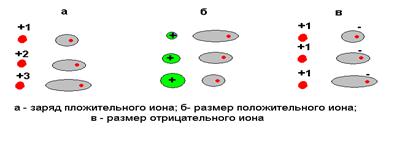
Главной характеристикой такой способности является ионный потенциал- отношение радиуса к заряду. Чем он больше, тем ярче проявляется его активность в поляризации внешних орбиталей соседнего иона, и наоборот, чем меньше значение, тем слабее поляризующая активность. Поляризация ионов оказывает заметное влияние на свойства образуемых ими соединений. Поскольку с усилением поляризации возрастает энергия связи, то это сказывается, например, на диссоциацию солей в водных растворах Примером может служить растворение BaCI2 и нерастворение HgCI2 воде. Радиус катиона бария значительно больше чем катиона ртути. Заряд одинаков. Ионный потенциал катиона ртути соответственно больше чем таковой у бария. Следствие этого практически полная нерастворимость хлорида ртути в воде.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 874; Нарушение авторских прав?; Мы поможем в написании вашей работы!