
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Квантовая механика атома водорода. Квантовые числа
|
|
|
|
Как следует из анализа экспериментальных данных, чтобы задать однозначно состояние атома, необходимы четыре различных квантовых числа.
Для атома водорода квантовая механика предсказывает точно те же энергетические уровни, что и теория Бора. В теории Бора существует только одно квантовое число п, которое получило название главного квантового числа. Это число сохранилось и в квантовой механике. По смыслу оно описывает номер энергетического уровня.
Главное квантовое число (n) – квантовое число, определяющее энергетические уровни электрона в атоме: n=1,2,3,...∞. 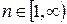
Однако экспериментальные данные о спектрах сложных атомов не объяснялись с точки зрения теории Бора.
Объяснение этих данных потребовало введение еще одного квантового числа, которое получило название орбитального квантового числа.
Орбитальное квантовое число (l) –квантовое число, определяющее момент импульса электрона в атоме, изменяется в пределах: l=0,1,2,…,n-1. 
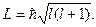 |
Момент импульса электрона (механический орбитальный момент равен l=mvrn) в квантовой механике имеет вид:
В атоме водорода полная энергия не зависит от значения l, а зависит только от п. Но в атомах с двумя и большим числом электронов энергия зависит от обоих квантовых чисел п и l.
Однако и этих двух квантовых чисел оказалось недостаточно. Оказалось, что в некоторых условиях эти уровни начинают расщепляться. Например, расщепление спектральных линий, соответствующих энергетическим уровням, на несколько, близко лежащих по энергии друг от друга линий, происходит при помещении атома в магнитное поле (в этом случае наблюдаемое расщепление получило название эффекта Зеемана). Набор расщепленных линий получил название тонкой структуры атома. Для объяснения этого эффекта понадобилось введение еще одного квантового числа, которое возникло по результатам анализа экспериментов в магнитном поле и получило название «магнитного квантового числа».
|
|
|
Магнитное квантовое число (m) – квантовое число, определяющее проекцию момента импульса электрона на заданное направление: m=0,±1,±2,...,±l, всего (2l+1) значений  .
.
Именно наличие магнитного квантового числа приводит к расщеплению энергетического уровня на 2l+1 подуровней (рис.13.6). Расщепление атомных уровней в магнитном поле на несколько близких по энергии линий получило название тонкой структуры.
Это квантовое число с точки зрения классической механики определяет ориентацию момента количества движения в пространстве. В квантовой механике ориентацию момента импульса обычно задают, указывая компоненту вдоль оси z. Компонента 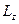 связана с магнитным квантовым числом m соотношением:
связана с магнитным квантовым числом m соотношением:
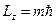
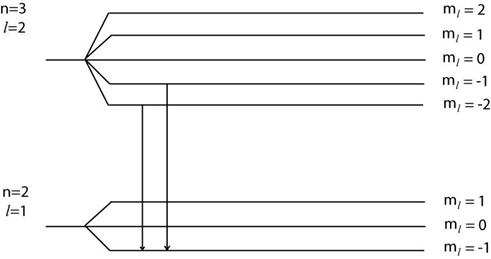
Рис. 13.6. Тонкая структура атома водорода. Уровень 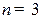 ,
,  расщепляется на 5 подуровней
расщепляется на 5 подуровней  , уровень
, уровень 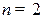 ,
, 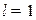 на 3 подуровня
на 3 подуровня 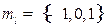
Тонкая структура была обнаружена при осуществлении разряда в водороде, помещенном в магнитном поле[5]. Магнитный момент L можно интерпретировать по аналогии с круговым током. Движение электрона в атоме по круговой орбите можно представить как круговой ток, который создает магнитное поле вдоль оси, перпендикулярной плоскости витка.
Наличие трех квантовых чисел не смогло дать объяснение всех экспериментальных данных. Тщательное исследование спектральных линий атома водорода показало, что каждая линия в действительности состоит из двух линий, находящихся очень близко друг от друга. Такое расщепление уровней получило название сверх тонкой структуры атомных уровней. Для их объяснения появилось четвертое квантовое число, называемое спином. С точки классической механики это как бы вращение электрона вокруг своей оси, как, например, Земля, вращаясь вокруг Солнца, еще вращается и вокруг своей оси. Момент количества движения электрона или внутренний момент в этом случае может иметь два направления «вверх» и «вниз».
|
|
|
Спин электрона (s) – собственный неуничтожаемый механический момент импульса, не связанный с движением электрона в пространстве. Спин[6] элементарных частиц, а также других микрочастиц, (в том числе ядер и атомов) – это квантовая величина, у которой нет классического аналога; это – внутреннее неотъемлемое свойство электрона. У электрона спин равен ½. Вводится понятие проекции спина на некоторую ось, проходящую через частицу. Проекции спина 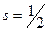 составляют
составляют 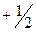 ,
, 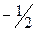 , то есть проекции спина принимают значения от +s до –s:
, то есть проекции спина принимают значения от +s до –s: 
Как оказалось, этих четырех квантовых чисел (n, l, ml, s) достаточно, чтобы описать спектры всех сложных атомов с любой заданной точностью.
На пальцах, описанные выше квантовые числа можно связать с классическими аналогиями для более полного представления их физического смысла. Главное квантовое число n описывает номер стационарной орбиты, орбитальный момент l – момент количества движения электрона вокруг ядра, а спин s – момент количества движения электрона вокруг своей оси, а магнитный момент ml - число возможных ориентаций плоскости орбиты электрона в атоме.
Принцип запрета Паули. В дальнейших исследованиях было установлено, что электроны в атоме не могут иметь четыре квантовых числа одинаковыми. Хотя бы одним из них, состояния двух электронов обязательно должны отличаться. Такой принцип был введен Вольфгангом Паули[7] и получил название принцип запрета Паули. Он гласит:
Два электрона не могут находиться в атоме в одном и том же квантовом состоянии.
Энергетические уровни сложных атомов (с двумя и более электронами) можно определить экспериментально по спектрам испускания. Число электронов в нейтральном атоме называется атомным номером Z. Число Z также равно положительному заряду (числу протонов) ядра и определяет свойства атома.
Простейший подход для описания сложных атомов был основан на предположении, что каждый электрон в атоме находится в состоянии, которое характеризуется квантовыми числами n, l, m, s. Но для объяснения возможных конфигураций электронов в атоме оказался необходим новый принцип.
|
|
|
Принцип запрета Паули составляет основу для понимания не только структуры сложных атомов, но и природы молекул, химической связи и ряда других явлений.
Оболочки или уровни атома связывают с главным квантовым числом n. Для разных значений орбитального момента l энергия уровня может оказываться различной, что происходит при помещении его в электрическое поле. В этом случае уровень расщепляется на подуровни (подоболочки).
Подоболочки атома обозначают буквами латинского алфавита:
0 1 2 3 4 ……
s p d f g ……
Квантовая механика прекрасно описала систему уровней в молекулах. В них кроме движения электронов относительно ядер происходит колебание атомов около их положений равновесия и вращательное движение молекул. Причем энергия всех видов движения принимает дискретные значения. Движению электронов, колебательному и вращательному движению атомов и молекул соответствует три типа уровней с энергиями Еэлект, Еколеб, Евращат. Полная энергия молекулы представляет собой сумму перечисленных видов энергий:
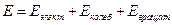 .
.
Расстояние между электронными уровнями порядка единиц электронвольт, между колебательными уровнями – порядка 10-2 – 10-1 эВ, а между вращательными - 10-3 – 10-5 эВ.
Пример.13.1. Каково строение атома гелия 4Не.
n1=n2=1, l1=l2=0, m1=m2=0, s1=-1/2, s2=+1/2.
Структура атома 4Не →1s2. Это означает, что в атоме гелия главное квантовое число n=1, символ (s) означает, что орбитальный момент l=0. Этими квантовыми числами обладают два электрона. Их общее состояние отличается лишь направлением спина.
Пример13.2. Каково строение атома лития 6Li.
n1=1, l1=0, m1=0, s1=-1/2.
n2=1, l2=0, m2=0, s2=+1/2.
n3=2, l3=0, m3=0, s1=-1/2.
Структура атома 6Li →1s22s1. В атоме лития заняты два энергетических уровня с главными квантовыми числами n=1 и n=2. На первой оболочке располагается два электрона с орбитальным моментом l=0 (1s2), а на второй оболочке – один электрон также при l=0 (2s1).
Пример13.3. В таблице 13.1 приведено строение оболочек атомов первых десяти элементов периодической таблицы Менделеева.
|
|
|
Таблица 13.1. Структура оболочек атомов.

У первых двух элементов электроны находятся на одной оболочке, у остальных вторая оболочка расщепляется на две подоболочки с l=0 (s-подоболочка) и c l=1 (р-подоболочка).
Пример.13.4. Какова оболочечная структура атома натрия 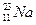 .
.
Оболочечная структура атома натрия имеет вид 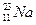 → 1s22s22р63s1. На первом уровне здесь, как и в других атомах, находится 2 электрона (для квантового числа n=1 и орбитального момента l=0). На втором уровне помещается 8 электронов, причем 2 электрона на s-подоболочке (l=0) и 6 электронов на р-подоболочке (l=1). На третьей оболочке (при l=0) располагается одиннадцатый электрон.
→ 1s22s22р63s1. На первом уровне здесь, как и в других атомах, находится 2 электрона (для квантового числа n=1 и орбитального момента l=0). На втором уровне помещается 8 электронов, причем 2 электрона на s-подоболочке (l=0) и 6 электронов на р-подоболочке (l=1). На третьей оболочке (при l=0) располагается одиннадцатый электрон.
Пример 13.5. Электронный микроскоп [8]. Принцип волнового дуализма, соотношения неопределенностей лежит в основе конструкции электронных микроскопов. Поэтому прохождение электронов в них может быть интерпретировано как прохождение света в оптическом микроскопе. Физическая идея электронного микроскопа заключается в рассеянии электронов на биологических объектах (тонких срезах). Причем энергия электронов должна быть такой, чтобы не разрушать молекулярные связи. Скорость электронов v в электронном микроскопе определяется из соотношения:
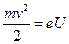 , (13.4.1)
, (13.4.1)
где U – ускоряющая разность потенциалов. Длина волны электронов λ вычисляется, подставляя значение скорости из выражения (13.4.1) в формулу (13.1.1):
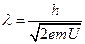 . (13.4.2)
. (13.4.2)
Для ускоряющего напряжения U=100кВ длина волны электронов составляет порядка 0.1 нм, что с учетом всех погрешностей прибора позволяет исследовать объекты размером 0.2 нм. Такое разрешение (порядка 10-10 м) недостижимо в оптических микроскопах, в которых пространственное разрешение на два – три порядка хуже. Оптические микроскопы позволяют рассматривать детали объектов до 0.1 - 0.2 мкм.
Разрешающая способность электронного микроскопа в 1000÷10000 раз превосходит разрешение оптического микроскопа и для лучших современных приборов может составлять несколько ангстрем.
Увеличение в самых сильных оптических микроскопах оказывается в ~500 раз хуже, чем в электронных микроскопах, и достигает примерно миллион раз. Существует несколько видов электронных микроскопов: просвечивающий, растровый, растровый просвечивающий и растровый туннельный. Схематическая конструкция, построения изображения и основные элементы двух типов электронных микроскопов (просвечивающего и сканирующего) представлены на рис.13.7.
На рис.13.7б представлена схема просвечивающего электронного микроскопа, позволяющего получить двухмерное изображение объекта. На рис.13.7а изображен растровый сканирующий микроскоп, на котором получают трехмерное изображение объекта.
Конструктивно электронный микроскоп состоит из электронной пушки, которая представляет собой ускоритель электронов на низкие энергии от 30 до 200 кэВ, системы электрических и магнитных фокусирующих и рассеивающих линз (играющих ту же роль, что оптические линзы – объектив и окуляр), детектора рассеянных на биологическом образце электронов (фотопластинки или люминесцентного экрана).
Просвечивающий электронный микроскоп [9] (ПЭМ) — это установка, в которой изображение от ультратонкого объекта (толщиной порядка 0,1 мкм) формируется в результате взаимодействия пучка электронов с веществом образца с последующим увеличением магнитными линзами (объектив) и регистрацией на флуоресцентном экране. С помощью первой магнитной линзы формируется параллельный пучок электронов, который падает на объект. Электроны проходят сквозь объект, причем они по-разному рассеиваются на каждой из рассматриваемых структур, формируя изображение элементов объекта. Их энергия выбирается так, чтобы они не разрушали рассматриваемые элементы объекта. Далее пучок попадает на вторую магнитную линзу – объектив, которая увеличивает изображение. Затем, как в обычном оптическом телескопе, электроны проходят через окуляр.
Сканирующий (или растровый) электронный микроскоп [10] (РЭМ) основан на отражении электронного пучка от объекта. Принцип работы РЭМ, заключающийся в сканировании поверхности образца сфокусированным электронным пучком, анализе отраженных от поверхности электронов и рентгеновского излучения, возникающего в результате их взаимодействия с веществом.
Изображение поверхности объекта формируется с пространственным разрешением в несколько нанометров, что позволяет получать сведения о составе, строении и некоторых других свойствах приповерхностных слоёв исследуемых образцов.
Современные растровые микроскопы позволяют увеличивать изображение до 1 миллиона раз, что превышает предел увеличения оптическими микроскопами в ~ 500 раз. В них используются пучки электронов до энергии 50 кэВ. Наилучшее разрешение на 2009 год составляет 0.4 нм.
Анализ пучка отраженных электронов позволяет получать информацию о рельефе поверхности, о кристаллической структуре приповерхностных слоёв, а анализ возникающего в процессе взаимодействия пучка электронов с образцом рентгеновского излучения, позволяет качественно и количественно охарактеризовать химический состав приповерхностных слоёв.
На электронных микроскопах можно исследовать крупные молекулы, структуру вещества или тканей. Изменяя напряжение можно варьировать разрешение микроскопа.
Электронные микроскопы широко используются в биологии, медицине, науках о материалах, нанотехнологиях, промышленности.
а) б)
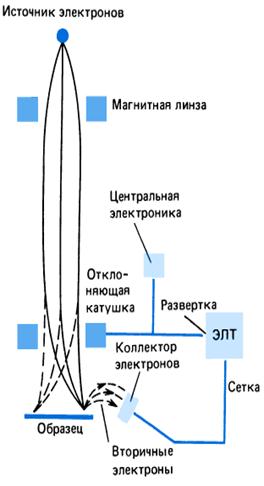
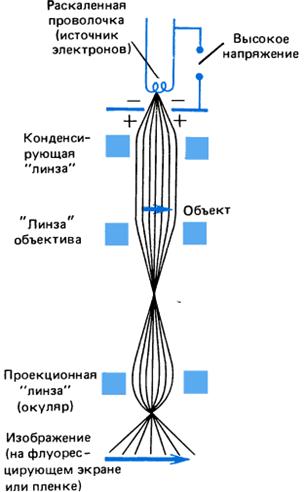
Рис.13.7. Схема растрового (а) и просвечивающего (б) электронного микроскопа.
Явление ядерного магнитного резонанса (ЯМР) является одним из практических примеров использования квантово-механических принципов. Магнитный резонанс – это избирательное поглощение веществом электромагнитных волн определенной частоты, обусловленное изменением ориентации магнитного момента частиц вещества. Когда поглощение энергии происходит только атомными ядрами – магнитный резонанс называют ядерным магнитным резонансом. ЯМР – квантовый эффект, который наблюдается, когда на вещество действуют взаимно перпендикулярно магнитное поле 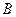 и слабое радиочастотное. Ядерный магнитный резонанс основан на эффекте Зеемана[11]. В этом случае энергетические уровни ядра, обладающего магнитным моментом
и слабое радиочастотное. Ядерный магнитный резонанс основан на эффекте Зеемана[11]. В этом случае энергетические уровни ядра, обладающего магнитным моментом 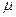 , расщепляются в магнитном поле на подуровни. Каждому из подуровней соответствует определенная ориентация магнитного момента относительно внешнего магнитного поля
, расщепляются в магнитном поле на подуровни. Каждому из подуровней соответствует определенная ориентация магнитного момента относительно внешнего магнитного поля 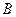 . Электромагнитное поле резонансной частоты
. Электромагнитное поле резонансной частоты 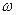 вызывает квантовые переходы
вызывает квантовые переходы 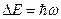 между этими подуровнями, которые определяются различными значениями магнитного квантового числа
между этими подуровнями, которые определяются различными значениями магнитного квантового числа 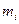 .
.
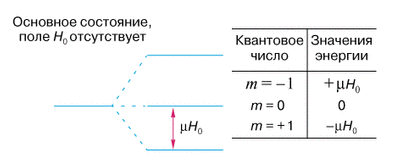
Рис.13.8. Эффект Зеемана.
Таким образом, при ЯМР происходит поглощение или излучение электромагнитной энергии веществом на некоторой частоте, называемой частотой ЯМР. В обычно применяемых магнитных полях 0.1 – 6 Тл частоты ЯМР попадают в диапазон коротких радиоволн 106 – 107 Гц. На этом принципе действуют магнитные резонансные томографы.
Пример.13.6. Магнитно - резонансный томограф (МРТ) [12]. Физические основы МРТ - томографии основываются на использовании ядерного магнитного резонанса и определяются магнитными свойствами атомных ядер. Биологическая среда - это в основном ядра атомов водорода 1H (протоны). Они обладают ядерным спином 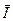 и механическим моментом вращения
и механическим моментом вращения 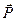 , который обуславливает появление магнитного момента
, который обуславливает появление магнитного момента 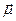 ядра (рис.13.8а). При наличии внешнего магнитного поля ядро вращается вокруг своей оси и способно взаимодействовать с внешним магнитным полем, то есть прецессирует вокруг его направления (рис 13.8б). Частоту прецессии определяют из уравнения Лармора:
ядра (рис.13.8а). При наличии внешнего магнитного поля ядро вращается вокруг своей оси и способно взаимодействовать с внешним магнитным полем, то есть прецессирует вокруг его направления (рис 13.8б). Частоту прецессии определяют из уравнения Лармора:
 , (13.4.3)
, (13.4.3)
где w0 – угловая частота Лармора; g - гиромагнитное отношение, зависящее от свойств ядер (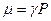 ); В0 – напряженность постоянного магнитного поля, в котором находится ядро.
); В0 – напряженность постоянного магнитного поля, в котором находится ядро.
Вторым физическим законом, положенным в основу МРТ – томографа является наличие у ядер (как и у атомов) квантовой характеристики - спина. Протоны имеют полуцелый спин s=1/2, что является причиной существования двух уровней, отличающихся спином. Поэтому для протонов существует два конуса прецессии: один - для ядер в состоянии с низкой энергией, а другой - для ядер в состоянии с высокой энергией.
Полезный сигнал в МРТ - томографах возникает в результате взаимодействия радиоволн с веществом. В состоянии равновесия несколько большее количество ядер находится на нижнем энергетическом уровне, что приводит к возникновению макроскопической намагниченности. Для того, чтобы вызвать переход ядра с нижнего энергетического уровня на верхний, необходимо воздействовать на систему.
Радиоволны можно рассматривать как кванты энергии. Действие радиочастотного импульса (рис.13.8в) приводит к квантовому переходу ядер с более низкого энергетического уровня в возбужденное состояние (на более высокий по энергии уровень). Переход осуществляется при поглощении квантов энергии (радиосигнала частоты 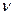 ), равных разности энергий между двумя уровнями
), равных разности энергий между двумя уровнями  . При отключении радиосигнала (рис.13.8г) протоны возвращаются в прежнее состояние и излучают энергию
. При отключении радиосигнала (рис.13.8г) протоны возвращаются в прежнее состояние и излучают энергию 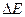 , что соответствует ЯМР - сигналу. При этом каждое ядро, возвращающееся в низшее энергетическое состояние, будет излучать энергию. Если радиочастотный импульс близок по частоте к ларморовой частоте ядер, то наблюдается резонанс. В этом случае амплитуда получаемого сигнала значительно усиливается. Этот сигнал с помощью преобразования Фурье раскладывают на частотные компоненты и определяют интенсивность каждой из них.
, что соответствует ЯМР - сигналу. При этом каждое ядро, возвращающееся в низшее энергетическое состояние, будет излучать энергию. Если радиочастотный импульс близок по частоте к ларморовой частоте ядер, то наблюдается резонанс. В этом случае амплитуда получаемого сигнала значительно усиливается. Этот сигнал с помощью преобразования Фурье раскладывают на частотные компоненты и определяют интенсивность каждой из них.
Принцип действия МРТ – томографа напоминает принципы достижения инверсионной заселенности высокоэнергичных уровней атомов или их соединений в рабочих кристаллах лазеров. Возвращение этих атомов в основное состояние позволяет усилить световой или радиочастотный сигнал.
Таким образом, в МРТ – томографе происходит облучение радиосигналом определенного среза тканей, а при выключении его возникает ответный сигнал облученных тканей. Расшифровка этого сигнала позволяет судить о наличии патологий в тканях. Осуществляя много срезов и объединяя полученные результаты можно определить размер патологического очага.
Любой МРТ – томограф (рис.13.9) включает в себя магнит большого размера, градиентные катушки и электронику, передатчик и приемник радиоимпульсов, источник питания, систему охлаждения, компьютерную систему получения и обработки сигналов, пульт управления оператора.
МРТ-томографы классифицируются по типу источника основного магнитного поля: постоянные, резистивные, сверхпроводящие и гибридные системы. В зависимости от напряженности основного магнитного поля МРТ-томографы делятся на несколько типов: томографы с ультранизким магнитным полем (0.02 – 0.01 Тл), с низким полем (0.1-0.3 Тл), со средним полем (0.3-0.6 Тл), с сильным полем (0.6-3 Тл). Для фундаментальных исследований созданы томографы с индукцией магнитного поля 10 -15 Тл и выше.
а) б) в) г)
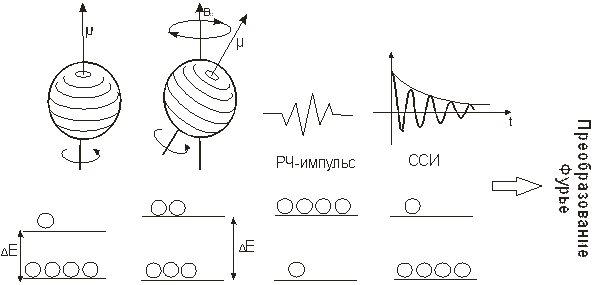
Рис.13.8. Принцип приема и передачи сигнала в МРТ – томографе.

Рис. 13.9. Важнейшие составные части МРТ-томографа. 1. Стол для пациентов. 2. Охлаждающая система 3. Вакуумная оболочка, 4. Главные катушки, сверхпроводящие, 5. Система перемещения стола, 6,7. Электронные шкафы с данными и для передатчика высокой частоты. 8,9. Система управления и обработки данных.
Контрольные вопросы к лекции №13:
1. Почему возникла необходимость в квантовой механике?
2. В чем заключалась гипотеза де Бройля?
3. Сформулируйте условие квантования?
4. В чем заключается принцип дополнительности?
5. Что такое квантовая механика?
6. Расскажите о волновой функции.
7. Напишите уравнение Шредингера.
8. В чем смысл принципа неопределенности?
9. Как выглядит квантовомеханическая картина строения атома?
10. Расскажите о квантовом осцилляторе.
11. Какие Вы знаете квантовые числа? В чем их смысл?
12. Объясните смысл принципа Паули.
13. Напишите структуру ядра 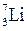 .
.
14. Расскажите о принципе действия электронного микроскопа.
15. Какие виды электронных микроскопов Вы знаете? В чем их различие?
16. Расскажите, какие положения квантовой механики лежат в основе действия магнитного резонансного томографа.
17. Что общего между действием лазера и МРТ – томографа?
[1] Луи де Бройль (1892-1987) – знаменитый французский физик. Получил сначала образование историка, а затем физика в Парижском университете. В 1929 году «за открытие волновой природы электронов» де Бройль был удостоен Нобелевской премии по физике. Член французской Академии наук.
[2] Эрвин Шрёдингер (1887—1961) австрийский физик-теоретик, один из создателей квантовой механики, иностранный почетный член (1934) АН СССР. Разработал (1926) так называемую волновую механику, сформулировал ее основное уравнение Шредингера, доказал ее идентичность матричному варианту квантовой механики. Он проводил исследования в области кристаллографии, математической физики, теории относительности, биофизики. В 1933 году удостоен Нобелевской премии по физике.
[3]В.Гейзенберг (1901-1976) немецкий физик. За создание квантовой механики в 1932 году удостоен Нобелевской премии по физике
[4] Для понимания выражения «оператор» запишем, где знак интеграла является оператором, превращающим скорость в путь. Другой пример. В этом случае скорость определяется при действии оператора производной на зависимость координаты от времени.
[5] Это явление называют эффектом Зеемана.
[6] Для понимания смысла спина его можно представить в виде внутреннего вращения материи частицы вокруг некоторой оси, которую считают направлением спина.
[7] Швейцарский физик ВольфгангПаули (1890 – 1958) В 1930 году теоретически предсказал существование нейтрино, в 1945 был награжден Нобелевской премией по физике «за открытие принципа запрета, который называют также принципом запрета Паули».
[8] В 1931 году Р. Руденберг получил патент на просвечивающий электронный микроскоп, а в 1932 году немецкие инженеры М. Кнолль и Э. Руска построили первый прототип современного прибора. Эта работа Э. Руски в 1986 году была отмечена Нобелевской премией по физике, которую присудили ему и изобретателям сканирующего зондового микроскопа Герду Карлу Биннигу и Генриху Рореру.
[9] Первый практический просвечивающий электронный микроскоп был построен А. Пребусом и Дж. Хиллиером в университете Торонто (Канада) в 1938 году с использованием идеи, предложенной ранее М. Кноллом и Э.Руска.
[10] Сканирующий электронный микроскоп был впервые предложен в работах немецкими учеными М.Кноллом и М.Арденне в 1930 годы, а в 1938 году М. Арденне построил такой микроскоп.
[11] Расщепление уровней в магнитном называют эффектом Зеемана.
[12] Ядерный магнитный резонанс (ЯМР) был открыт в 1938 году И.Раби, за что в 1944 году он был удостоен Нобелевской премии. За открытие и первое успешное определение ЯМР сигнала в жидкостях и вердых телах Ф. Блох и Э. Парселл в 1952 году получили Нобелевскую премию в области физики. Позднее, еще три Нобелевские премии по химии, медицине и биологии были получены за открытия в области применения ЯМР. В 1991 году и 2002 году За работы по развитию ЯМР – спектроскопии были получены две Нобелевские премии по химии, а в 2003 году – Нобелевская премия по физиологии и медицине. Хотя ЯМР –томография и ЯМР –спектроскопия были изобретены в 1960 году российским ученым В.А. Ивановым.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 7488; Нарушение авторских прав?; Мы поможем в написании вашей работы!