
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ненасыщенные галогенпроизводные
|
|
|
|
Галогенпроизводные ароматических углеводородов
Углеводородов
Изомерия. Номенклатура. Три типа галогенпроизводных с двойной связью.
Винилгалогениды. Способы получения: из вицинальных дигалогенидов, алкенов и ацетиленовых углеводородов. Строение винилхлорида, причины инертности винилгалогенидов в реакциях нуклеофильного замещения. Электрофильное присоединение галогенов и галогенводородов. Промышленные способы получения винилхлорида. Поливинилхлориды.
Аллилгалогениды. Способы получения: из алкенов (аллильное хлорирование и бромирование), присоединение галогенводородов к сопряженным диенам. Строение аллилгалогенидов. Причины их повышенной реакционной способности в реакциях SN1 и SN2.
Галогенпроизводные ароматических углеводородов. Гомологический ряд. Изомерия. Классификация. Номенклатура. Способы получения: из бензола и его гомологов, галогенирование в ядро и боковую цепь, условия реакции, механизм. Химические свойства. Реакции нуклеофильного замещения галогена. Причины инертности арилгалогенидов. Механизмы реакции. Влияние электроноакцепторных заместителей на реакционную способность.
Ненасыщенные галогенпроизводные в зависимости от удаления атома галогена от кратной связи делят на три группы:
а) атом галогена находится при атоме углерода с кратной связью
(СН2=СН-Cl) – винилгалогенид.
б) галоген удален от кратной связи на одну метиленовую группу
(СН2=СН-СН2-Cl) – аллилгалогенид.
в) галоген удален более чем на одну метиленовую группу
(СН2=СН-(СН2)2-Cl)
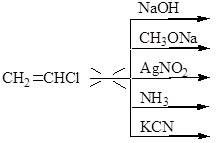
а) Хлористый винил СН2=СН-Cl можно получить в результате следующих химических превращений:
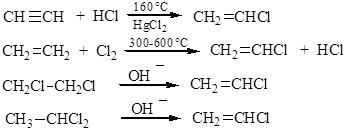
Рассмотрим химические свойства этих соединений в двух аспектах: а) влияние двойной связи на реакционную способность галогена, б) влияние галогена на реакционную способность двойной связи.
|
|
|
Галогенпроизводные группы а) отличаются малой подвижностью галогена, что объясняется эффектом сопряжения неподеленной пары электронов галогена с электронами кратной связи, приводящее к изменению кратности связи (больше 1) С-Cl, увеличению энергии связи и уменьшению ее длины.
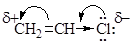
Данные по дипольным моментам и длинам связей (табл. 4) подтверждают это рассуждение
Таблица 13.1
Дипольные моменты, энергии и длины связей хлорэтана и хлорэтилена
| Вещество | Длина связи С-Сl, Å | Дипольный момент, D | Энергия связи, ккал/моль |
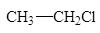
| 1,77 | 2,02 | |
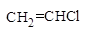
| 1,69 | 1,44 |
Обычные реакции нуклеофильного замещения, характерные для алкилгалогенидов, невозможны для хлористого винила и подобных ему соединений.
С другой стороны, атом галогена в значительной степени снижает электронную плотность С=С, благодаря своему отрицательному индукционному эффекту, и реакции электрофильного присоединения по С=С связи затрудняются.
Присоединение происходит в соответствии с правилом Марковникова:
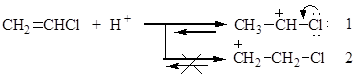
Реакция присоединения протекает через стадию образования более стабильного катиона (1).

б) Галоген находится в a-положении по отношению к кратной связи:
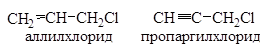
Хлористый аллил получают в промышленности высокотемпературным хлорированием пропилена:
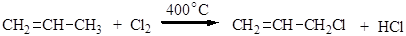
Для галогена этой группы соединений характерна максимальная реакционная способность (подвижность) в реакциях замещения. Это связано со способностью аллилгалогенидов к диссоциации
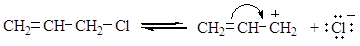
Способность к диссоциации объясняется большой устойчивостью образующегося карбониевого катиона по сравнению с алкильным карбониевым катионом:
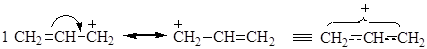
В этом случае p-электроны С=С связи в большей степени гасят положительный заряд, чем положительный индукционный эффект алкильной группы и эффект сверхсопряжения в алкилгалогенидах. Реакция замещения атома хлора в аллилгалогенидах протекает по механизмам SN1, в этом случае возможна перегруппировка.
|
|
|
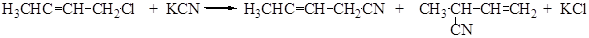
в) Галоген удален от двойной связи двумя и более С-С связями
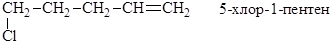
В этом случае свойства галогена аналогичны свойствам галогена в галоидных алкилах, а свойства двойной связи аналогичны свойствам кратной связи в алкенах.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 2819; Нарушение авторских прав?; Мы поможем в написании вашей работы!