
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Осаждение урана из карбонатных растворов
|
|
|
|
Аммиачное осаждение. Аммиак, как слабое основание, не может разрушить карбонатный комплекс урана. Поэтому сначала нужно удалить из раствора карбонат-ион. Это достигается подкислением раствора до рН = 3 - 5. При действии кислоты на карбонатный раствор происходят следующие процессы:
Na2CО3 + H2SО4 = Na2SО4 + H2О + CО2,
Na4[UО2(CО3)3] + 3 H2SО4 = 2 Na2SО4 + UО2SО4 + 3 H2О + 3 CО2,
2 NaAlО2 + 4 H2SО4 = Na2SО4 + Al2(SО4)3 + 4 H2О,
2 Na3[Fe(CО3)3] + 6 H2SО4 = 3 Na2SО4 + Fe2(SО4)3 + 6 H2О + 6 CО2.
 Сульфаты алюминия и железа частично гидролизуются. Если в растворе имеются фосфор и ванадий, то часть урана может при этом осадиться:
Сульфаты алюминия и железа частично гидролизуются. Если в растворе имеются фосфор и ванадий, то часть урана может при этом осадиться:
Na3PО4 + UО2SО4 = NaUО2PО4 + Na2SО4,
NaVО3 + UО2SО4 + H2О = NaUО2VО4 + H2SО4.
Для полного удаления выделяющейся углекислоты и растворенной углекислоты раствор нагревают почти до кипения и продувают через него воздух в течение 2 ч. После этого в раствор добавляют аммиак до рН = 6,5 - 7,0. Проходят те же реакции, что при аммиачном осаждении из кислых растворов; осадок отфильтровывают. В нем содержится 40—60 % урана (на сухую массу).
Можно осуществить и безаммиачное осаждение урана. В этом случае нейтрализацию карбонатного раствора кислотой проводят только до рН = 5 - 6. Поскольку концентрация кислоты малая, то процесс разрушения карбонатного комплекса идет медленнее. После разрушения комплекса и удаления углекислоты при длительном кипячении раствора происходит гидролиз:
UО2SО4 + 2 Н2О = UО2(OH)2 + H2SО4,
Fe2SО4 + 6 H2О = 2 Fe(OH)3 + 3 H2SО4 и т. д.
Как видно, данный способ требует большого расхода кислоты на разрушение избытка соды и много времени на удаление углекислоты.
Осаждение урана едким натром. Применение едкого натра позволяет осадить уран из карбонатного раствора без предварительного разрушения карбонатного комплекса и избытка соды. В сильнощелочной среде при рН > 12 едкий натр разрушает комплекс, осаждает уран:
|
|
|
2 Na4[UО2(CО3)3] + 8 NaOH = 2 Na2UO4 + 6 Nа2СO3 + 4 Н2O
и ряд примесей, например:
Na3[Fe(CO3)3] + 3 NaOH = Fe(OH)3 + 3 Na2CO3.
Могут осаждаться и другие гидроксиды (Са, Mg). В растворе остаются фосфор и ванадий в виде ортофосфата натрия и метаванадата натрия. В сильнощелочной среде алюминий будет находиться в растворе в виде алюмината натрия (NaA1O2). В растворе останется и молибден:
Na4[MoO2(CO3)3] + 4 NaOH = Na2MoO4 + З Na2СО3 + 2 Н2O.
На этой стадии молибден отделяется от урана. При подкислении маточника до рН = 2,5 - З осаждается молибденовая кислота. При щелочном разрушении карбонатного комплекса регенерируется сода. После фильтрации раствор, содержащий Na2CO3 и избыточный NaOH (5 - 10 г/л), насыщается углекислотой:
СO2 + 2 NaOH = Na2CO3 + H2O,
Na2CO3 + Н2O + CO2 = 2 NaHCO3.
После этого данный раствор может быть направлен на карбонатное выщелачивание. Регенерация соды снижает общие расходы на получение урана.
Осаждение диураната натрия проводят при повышенных температурах для ускорения созревания осадка в целях получения хорошо фильтруемого осадка. Некоторое увеличение растворимости диураната натрия не играет роли, если маточный раствор возвращается на выщелачивание. Концентрация урана в фильтрате резко увеличивается при большом содержании избыточной соды и ванадата натрия. При концентрациях ванадия 2 - 3 г/л щелочное осаждение становится неэффективным.
Выделение урана и ванадия из карбонатных растворов. Карбонатный раствор урана и ванадия нейтрализуется серной кислотой до рН 6. При этом карбонатный комплекс разрушается и уран осаждается в виде натрийуранилванадата («желтый кек»):
Na4[UO2(CO3)3] + NaVO3 + 2 H2SO4 + n H2O =
= NaUO2VO4 × nH2O + 2 Na2SO4 + 3 CO2 + 2 H2O.
Отфильтрованный «желтый кек» сплавляют с содой, поваренной солью и древесными опилками при температуре 800-900 °С:
3 NaUO2VO4 + С + NaCI + Na2CO3 = U3O8 + 3 NaVO3 + CO + NaCI + Na2CO3.
Из сплава ванадат натрия выщелачивают водой, остаток представляет концентрат с содержанием урана 60 %. Ванадий выделяют в виде «красного кека» (V2O5 × nН20) из нагретых растворов путем подкисления до рН 2,5:
|
|
|
.
Процесс организуется по технологической схеме, приведенной на рисунке.

Технологическая схема выделения и разделения урана и ванадия из карбонатных растворов.
Восстановление урана водородом. Растворимый карбонатный комплекс образует только шестивалентный уран. Поэтому если в карбонатной среде восстановить уран до четырехвалентного состояния, то он будет осаждаться в виде гидратированного диоксида. Принципиально можно использовать многие восстановители: дитионит натрия (Na2S2O4), цинковую пыль и др., можно использовать водород, который в атомной промышленности получается попутно при получении элементного фтора при электролизе KF × 2HF. Восстановление проводится на поверхности катализатора - никелевого порошка, одновременно восстанавливается и ванадий:
Na4[UO2(CO3)3] + Н2 + n Н2O = UO2 nH2O + Na2CO3 + 2 NaHCО3,
2 NaVО3 + 2 NaHCО3 + 2 H2 = V2О3 + 2 Na2CО3 + 3 H2О.
Скорость восстановления описывается следующим кинетическим уравнением:
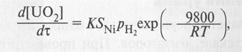
где SNi – поверхность никелевого катализатора; pH2 - парциальное давление водорода, атм; 9800 ккал/моль – энергия активации Е
Процесс протекает при температуре 100 - 150 °С и парциальном давлении водорода (3,5 - 14) × 10 Па, концентрация никелевого катализатора 3 - 10 г/л. Раствор после фильтрации может быть направлен на карбонатное выщелачивание (в нем концентрация урана 2 - 3 мг/л). От осадка никелевый порошок отделяется с помощью ЭМС. После этого смесь оксидов урана и ванадия сплавляют с содой, при этом ванадий окисляется и переходит в водорастворимое состояние:
V2O3 + Na2CO3 + O2 = 2 NaVO3 + CO2.
Из плава ванадат натрия выщелачивается водой. Уран остается в виде черного кека, он содержит 85—90 % закиси-окиси урана.
На процесс восстановления урана водородом каталитическое действие оказывает свежеосажденный диоксид урана. Каталитические свойства теряются при подсушке диоксида урана. Скорость восстановления водорода пропорциональна парциальному давлению водорода и количеству диоксида. Казалось бы, все хорошо, сам продукт реакции катализирует процесс восстановления урана. Но приемлемая скорость восстановления достигается при концентрации диоксида урана 20 - 40 г/л, что в десятки раз больше, чем концентрация урана в карбонатном растворе (0,5 - 1,0 г/л).
приемлемая скорость восстановления достигается при концентрации диоксида урана 20 - 40 г/л, что в десятки раз больше, чем концентрация урана в карбонатном растворе (0,5 - 1,0 г/л).
|
|
|
Восстановление урана в карбонатном растворе можно осуществить и электролитически. При пропускании карбонатного раствора через ряд последовательно расположенных электролитических ванн уран и ванадий будут осаждаться на катодах. После окончания цикла поглощения ванны ставят на регенерацию, заполняют растворами карбоната аммония и меняют на них полюса, на анодах происходит окисление и растворение урана и ванадия, начинается карбонатный аффинаж урана.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2084; Нарушение авторских прав?; Мы поможем в написании вашей работы!