
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Способы получения
|
|
|
|
Любые соединения урана, металл и его сплавы фторируются фтором до UF6. Однако использование фтора, как вещества дорогого, должно быть рациональным, т.е. следует стремиться к расходованию минимального количества F2.
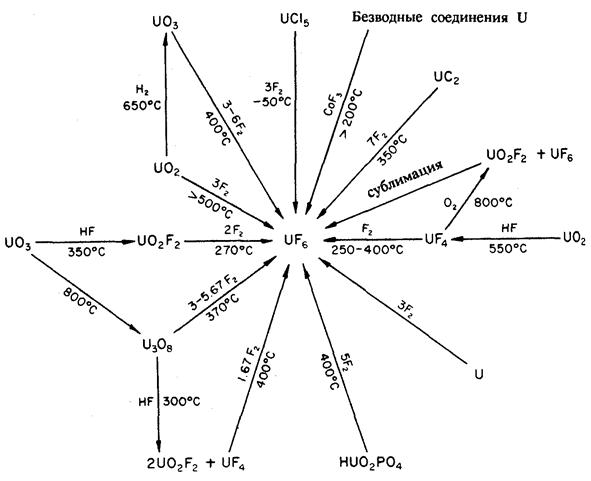
Реакции, приводящие к образованию гексафторида урана
Способ 1. Фторирование тетрафторида урана, является основным технологическим методом получения гексафторида урана. Реакция, лежащая в основе метода, достаточно проста:
UF4 + F2 → UF6 T > 350 oC
При низких температурах реакция идёт стадийно:
4 UF4 + ½ F2 → U4F17 T < 200 oC
U4F17 + ½ F2 → 2 U2F9 T < 200 oC
2 U2F9 + F2 → 4 UF5 T < 200 oC
4 UF5 + 2 F2 → 4 UF6 T > 350 oC
∑: 4 UF4 + 4 F2 → 4 UF6
Способ 2. Фторирование с использованием фторидов галогенов, ClF3 или BrF3, например:
3 UF4 + 2 ClF3 → 3 UF6 + Cl2 T = 250 oC
Способ 3. Фторирование с переносчиками фтора. В качестве переносчиков фтора могут выступать фториды трёхвалентных кобальта или марганца:
Co(III) + e- ↔ Co(II)
Mn(III) + e- ↔ Mn(II)
UF4 + 2 CoF3 → UF6 + 2 CoF2 T = 250-275 oC
CoF2 + ½ F2 → CoF3 T < 250 oC
Достоинствами этого способа являются низкие рабочие температуры и отсутствие газов-разбавителей.
Способ 4. Фторирование без использования фтора. В основе метода лежит окисление тетрафторида урана кислородом. При этом половина урана переходит в гексафторид:
2 UF4 + O2 → UF6 + UO2F2 T = 700-800 oC
Уранил фторид направляют на восстановление до терафторида:
UO2F2 + H2 + 2 HF → UF4 + 2 H2O T > 550 oC
который снова, с добавкой новой его порции, возвращается на окисление.
Очистка F2 и UF6 от HF проводится с использованием сорбентов, NaF или KF:
NaF + HF → NaF·HF (т.е. NaHF2)
Учитывая, что у фтористого водорода HF tпл. = -83оС, а tкип. = 19,5 оС, возможна и возгонка UF6 с последующей его избирательной конденсацией. Но при этом, конечно, какая-то часть UF6 захватывается в HF (РUF6 даже при отрицательных температурах относительно высока). В качестве метода очистки может быть использована и кристаллизация UF6 в среде жидкого HF при t = -(40÷60) оС.
|
|
|
На практике очистка гексафторида урана осуществляется следующим образом. В результате фторирования тетрафторида образуется газовая смесь, содержащая UF6, F2, HF, N2 и др., плюс взвешенные частицы непрореагировавшего UF4. Эта смесь направляется в пылеулавливатели (пылеотбойники, циклоны, пористые металлические фильтры). Материал аппаратов – никель либо сплавы на его основе (монель, инконель). Далее следует конденсация (листовой конденсатор – труба с пластинами внутри и трубами хладагента). Конденсаторов два – головной, работающий при температуре -40 оС, и хвостовой, работающий при -60 оС; основная масса UF6 конденсируется в первом. По мере заполнения конденсатора система переключается на параллельный аппарат, а полный выводится из системы охлаждения и при закрытых вентилях нагревается до температуры 90-100 оС и давления 3-4 атм. Жидкий гексафторид урана затем разливается в контейнеры.
Фтор получают электролизом расплавов кислых фторидов калия. Чем выше содержание фтора в кислом фториде, тем ниже рабочая температура процесса:
KHF2 (высокотемпературный режим 250-270 oC);
KH2F3 (среднетемпературный режим 100-110 oC);
KH3F4 (низкотемпературный режим 80-85 oC).
На катоде и аноде протекают следующие реакции:
катод: 2 H+ + 2 e- → H2
анод: 2 F- - 2 e- → F2
Расход электроэнергии при получении фтора очень высокий – 17-18 кВт·час / кг F2.
Общая технологическая схема получения гексафторида урана представлена на рисунке.
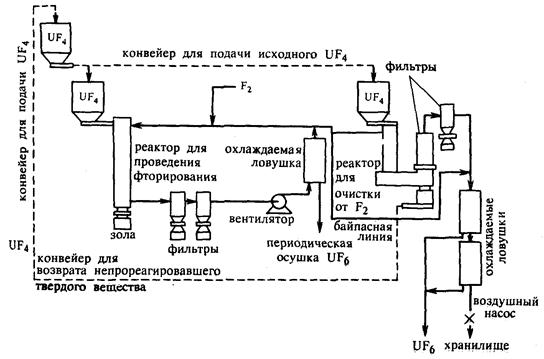
Технологическая схема производства гексафторида урана.
Разделение изотопов урана
Возможность разделения газов при течении через пористую среду была экспериментально открыта Грахомом (Грэмом) в середине 19-го века. Максвелл показал, что эффект разделения обусловлен тем обстоятельством, что относительная частота, с которой молекулы различных компонентов попадают в малые отверстия, обратно пропорциональна квадратному корню отношения их молекулярных весов.
|
|
|
Работы над разделением изотопов элементов были начаты в начале 20 века. Астон первый применил газовую диффузию для разделения изотопов. В 1920 г. он осуществил частичное разделение изотопов неона в одной газодиффузионной ступени с помощью пористой глиняной трубы. Герц увеличил степень разделения, применив каскад из 24-50 ступеней. В подобном аппарате достигается практически полное разделение изотопов неона с массами 20 и 22, а также полное разделение водорода и дейтерия.
Трудность в разделении 235 и 238 изотопов урана заключается в небольшой относительной разнице между атомными массами этих изотопов – немногим более 1 %. Основные работы по разработке основ методов разделения изотопов урана были выполнены в начале 1940-х годов, в основном в ходе реализации «Манхэттенского проекта». Всего было предложено пять методов.
Отто Фриш, работая в Бирмингеме, предложил метод термодиффузии. Газообразное соединение урана вводится в вертикальную трубку с горячей проволокой вдоль оси. Молекулы, содержащие лёгкий изотоп, диффундируют к горячей центральной зоне и уносятся вверх конвекционными потоками. Молекулы с тяжёлым изотопом движутся к внешним (более холодным) стенкам и уносятся вниз.
Метод газовой диффузии, основанный на движении молекул через пористую мембрану, применительно к урану разрабатывал профессор Саймон, работая в Оксфордском университете.
Электромагнитный метод разделения был разработан Эрнестом Лоуренсом в Калифорнийском университете. Метод основан на действии электрического и магнитного полей на пучок заряженных ионов урана. При этом более лёгкие ионы отклоняются сильнее.
Центрифужный метод разделения был разработан Джесси Бимсом из университета Вирджинии.
И, наконец, американец Абелсон предложил метод жидкостной термодиффузии. Сжиженный гексафторид урана под давлением пропускается через двустенную трубу. Труба нагревается снаружи паром и охлаждается изнутри водой. Как и в методе газовой термодиффузии более лёгкий изотоп движется к горячей внешней стенке и поднимается кверху трубы.
|
|
|
Используя все эти методы в рамках «Манхэттенского проекта» к 24 июля 1945 г. было наработано 40 кг урана с обогащением 80% по 235-ому изотопу.
В настоящее время в промышленных масштабах используются два метода разделения изотопов урана – газовая диффузия (метод считается устаревшим) и центрифужное разделение.
Гексафторид урана является монопольным соединением для разделения изотопов урана. Это обусловлено комбинацией свойств этого соединения:
· UF6 легко переходит в газовую фазу (температура кипения 56,4 оС);
· в газовой фазе сохраняются молекулы UF6 – гексафторид урана является термически устойчивым соединением и не диссоциирует;
· фтор в природе представлен единственным изотопом, поэтому разница в массах молекул UF6 определяется только разницей в атомных массах изотопов урана.
Рассмотрим основы существующих методов обогащения урана.
Газовая диффузия явилась первым процессом, использованным в большом масштабе при разделении изотопов. Развит в 1940-50е годы. Принцип метода заключается в следующем: в газовой смеси, находящейся в температурном равновесии, кинетическая энергия всех молекул одинакова. Более лёгкие молекулы, поэтому, перемещаются более быстро, чем тяжёлые, и по этой причине будут соударяться со стенками контейнера более часто. Если стенка представляет собой мембрану с отверстиями, через которые могут проходить только индивидуальные молекулы, но не весь поток, то проходящий газ будет содержать более высокую концентрацию лёгких молекул. Размер пор в мембране составляет 100-300 Å.
Максимальный теоретически достижимый коэффициент разделения определяется массами лёгкой и тяжёлой молекул и равен квадратному корню из отношения этих масс. Для процесса диффузии с участием гексафторида урана максимальный коэффициент разделения α рассчитывается следующим образом. Кинетическая энергия отдельной молекулы, имеющей массу М и скорость V, определяется по уравнению
|
|
|
Е кин = ½ М V 2
Для смеси, состоящей из молекул с молекулярными массами М 1 и М 2 и скоростями V 1 и V 2, справедливо
½ М 1 V 12 = ½ М 2 V 22
Отсюда максимальный коэффициент разделения α* равен
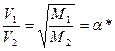
Для молекул газообразного UF6
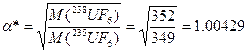
Поскольку эта величина близка к единице, то степень обогащения, достигаемая в одной стадии диффузии, оказывается весьма небольшой, однако разделение может быть многократно повторено. Для производства 235U с обогащением 90% (масс.) из материала с содержанием 235U 0,711% (масс), как это имеет место в природных рудах, необходимо провести 3000 последовательных ступеней газодиффузионного разделения.
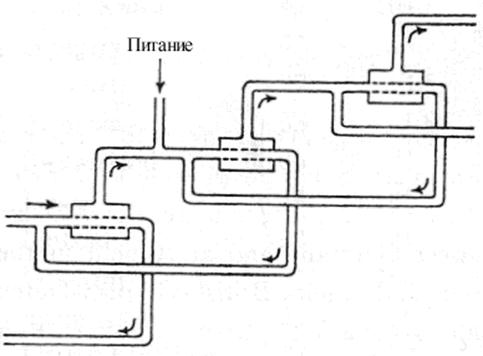
Разделение изотопов методом газовой диффузии. Штриховые линии представляют пористые перегородки. Более лёгкая фракция, которая проходит через перегородку быстрее, уходит направо. Более тяжёлая фракция возвращается налево на повторную переработку. Для поддержания циркуляции используются насосы.
Диффузионная камера имеет примерно 3,5 м в диаметре и 6 м длиной. Перекачка газа и обеспечение необходимого давления через мембрану осуществляется с помощью компрессоров, каждый весом около 16 тонн и приводимый в движение электродвигателем мощностью 1600 кВт.
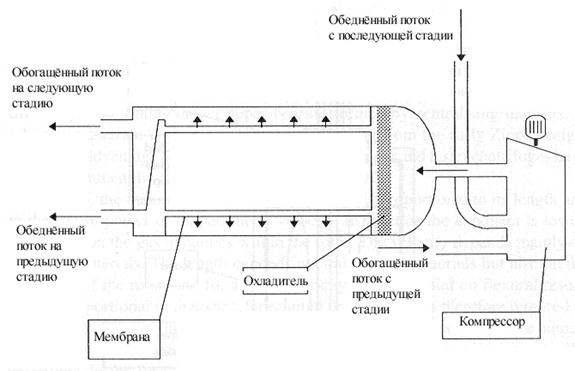
Схема разделительной стадии в методе газовой диффузии.
Последний завод такого типа вступил в действие в Трискастине (Франция) в начале 1980-х. Недостатком метода является очень высокое энергопотребление, к примеру один завод в США потребляет 1 800 000 кВт электроэнергии.
Разделение изотопов в центрифугах основано на том, что во вращающемся роторе изотопы разделяются, при этом тяжёлые отбрасываются к периферии, а лёгкие – к центру. Эффективность разделения зависит от скорости на периферии.
В равновесных условиях при данной температуре молекулы идеального газа в центробежном поле распределяются в зависимости от массы. В случае присутствия двух изотопов достигается коэффициент разделения

где Δ M – разность масс изотопов, R – газовая постоянная, Т – абсолютная температура, V = ωr – линейная скорость, L – активная скорость ротора центрифуги, r – радиус ротора центрифуги, ω – угловая скорость ротора.
Ранние разработки тормозились из-за проблем организации вращения (выбор подшипников). В 1960-е была разработана схема, в которой заострённый ротор опирается на углубление, заполненное маслом, а в верхней части установлен бесконтактный подшипник с централизующими магнитами. Начиная с 1960-х технологию засекретили. Потребление энергии таким заводом составляет менее 5% от газодиффузионного.
Схематически конструкции центрифуг представлены ниже.
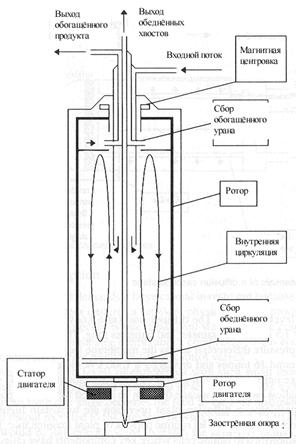
Схематическая конструкция центрифуги для разделения изотопов.
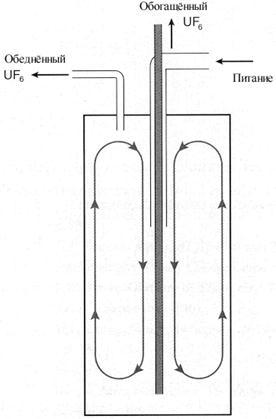
Разделение изотопов в центрифуге.
Все современные установки для разделения изотопов (в том числе и урана) обладают рядом общих свойств:
· Наличие огромного числа идентичных элементов оборудования. Это является следствием низкой разделительной мощности отдельных агрегатов.
· Длительность пускового периода, т.е. времени от загрузки сырья до установления стационарного рабочего режима с выдачей продукции (50-100 дней). Это является следствием низкой производительности и сравнительно большого объёма отдельных агрегатов. Полное накопление изотопа в установке соответствует её производительности за несколько месяцев работы.
· Очень большие энергетические затраты.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1235; Нарушение авторских прав?; Мы поможем в написании вашей работы!