
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электростатическая теория связи
|
|
|
|
ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ
Относительно природы химической связи в комплексных соединениях существует несколько современных теорий, которые не содержат противоположных утверждений, однако дополняют друг друга. Все они, как правило, приводят к идентичным результатам.
1 Электростатическая модель Косселя и Магнуса рассматривает химическую связь в комплексных соединениях, основываясь на законе Кулона. При этом допускается, что все частицы в комплексном ионе представляют собой недеформированные шарики с определенными зарядами и радиусами. Устойчивый комплекс образуется, если силы притяжения лигандов к комплексообразователю уравновешивают силы отталкивания между лигандами. При увеличении количества лигандов силы отталкивания между ними начинают преобладать, и комплекс теряет свою стойкость.
Эта теория позволила объяснить стойкость комплексов, координационные числа комплексообразователей и пространственное размещение лигандов. На основе кулоновского взаимодействия заряженных частиц с учетом принципа наименьшей энергии системы удалось рассчитать оптимальные значения координационных чисел: они равны 1 или 2, когда степень окисления центрального атома составляет +1, 2 или 4, если степень окисления +2 и 4, 5 или 6 при степени окисления +3. Кроме того, электростатическая теория доказала, что пространственное строение комплекса зависит от величины координационного числа.
Согласно закону Кулона прочность комплекса возрастает с увеличением заряда комплексообразователя и уменьшением радиусов лигандов. Например, для галогенидных комплексов алюминия (+3) стойкость уменьшается в направлении от [AlCl4–] до [AlI4–], поскольку в этом ряду закономерно увеличивается радиус лигандов.
|
|
|
Установлено, что стойкость комплексов с одинаковыми лигандами тем больше, чем выше степень окисления комплексообразователя, как видно из сравнения констант нестойкости аммиакатов меди(+1) и меди(+2), а также цианидных комплексов железа(+2) и железа(+3):
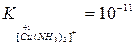 и
и 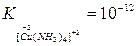 ,
,
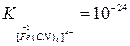 и
и 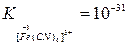 .
.
Электростатическая модель обосновала значения координационных чисел в зависимости от природы лигандов. Поскольку силы отталкивания между одноименно заряженными ионами больше, чем между нейтральными лигандами, координационное число в комплексе с нейтральными лигандами всегда выше, чем в комплексе с анионными лигандами, например:
[Co(CNS) 4 –]2–, однако [Co(H2O) 6 0]2+.
Несмотря на простоту и наглядность, электростатическая теория имеет определенные недостатки и не может объяснить некоторые факты: существование комплексов с комплексообразователем в нулевой степени окисления и нейтральными лигандами, например:
o o
[Fe(CO)5]0], [Ca(NH3)60] и др., более высокую стойкость комплексов 4d- и 5d-металлов по сравнению с комплексами 3d-металлов, магнитные и оптические свойства комплексных соединений и т.п.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1229; Нарушение авторских прав?; Мы поможем в написании вашей работы!