
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Равновесие адсорбции
Теоретические основы адсорбции
Поглотительная (адсорбционная способность) – величина адсорбции, активность, ёмкость – концентрация адсорбата в единице объёма или массы адсорбента.
Адсорбция – экзотермический процесс.
Зависимость величины адсорбции от равновесной концентрации (давления) поглощаемого вещества в газовой фазе в условиях равновесия при определённой температуре называется изотермой адсорбции:
а*=f(p) или a*=f(p/ps)
Возможные формы изотерм адсорбции представлены на рисунке 19.
 При высоких температурах и малых парциальных давлениях рi уравнение изотермы адсорбции принимает вид закона Генри:
При высоких температурах и малых парциальных давлениях рi уравнение изотермы адсорбции принимает вид закона Генри:
а*=mр, где m – коэффициент фазового равновесия, а изотерма имеет форму кривой 3 (см.рис.19).
При практических расчётах используется эмперическое уравнение Фрейдлиха:
а*=Крn, где К, n – константы для данной температуры. Изотерма в этом случае имеет вид экспоненты.
Для широкого интервала давлений в случае мономолекулярной адсорбции (без капиллярной конденсации) изотерма адсорбции описывается уравнением Ленгмюра:
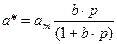 , где
, где
аm – предельная величина адсорбции (ёмкость монослоя) при р/рs=1, рs - давление насыщенного пара при даной температуре;
b – коэффциент, зависящий от температуры.
Изотерма Ленгмюра имеет вид кривых 1,2 на рис.19.
С помощью данных, получаемых из изотермы Ленгмюра (am), можно рассчитать удельную поверхность сорбента:
S = am∙NA∙ωm, где
S – удельная поверхность адсорбента;
NA = 6,022∙10231/моль – число Авагадро;
ωm – элементарная площадка, занимаемая молекулой адсорбата в плотном слое на поверхности адсорбента (справочные данные).
Для описания полимолекулярной адсорбции без капиллярной конденсации используется уравнение изотермы БЭТ (Брунауэра, Эммета, Теллера):
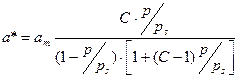 ,
,
С – константа, определяющая вид изотермы и определяется по формуле:
 , где
, где
Q1 – теплота адсорбции в 1-ом слое;
λ – теплота конденсации пара адсорбтива.
При Q1> λ изотерма имеет вид кривой 5 на рис.19,
При Q1< λ изотерма имеет вид кривой 4 (s-форма) на рис.19
Дальнейшее развитие теория адсорбции получила в работах школы академика М.М.Дубинина, создавшего потенциальную теорию адсорбции, основанную на термодинамических закономерностях, обосновавших теорию объемного заполнения микропор. Основное уравнение потенциальной теории:
 , где
, где
W0 – предельный объём адсорбционного пространства;
V* - молекулярный объём адсорбата в ожиженном состоянии при температуре Т;
А – мольная работа адсорбции,
А = -∆G = RT ln(ps/р);
Е – характеристическая энергия адсорбции;
n – константа, принимающая значения от1 до 6.
|
Дата добавления: 2014-01-07; Просмотров: 363; Нарушение авторских прав?; Мы поможем в написании вашей работы!