
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Спектр атома водорода
|
|
|
|
Вывод
Спектральные закономерности
Доказательства сложной структуры атома
Атомная физика
Лекция 11
Уравнение Эйнштейна для фотоэффекта
Законы Столетова для фотоэффекта
1 Максимальная кинетическая энергия фотоэлектронов линейно возрастает с увеличением
частоты света и не зависит от его интенсивности
2 Сила фототока насыщения пропорциональна интенсивности света
3. Для каждого вещества существует красная граница фотоэффекта, то есть наименьшая частота νmin, при которой возможен фотоэффект
Объяснение фотоэффекта проведено на основе квантовой гипотезы Планка
hν = А + Ек(max)
Энергия падающего фотона расходуется на преодоление работы выхода и сообщение электронам кинетической энергии
Работа выхода электронов из металла равна минимальной энергии, которой должен обладать электрон для освобождения с поверхности вещества.
Фотоэффект невозможен, если энергии падающего фотона недостаточно для преодоления работы выхода, hν < А
Частота и длина волны красной границы фотоэффекта:
ν =А/h
λ=hc/A
Открытие электрона
Открытие периодического закона Менделеева
Закономерности линейчатых спектров
Радиоактивность
Интерференция, дифракция и дисперсия света сопровождаются спектральным разложением немонохроматической волны.
Сплошной спектр (непрерывный) содержит все длины волн. В спектре нет разрывов, и на экране можно видеть сплошную разноцветную полосу с плавным переходом от одного участка спектра к другому.
Сплошные спектры дают нагретые тела в твердом или жидком состоянии, а также сильно сжатые газы.
Линейчатый спектр излучения состоит из набора цветных линий различной яркости, разделенных широкими темными полосами. Каждой линии соответствует определенная частота ЭМВ.
|
|
|
Линейчатые спектры излучают все вещества в газообразном атомарном состоянии
Линейчатые спектры химических элементов специфичны, то есть каждому элементу соответствует свой набор спектральных линий.
При пропускании белого света через пары вещества наблюдаются темные линии на фоне сплошного спектра излучения источника. Эти линии образуют спектр поглощения данного вещества
Линии спектра поглощения располагаются точно в тех местах, где наблюдались бы линии спектра излучения данного вещества.
Газ поглощает наиболее интенсивно свет именно тех частот, которые он сам
испускает в нагретом состоянии
Видимый участок спектра атома водорода содержит четыре линии. Их частоты
описываются формулой Ридберга
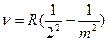
R = 3.29 x 1015 Гц
m =3,4,5…
Совокупность спектральных линий атома водорода в видимой части спектра была названа серией Бальмера.
Позже аналогичные серии спектральных линий были обнаружены в ультрафиолетовой и инфракрасной частях спектра. В 1890 году И. Ридберг получил эмпирическую обобщенную формулу для частот спектральных линий:
 , где m>n
, где m>n
n=1 серия Лаймана, УФ
n= 2 серия Бальмера, видимый свет
n =3 серия Пашена, ИК
Теория строения атома должна объяснить происхождение и закономерности линейчатых спектров, а также экспериментальную формулу Ридберга для спектра атома водорода.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 526; Нарушение авторских прав?; Мы поможем в написании вашей работы!