
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Способы получения. Моно- и полигалогенопроизводные предельных углеводородов (кроме полифторпроизводных)
|
|
|
|
Номенклатура
Изомерия
Моно- и полигалогенопроизводные предельных углеводородов (кроме полифторпроизводных)
ГАЛОГЕНПРОИЗВОДНЫЕ АЛИФАТИЧЕСКИХ УГЛЕВОДОРОДОВ (алкил- и алкенилгалогениды и др.)
ЛЕКЦИЯ 6
Это производные углеводородов, у которых один или несколько атомов водорода замещены на атом галогена. Они имеют огромное значение в науке и технике, т.к. они гораздо активнее углеводородов, с их помощью легко осуществляются переходы к другим классам органических соединений.
Классификация
1. По строению углеродной цепи (предельные и непредельные);
2. По количеству атомов галогена (моно- и полигалогенопроизводные);
3. По положению галогена (первичные, вторичные, третичные);
4. По природе галогена (фтор-, хлор-, бром- и йодпроизводные).
Моногалогенпроизводные
СН3Cl хлористый метил
СН3I йодистый метил
С2Н5Br бромистый этил
(СН3)3СI йодистый третбутил и т.д.
Полигалогенопроизводные
СН2Cl2 хлористый метилен
CHCl3 хлороформ (хлористый метин)
CCl4 четыреххлористый углерод
CH3-CHCl2 хлористый этилиден
CH2Cl-CH2Cl хлористый этилен и т.д.
На примере монохлорпроизводных бутана
СН3-СН2-СН2-СН2-Cl хлористый бутил (1)
СН3-СН-СН2-СН3 хлористый вторбутил (2)
Cl
СН3-СН-СН2-Cl хлористый изобутил (3)
СН3
СН3
СН3-С-Cl хлористый третбутил (4)
СН3
(1,3) - изомерия цепи
(1,2), (3,4) – изомерия положения
Названия перечисленных моно- и полигалогенопроизводных составлены по радикально-функциональной номенклатуре (IUPAC), согласно которой к названию радикала добавляется название функции. Исключение представляют тригалогензамещенные метана (хлороформ). Более сложные соединения следует называть, пользуясь заместительной номенклатурой (IUPAC). Согласно ее правилам соединение называется как производное соответствующего углеводорода, пронумерованного со стороны галогена, который в названии обозначается приставкой (непредельные нумеруют со стороны двойной связи).
|
|
|
1 2 3 4 5
СН3- СН- СН2- СН- СН3 2-бром-4-метилпентан
Br СН3
1. Действие галогенов на углеводороды (см. свойства углеводородов). Применяется, в основном, для получения полигалогенопроизводных.
2. Присоединение Нhal к непредельным углеводородам (см. свойства непредельных УВ).
3. Замещение группы ОН в спиртах на Hal (препаративный метод получения моногалогеналкилов):
а) взаимодействие с галогенводородными кислотами
СН3ОН + HCl  Н2О + СН3Cl
Н2О + СН3Cl
б) взаимодействие спиртов с галоидными соединениями фосфора
Cl Cl Cl Cl
С2Н5ОН + PCl5  C2Н5Сl + P -Сl
C2Н5Сl + P -Сl  P + HCl
P + HCl
Cl Cl O Cl
3(CН3)3СОН + PBr3  3(CH3)3CBr + P(OH)3
3(CH3)3CBr + P(OH)3
третбутиловый
спирт
Надо иметь в виду, что первичные спирты взаимодействуют с PCl3 с образованием сложных эфиров фосфористой кислоты, например,
Cl HOCH3 OCH3
P-Cl + HOCH3  3HCl + P-OCH3
3HCl + P-OCH3
Cl HOCH3 OCH3
Третметилфосфит
в) взаимодействие с хлористым тионилом:
Cl HO
2СН3ОН + S=O  2CH3Cl + S=O
2CH3Cl + S=O  SO2 + H2O
SO2 + H2O
Cl HO
хлорангидрид сернистая
сернистой кислота
кислоты
4. Замещение на галоген кислорода в альдегидах и кетонах
Cl
СН3-С-СН3 + PCl5  CН3-С-СН3 + POCl3
CН3-С-СН3 + POCl3
O Cl
2,2-дихлорпропан
5. Из серебряных солей карбоновых кислот под действием галогена
O
СН3-СН2-С + Br2  CН3-СН2-Br + CО2 + AgBr
CН3-СН2-Br + CО2 + AgBr
OАg
6. Получение тригалогензамещенных метана из альдегидов или кетонов, имеющих в 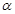 -положении метильную группу:
-положении метильную группу:
СН3-СН- СН3-С-
ОН О
Действие галогена в присутствии щелочи приводит к максимальному галоидированию в 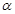 -положение.
-положение.
а) СН3-С-Н + 3I2 + 3 КОН  3KI + 3H2O + CI3-C-H
3KI + 3H2O + CI3-C-H 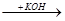
О О
CHI3 + KO-C-H
желтый О
осадок
7. Действие галоидных солей на галоидные алкилы (реакция Финкельштейна)
Применяется для получения труднодоступных йодистых и фтористых алкилов. Фтор слишком активен, а йод недостаточно активен для прямого галоидирования.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1053; Нарушение авторских прав?; Мы поможем в написании вашей работы!