
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Мал. 17
|
|
|
|
результаті кристалізації виходить сплав, що складається з однотипних кристалів твердого розчину.
На кривих охолодження температури кристалізації сплавів лежать між температурами кристалізації вихідних компонентів. У процесі кристалізації твердого розчину змінюється склад як рідкої, так і твердої фаз. Наприклад, у сплаві 1 центри кристалізації, які виникли при кристалізації, будуть відповідати точці 0 при зниженні температури, наступні шари зерна будуть мати вже концентрацію, що відповідає точці 0 і т.д.. Мал. 18 Тільки наприкінці кристалізації (точка В') складу кристалів твердого розчину буде відповідати концентрація сплаву 1.
При швидкому охолодженні неоднорідність по об’єму зерна, що виникла в процесі кристалізації, може зберегтися і зветься дендритною ліквацією. Зміна хімічного складу поблизу границь зерен внаслідок дендритної ліквації може привести до міжкристалічної корозії в хромонікелевих сталей.
Дендритна ліквація може бути усунута шляхом тривалої витримки сплавів при високих температурах. Нижче лінії солідус AbB (AqB- ліквідус) усі сплави системи складаються з кристалів твердого розчину різної концентрації. Необмежена розчинність у твердому стані зустрічається порівняно рідко. Значно частіше утворяться сплави з обмеженою розчинністю у твердому стані. Діаграма стану 3
типу для випадку обмеженої розчинності у твердому стані зображена на малюнку 18.
При кристалізації компонент В розміщується в гратках компонента А в атомарному вигляді з утворенням твердого розчину a з максимальною концентрацією, що відповідає точці Е при температурі tl. У тому випадку, якщо компонент А в гратках компонента В розміститися не може, область твердого розчину з боку компонента В відсутня. За межею насичення (точка С), коли з'являється друга фаза (компонент В) і утвориться евтектика, лінія солідус стає горизонтальною (ЕД). Таким чином, діаграма стану з обмеженою розчинністю сполучить у собі два попередні типи діаграм.
|
|
|
 Оскільки межа насичення змінюється зі зміною температури, концентрація a-твердого розчину при кімнатній температурі буде менша, ніж у точці Е. Усі сплави з концентрацією компонента В меншою, ніж у точці Е', при кристалізації утворять насичені a-тверді розчини і при охолодженні нижче лінії солідус не мають структурних перетворень. Сплави, що знаходяться по концентрації між точками Е и Е' при охолодженні мають структурні перетворення, що полягають в утворенні у зернах чи по границях a-твердого розчину вторинних кристалів елемента В. Ці кристали з'являються при охолодженні сплаву до лінії ЕЕ' (нижче її), коли a- кристали стають перенасиченими компонентом В для даної температури. При концентраціях елемента В, більших ніж межа насичення (точка Е), утворяться сплави з надлишковим вмістом кристалів чистого компонента В (заевтектичні). Сплав, що відповідає по концентрації точці С, має евтектичну будову.
Оскільки межа насичення змінюється зі зміною температури, концентрація a-твердого розчину при кімнатній температурі буде менша, ніж у точці Е. Усі сплави з концентрацією компонента В меншою, ніж у точці Е', при кристалізації утворять насичені a-тверді розчини і при охолодженні нижче лінії солідус не мають структурних перетворень. Сплави, що знаходяться по концентрації між точками Е и Е' при охолодженні мають структурні перетворення, що полягають в утворенні у зернах чи по границях a-твердого розчину вторинних кристалів елемента В. Ці кристали з'являються при охолодженні сплаву до лінії ЕЕ' (нижче її), коли a- кристали стають перенасиченими компонентом В для даної температури. При концентраціях елемента В, більших ніж межа насичення (точка Е), утворяться сплави з надлишковим вмістом кристалів чистого компонента В (заевтектичні). Сплав, що відповідає по концентрації точці С, має евтектичну будову.
Діаграма стану 4 типу для випадку утворення хімічної сполуки. Виникає хімічна сполука, якщо вона стійка і не розкладається аж до температури плавлення, поводиться в процесі кристалізації так як і чистий компонент. Вид діаграми стану буде залежати від того. як утворена хімічна сполука взаємодіє з вихідними компонентами в процесі кристалізації.
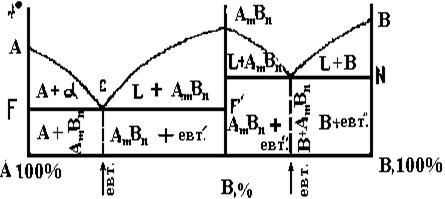 На мал.20 представлена діаграма для випадку роздільної кристалізації хімічних сполук і вихідних компонентів.
На мал.20 представлена діаграма для випадку роздільної кристалізації хімічних сполук і вихідних компонентів.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 298; Нарушение авторских прав?; Мы поможем в написании вашей работы!