
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Рівномірну чи загальну
|
|
|
|
Мал.40
Потенціал в, в +1,42 +0,8 +0,34 0 -0,23 -0,44 -0,76 -1,66 -2,38
Електродний
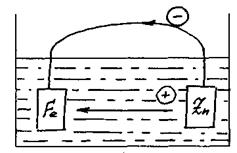 Метали, що мають позитивний електрохімічний потенціал не кородують, а з негативним потенціалом піддаються корозії. Тому для запобігання корозії необхідно, щоб весь сплав чи його поверхневий шар мали позитивний електрохімічний потенціал. При з'єднанні двох металів у пари в електроліті буде кородувати той, котрий заряджається більш электровід’ємно.
Метали, що мають позитивний електрохімічний потенціал не кородують, а з негативним потенціалом піддаються корозії. Тому для запобігання корозії необхідно, щоб весь сплав чи його поверхневий шар мали позитивний електрохімічний потенціал. При з'єднанні двох металів у пари в електроліті буде кородувати той, котрий заряджається більш электровід’ємно.
Наприклад при зануренні Fе і Zn в електроліт обидва метали починають розчинятися заряджаючи при цьому электровід’ємно Zn. Так як Zn заряджається більш электро-від’ємно, то при з’єднанні в пари електрони по зовнішньому ланцюзі підуть від Zn до Fе, а іони в зв'язку з цим одержать спрямований рух від Zn до Fе. Значить у цій парі кородувати (розчинятися) першим буде більш електронегативний Zn.
Метал, що має більше значення електрохімічного потенціалу, не буде кородувати доти, доки цілком не розчиниться метал з меншим (більш електронегативний) значенням електрохімічного потенціалу. У сплаві, що складається з зерен різних фаз, кожна пара зерен утворить гальванічний мікроелемент, а реальний сплав можна розглядати як багато-електродний гальванічний мікроелемент.
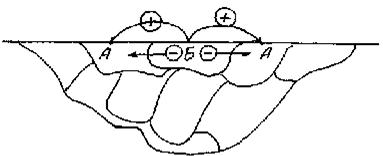 |
Мал.41
Якщо електрохімічний потенціал фази А більше електрохімічного потенціалу фази Б, то електричний струм потече від зерен фази Б к зернам фази А через метал, а позитивно заряджені іони - від фази Б через електроліт до фази А. У результаті в такому сплаві зерна однієї фази (Б) будуть розчинятися, а іншої (А) залишатися незмінними, з чого можна зробити висновок про необхідність одержання однорідної однофазної структури сплавів для забезпечення найбільш високих антикорозійних властивостей.
|
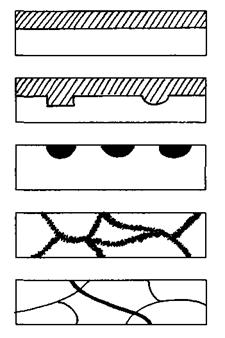
Розрізняють наступні види електрохімічної корозії:
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 270; Нарушение авторских прав?; Мы поможем в написании вашей работы!