
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Законы Гей-Люссака 1802 г
|
|
|
|
Идеальным газом называется такой, молекулы которого ничтожно малы (материальные точки), упруги и не связаны межмолекулярными силами.
Газовые законы для идеального газа
Закон Бойля - Мариотта 1662 – 1667 гг.
Для данной массы газа при постоянной температуре t = const давление газа изменяется обратно пропорционально объему. PV = сonst.
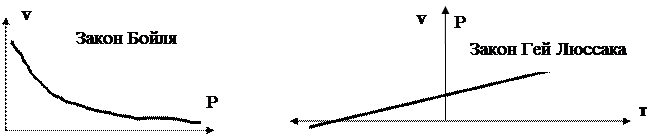
Рис. 18 Графики давления и объема газа для закона Бойля-Мариотта (слева) и Гей Люссака
Зависимость между объемом –V и давлением - Р в законе Бойля =Мариотта. Справа зависимость объема –V и давления -Р от температуры -Т
Для данной массы газа при постоянном давлении (P = const) объем увеличивается пропорционально росту температуры. То же самое при постоянном объеме давление увеличивается с ростом температуры.
V=V0 (1 + αT) P = P0 (1 + αT) Оказалось, что α =1/273,16 К = 1/ 277 К-1, где
Т – температура по шкале Кельвина Т = tc - 273.16, где tc – температура по шкале Цельсия.
Из закона Гей - Люссака следует V/V0 = T/T0 = P/P0
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 381; Нарушение авторских прав?; Мы поможем в написании вашей работы!