
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Равновесие при абсорбции. Закон Генри
|
|
|
|
Система состоит из трёх компонентов (распределяемое вещество А и два распределяющих вещества) и двух фаз – жидкой и газовой. Такая система по правилу фаз имеет три степени свободы:  . Для абсорбции переменными являются Т, Р, концентрация компонента А в газовой и жидкой фазах. Следовательно, в состоянии равновесия при Т=const и постоянном общем давлении Р зависимость между парциальным давлением газа
. Для абсорбции переменными являются Т, Р, концентрация компонента А в газовой и жидкой фазах. Следовательно, в состоянии равновесия при Т=const и постоянном общем давлении Р зависимость между парциальным давлением газа 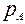 или его концентрацией и составом жидкой фазы однозначна. Эта зависимость выражается законом Генри: парциальное давление
или его концентрацией и составом жидкой фазы однозначна. Эта зависимость выражается законом Генри: парциальное давление 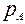 растворённого газа пропорционально его мольной доле
растворённого газа пропорционально его мольной доле  в растворе:
в растворе:
 (2.1)
(2.1)
где  - парциальное давление поглощаемого газа над раствором, находящегося в равновесии, при концентрации раствора
- парциальное давление поглощаемого газа над раствором, находящегося в равновесии, при концентрации раствора 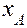 , Е – константа Генри. Е не зависит от общего давления в системе, но зависит от природы абсорбента и поглощаемого газа, а также от Т.
, Е – константа Генри. Е не зависит от общего давления в системе, но зависит от природы абсорбента и поглощаемого газа, а также от Т.
Растворимость газа в жидкости при данной температуре пропорционально его парциальному давлению над жидкостью:
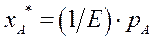 (2.2)
(2.2)
Здесь 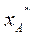 - концентрация газа в растворе, равновесная с газовой фазой, в которой парциальное давление поглощаемого компонента равна
- концентрация газа в растворе, равновесная с газовой фазой, в которой парциальное давление поглощаемого компонента равна 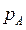 .
.
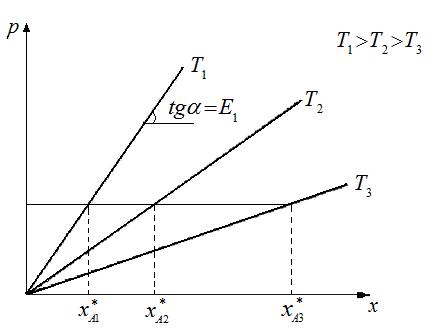
Рис.2.1 Растворимость газа в жидкость от Т.

Для идеальных растворов на диаграмме р–х (рис.2.1) зависимость равновесных концентраций от давления изображается прямой, с наклоном, равным Е.
Как видно из рис.2.1,чем больше Т, тем меньше растворимость.
Если 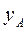 – молярная доля извлекаемого компонента А в газовой смеси и Р – общее давление в системе, то парциальное давление
– молярная доля извлекаемого компонента А в газовой смеси и Р – общее давление в системе, то парциальное давление 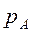 , по закону Дальтона, можно записать:
, по закону Дальтона, можно записать:
 (2.3)
(2.3)
Тогда, с учетом уравнения (2.1) получим:
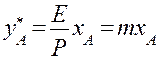
Итак для закона Генри имеем:
 (2.4)
(2.4)
Здесь 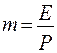 - коэффициент распределения, или константа фазового равновесия.
- коэффициент распределения, или константа фазового равновесия.
|
|
|
Величина m уменьшается с увеличением Р и снижения Т. Таким образом, растворимость газа в жидкости растёт с ростом давления и снижения Т.
Когда в равновесии с жидкостью находятся смесь газов, закону Генри может следовать каждый из компонентов смеси в отдельности.
Закон Генри справедлив только для идеальных газов, а также к сильно разбавленным реальным растворам. Для хорошо растворимых газов, при больших концентрациях их в растворе, растворимость меньше, чем по закону Генри. Для систем, не подчиняющихся закону Генри, m является величиной переменной и линия равновесия представляет собой кривую, которую строят обычно по опытным данным.
При больших давлениях (1 МПа и выше) изменение объёма жидкости вследствие растворения в ней газа соизмеримо с изменением объёма газа и равновесие в этом случае не следует закону Генри. При этих условиях константу фазового равновесия можно определить как:
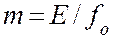 (2.5)
(2.5)
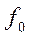 - фугитивность (летучесть) поглощаемого газа, выраженная в единицах давления.
- фугитивность (летучесть) поглощаемого газа, выраженная в единицах давления.
При записи уравнений материального баланса и рабочих линий целесообразно выбрать единицы измерения расходов таковыми, чтобы эти величины не менялись по высоте аппарата. Это сделает рабочие линии прямыми.
При выражении состава фаз не в абсолютных, а в относительных концентрациях видоизменяется и запись закона Генри.
Общая масса фазы, состоящей из распределяемого компонента и 1 кг носителя равна (1+Х) кг (жидкая фаза) и (1+У) кг (газовая фаза). Тогда весовые концентрации х и у распределяемого компонента в фазах:
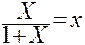

Тогда закон Генри запишется:
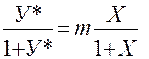 (2.6)
(2.6)
Следовательно, линия равновесия в системе газ – жидкость в координатах Х и У изображается кривой. При малых концентрациях Х в жидкости (2.6) упрощается и принимает вид:
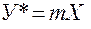
В случае абсорбции многокомпонентных смесей парциальное давление каждого компонента в газовой смеси зависит не только от его концентрации в растворе, но и от концентрации в растворе других компонентов, т.е. является функцией большого числа переменных. Поэтому в подобных случаях, равновесные зависимости основываются на опытных данных.
|
|
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 470; Нарушение авторских прав?; Мы поможем в написании вашей работы!