
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Литиевые системы с твердым катодом
|
|
|
|
Система Li│MnO2
В качестве электролита чаще используется 1М раствор LiClO4. в смешанном растворителе ПК + ДМЭ, поэтому электрохимическая система может быть записана более подробно:
(–) Li│ LiClO4, ПК + ДМЭ │MnO2 (+)
Система Li│MnO2 имеет достаточно высокие удельные характеристики при относительно низкой цене. Удельная энергия 200 – 250 Вт·ч/кг или 450 – 550 Вт·ч/л (несколько ниже, чем у Li│SO2 и Li│CuO). Существенным недостатком этой системы является малая удельная мощность, обусловленная слабыми разрядными токами (менее 1 мА/см2) и ограниченный, по сравнению с другими ЛИТ, температурный интервал работоспособности: от –20°С до +50°С. В остальном же они обладают всеми достоинствами ЛИТ, в том числе и чрезвычайно высокой сохранностью своих характеристик (хранение до 10 лет и более). НРЦ = 3.5 В. Разрядное напряжение 2.8 – 3.0 В. Разряд обычно ведут до 2 В, глубокий разряд небезопасен. Эта систем появилась одной из первых и широко применяется во всем мире. В России производятся в г. Саратов.
Рассмотрим химию протекающих процессов. В результате токообразующей реакции
х Li+ + х е + MnO2 → LixMnO2
или
х Li + MnO2 → LixMnO2
образуется так называемое соединение внедрения. Большинство твердых катодных материалов восстанавливается по аналогичному механизму внедрения.
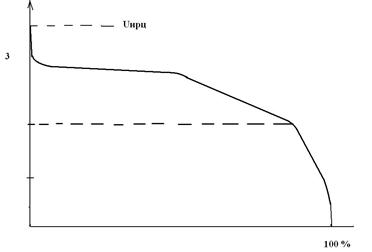
Схематичная разрядная кривая литий-диоксидмарганцевого ХИТ.
Вообще, при разряде твердых катодов (оксидов, халькогенидов и т.п.) первичный процесс протекает следующим образом: электроны, поступающие из внешней цепи, поглощаются электронной подсистемой кристаллической решетки, понижая степень окисления металла, а компенсирующие их заряд катионы Li+ десольватируются и внедряются в кристаллическую решетку из раствора. Например, рассматривая эту реакцию как окислительно-восстановительную, можно говорить о понижении степени окисления ионов марганца в MnO2 с +4 до +3.
|
|
|
Дальнейшая судьба такого соединения зависит от кристаллографической структуры, от соотношения параметров кристаллической решетки твердого тела и размеров катиона Li+. Если объем элементарной ячейки кристаллической решетки достаточно велик, то соединение внедрения оказывается стабильным, и именно оно будет продуктом разряда. Подобные соединения могут работать обратимо, так что катион Li+ может быть выведен обратно в раствор при изменении направления электрического тока. В последнем случае процесс внедрения называют также интеркаляцией, а образовавшиеся соединения внедрения – интеркалятами (от англ. «intercalate» – вставлять). Такое вещество является пригодным для использования в перезаряжаемых ЛИТ – литиевых аккумуляторах.
В противном случае внедрение иона лития совершается необратимо, с разрушением исходной кристаллической решетки и построением новых веществ. Такой вариант пригоден для первичных ЛИТ.
Как уже говорилось при рассмотрении элемента Лекланше Zn|MnO2, диоксид марганца – весьма сложное вещество, существующее во множестве модификаций и переходных форм. В зависимости от модификации MnO2 и от значения «х» в уравнении токообразующей реакции, она может протекать как необратимо, так и обратимо.
Система Li│CuO
В качестве электролита чаще используется 1М раствор LiClO4. в смешанном растворителе ПК + ТГФ, поэтому электрохимическая система может быть записана более подробно:
(–) Li│ LiClO4, ПК + ТГФ │CuO (+)
Токообразующая реакция простая:
2Li + CuO → Li2O + Cu
НРЦ = 2.4 В. Элементы имеют высокую (хотя и вдвое меньшую, чем у Li│SOCl2) удельную энергию 300 Вт·ч/кг и 600 Вт·ч/л, разрядное напряжение 1.5 В, что делает их взаимозаменяемыми с традиционными элементами Лекланше. Выпускаются цилиндрической и пуговичной конструкции малых типорамеров для питания электроники. Рассчитаны на длительный разряд малыми токами (больших токов не выдерживают). Обладают чрезвычайно высокой сохранностью энергии (потери менее 2 % за 15 лет хранения).
|
|
|
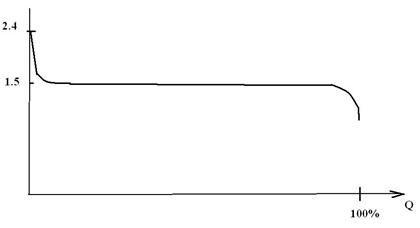
Схематичная разрядная кривая источника тока Li│CuO.
Система Li│LiJ│J2
В качестве примера полностью твердофазного ЛИТ рассмотрим электрохимическую систему литий | йод. Токообразующая реакция имеет вид
Li + 0.5J2 → LiJ
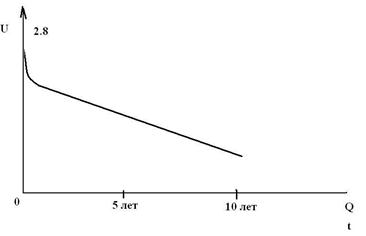
Схематичная разрядная кривая источника тока литий | йод.
НРЦ = 2.8 В, удельная энергия достигает 700 – 1000 Вт·ч/л. Источник тока состоит из литиевого анода и катодной массы, содержащей йод, которые находятся в непосредственном контакте друг с другом. Никакого жидкого электролита, а также разделителя-сепаратора в таком источнике тока нет. Роль твердого электролита и сепаратора играет слой йодида лития LiJ, образующийся сразу же за счет прямой химической реакции между литием и йодом. В ходе дальнейшего разряда LiJ только накапливается. Этот слой обладает очень высоким электрическим сопротивлением, которое возрастает по мере увеличения его толщины при разряде. Поэтому йодно-литиевые ХИТ могут разряжаться только чрезвычайно малыми токами (1 – 2 мкА/см2), а разрядная кривая имеет падающий вид из-за непрерывного роста внутреннего сопротивления (см. рисунок). Но в таком слаботочном режиме система литий | йод может работать годами. Основное применение – питание имплантируемых кардиостимуляторов и нейростимуляторов. Как и у других ЛИТ – высокая надежность, сохранность более 10 лет. Эти ЛИТ также производятся в России в г. Саратове.
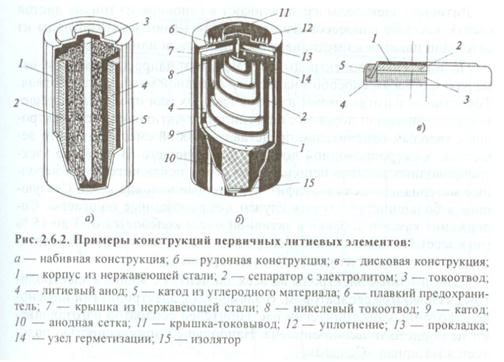
На рисунке ниже даны примеры конструкции первичных ЛИТ.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 521; Нарушение авторских прав?; Мы поможем в написании вашей работы!