
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция №6. Тепловой эффект реакции при стандартных условиях равен разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ
|
|
|
|
Тепловой эффект реакции при стандартных условиях равен разности между суммой теплот образования продуктов реакции и суммой теплот образования исходных веществ умноженных на соответствующие стехиометрические коэффициенты.
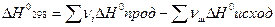 (20)
(20)
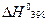 тепловой эффект химической реакции
тепловой эффект химической реакции
.
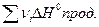
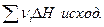 - сумма теплот образования продуктов реакции и исходных веществ
- сумма теплот образования продуктов реакции и исходных веществ
.
Для реакции 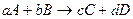 Можно выразить:
Можно выразить:

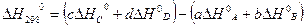 (21)
(21)
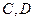 – продукты реакции.
– продукты реакции.
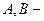 исходные соединения,
исходные соединения,
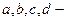 стехиометрические коэффициенты..
стехиометрические коэффициенты..
Второе следствие закона Гесса.
Тепловой эффект реакции при стандартных условиях равен разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов реакции, умноженных на соответствующие стехиометрические коэффициенты.
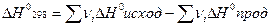 (22)
(22)
Теплоемкость.
Теплоемкостью называют способность веществ поглощать при нагревании теплоту. Различают удельную и молярную теплоемкости
Удельной теплоемкостью называется количество теплоты, необходимое для нагревания единицы массы вещества на 1,К.
Молярной теплоемкостью называется количество теплоты, необходимое для нагревания 1моля вещества на 1,К. В зависимости от нагревания или охлаждения вещества различают теплоемкость при постоянном объеме Сv и теплоемкость при постоянном давлении Ср.
В тепловых расчетах используют истинную теплоемкость веществ при данной температуре или среднюю теплоемкость в пределах заданных температур.
Истинной теплоемкостью называют отношение бесконечно малого количества теплоты полученного телом к соответствующему приращению его температуры.
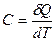 (23)
(23)
С – молярная теплоемкость, Дж/моль К
Средней теплоемкостью называют отношение конечного количества теплоты,подведенного к одному моль вещества,к разности температур Т2 - Т1
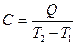 . (24)
. (24)
Количество теплоты, переданное телу при постоянном объеме., равно приращению внутренней энергии 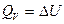 . Истинная теплоемкость выразиться уравнением.
. Истинная теплоемкость выразиться уравнением.
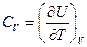 (25)
(25)
Количество теплоты, переданное телу при постоянном давлении равно, приращению энтальпии. 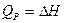 Отсюда истинная теплоемкость выразиться уравнением:
Отсюда истинная теплоемкость выразиться уравнением:
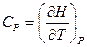 (26)
(26)
Количество теплоты, затраченное на нагревание n молей вещества от Т1 до Т2 определяется соотношением:
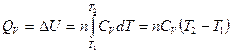 (27)
(27)
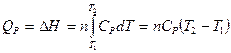 (28)
(28)
Теплоемкости при постоянном объеме и постоянном давлении отличаются на величину работы, необходимой для изменения объема системы.
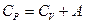 (29)
(29)
Для 1 моль идеального газа при нагревании на 1, К при p = const
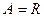 . Следовательно,
. Следовательно,
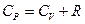 (30)
(30)
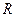 - универсальная газовая постоянная.
- универсальная газовая постоянная.
Для жидкостей и твердых тел вследствие малого изменения объема при нагревании 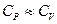
Уравнение Кирхгофа
Зависимость теплового эффекта химической реакции от температуры выражает уравнение Кирхгофа в интегральной форме:
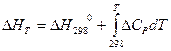 (31)
(31)
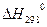 - тепловой эффект реакции при стандартных условиях
- тепловой эффект реакции при стандартных условиях
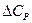 – изменение теплоемкости системы.
– изменение теплоемкости системы.
Значение 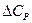 определяется как разность суммарной теплоемкости продуктов исходных веществ с учетом их стехиометрических коэффициент:
определяется как разность суммарной теплоемкости продуктов исходных веществ с учетом их стехиометрических коэффициент:
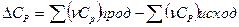 (32)
(32)
для химической реакции 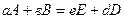
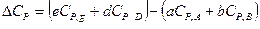
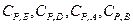 - молярные теплоемкости реагентов при постоянном давлении.
- молярные теплоемкости реагентов при постоянном давлении.
Влияние температуры на тепловой эффект химической реакции обуславливается знаком величины 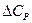
.
1) при 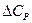 > 0 тепловой эффект с ростом температуры возрастает:
> 0 тепловой эффект с ростом температуры возрастает: 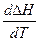 > 0
> 0
2) при 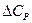 < 0 тепловой эффект реакции с ростом температуры уменьшается
< 0 тепловой эффект реакции с ростом температуры уменьшается 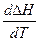 < 0
< 0
3) при 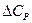 = 0
= 0 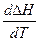 = 0 тепловой эффект реакции не зависит от температуры.
= 0 тепловой эффект реакции не зависит от температуры.
Вопросы для самопроверки
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 734; Нарушение авторских прав?; Мы поможем в написании вашей работы!