
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Горение газового топлива
|
|
|
|
Ранее были изложены основные законы кинетики (законы действующих масс и Аррениуса), позволяющие определять скорость химических реакций на основе стехиометрических соотношений молекул исходных и конечных продуктов. Экспериментально установлено, что скорости протекания реакций существенно превышают расчетные значения, полученные с применением закона действующих масс и закона Аррениуса.
В действительности реакции в веществах, находящихся в парогазовом состоянии, протекают чаще не между исходными молекулами горючего и окислителя, а через ряд промежуточных стадий, в которых вместе с молекулами участвуют активные осколки молекул - радикалы и атомы, имеющие свободные связи Н, ОН, О, СН и др. При этом переход от исходных веществ к конечным продуктам происходит через ряд промежуточных реакций, протекающих с большой скоростью, так как они обладают низкой энергией активации. Такие реакции, отличительной особенностью которых является огромная скорость их протекания, получили название цепных.
При горении газов протекают разветвленные реакции, в процессе которых один активный центр порождает два или большее число новых активных центров. Теорию цепных реакций разработал академик Н.Н. Семенов.
Согласно этой теории, цепная разветвленная реакция включает следующие процессы: зарождение цепей - образование активных частиц из исходного продукта; разветвление цепей - процесс, при котором одна активная частица, реагируя с исходными, вызывает образование двух или нескольких новых активных частиц; по мере убывания горючих компонентов реакция замедляется, наступает обрыв цепей и реакция вырождается - горение прекращается.
|
|
|
Началу реакции между веществами предшествует период накопления активных центров в виде заряженных частиц за счет разрушения части исходных молекул другими, обладающими большими энергиями движения и более высокой энергией связи атомов в молекуле. Этот период называют периодом индукции. При высокой температуре вступающих в реакцию веществ период индукции занимает от долей секунды до 1…2 с.
Рассмотрим механизм цепной разветвленной реакции на примере горения водорода (рис. 4.4). Из цикла цепной реакции следует, что наряду с образованием конечного продукта Н2О увеличивается число активных частиц - возбудителей цепи Н. На один вступивший в реакцию активный атом водорода после первого цикла образуется три атома водорода, после второго цикла - 9, после третьего - 27 и т.д. Это приводит к дальнейшему лавинообразному ускорению реакции. В реальных процессах одновременно с лавинообразным ускорением образования активных центров часть их по ряду причин при контакте со стенками сосуда, друг с другом теряет активность, что ведет к постепенному снижению скорости нарастания реакции и переходу ее в установившееся состояние, если имеет место постоянный подвод кислорода и водорода в зону реакции.
Горение газового топлива в смеси с воздухом происходит с большой скоростью (готовая смесь метана с воздухом объемом 10 м3 сгорает за 0,1 с).
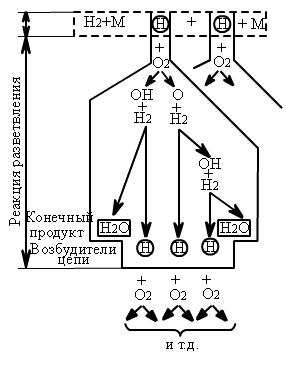
| Рис. 4.4. Цикл цепной реакции горения водорода: H - возбудитель цепной реакции; H2O - конечный продукт |
Поэтому интенсивность сжигания природного газа в топках паровых котлов определяется скоростью его смешения с воздухом в горелочном устройстве и топке, т.е. скоростью подготовки горючей смеси.
В турбулентном потоке горючей смеси метана с воздухом скорость распространения пламени uПЛ, м/с, определяется турбулентной диффузией веществ и находится по приближенной формуле
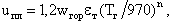
| 4.15 |
где wГОР - скорость воздуха на выходе из горелки, м/с; ТГ, - расчетная температура газовой среды, К; n = 0,60…1,65 - показатель степени; изменяется в зависимости от состава горючей смеси и скорости потока. Для промышленных горелок, сжигающих природный газ, значение n близко к единице; εТ = 0,25…0,30 - степень турбулентности потока воздуха. В итоге скорость распространения газового пламени обычно составляет uПЛ = 8… 12 м/с.
|
|
|
Трудность обеспечения полного смешения расхода газа с воздухом за короткий промежуток времени связано с большим различием объемных расходов газа и воздуха - на сжигание 1 м3 газа требуется 10 м3 воздуха. Для полноты перемешивания приходится в поток воздуха внутри горелки вводить газ большим количеством мелких струй малого диаметра и с большой скоростью. Воздушный поток также сильно турбулизуется в специальных завихривающих устройствах.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 647; Нарушение авторских прав?; Мы поможем в написании вашей работы!