
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Первый способ - регулирование РН солевого раствора
|
|
|
|
Способы подавления гидролиза солей
Существует три способа подавления гидролиза солей.
· Соли, образованные слабым гидроксидом и сильной кислотой, необходимо подкислять для подавления гидролиза, то есть понижать РН.
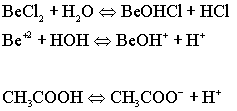
В результате увеличения концентрации продуктов реакции, в данном случае H+, по принципу Ле Шателье равновесие смещается в обратном направлении, то есть в сторону образования соли.
· Соли, образованные сильным гидроксидом и слабой кислотой, необходимо подщелачивать для подавления гидролиза, то есть повышать РН.
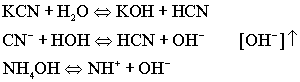
Два других способа подавления гидролиза:
· понижение температуры солевого раствора,
· повышение концентрации солевого раствора.
Данные способы применяются к солям, образованным слабым гидроксидом и слабой кислотой, для которых регулирование PH раствора не действенно.
На практике, как правило, применяют все три способа подавления гидролиза одновременно.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 306; Нарушение авторских прав?; Мы поможем в написании вашей работы!