
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Задачи с разбором. 1. Сколько атомов водорода содержится в 1 л водорода при н
|
|
|
|
1. Сколько атомов водорода содержится в 1 л водорода при н. у.?
Решение. Т. к. 1 моль любого идеального газа занимает при н. у. 22,4 л, то в 1 л водорода (мы можем считать его приближенно идеальным газом) будет содержаться 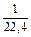 = 0,045 моль молекул водорода. Каждая молекула водорода состоит из двух атомов, значит, количество атомов в два раза больше: 2 × 0,045 = 0,09 моль. Чтобы найти, сколько атомов находится в этом количестве вещества, умножим его на число Авогадро:
= 0,045 моль молекул водорода. Каждая молекула водорода состоит из двух атомов, значит, количество атомов в два раза больше: 2 × 0,045 = 0,09 моль. Чтобы найти, сколько атомов находится в этом количестве вещества, умножим его на число Авогадро:
0,09 × 6,022 × 1023 = 5,4 × 1022 штук.
2. Какова масса 1 молекулы NaOH?
Решение. Рассчитаем сначала молекулярную массу NaOH в единицах а. е. м., исходя из значений атомных масс натрия, кислорода и водорода.
M r (NaOH) = 23 + 16 + 1 = 40 а. е. м.
А теперь переведем в единицы СИ:
40 × 1,6606 × 10–27 = 6,64 × 10–26 кг.
3. Какая энергия выделяется при образовании атома гелия из элементарных частиц?
Решение. Атомная масса гелия 4,0026 а. е. м. Рассчитаем суммарную массу элементарных частиц, составляющих гелий:
2 m p + 2 m n + 2 m e = 2(1,007 + 1,009 + 5,5 × 10–4) = 4,0331 а. е. м.
Дефект массы составляет
4,0331 – 4,0026 = 3,05 × 10–2 а. е. м.
или
3,05 × 10–2 × 1,6606 × 10–27 = 5,1 × 10–29 кг.
Е = D mc 2 = 5,1 × 10–29 × (3 × 108)2 = 4,6 × 10–13 Дж.
4. А г СаО растворили в избытке воды массой В г. Выразите массовую долю вещества в полученном растворе.
Решение. Для решения этой задачи необходимо помнить, что при растворении оксида кальция в воде происходит реакция СаО + Н2О = Са(ОН)2, поэтому растворенным веществом будет гидроксид кальция.
w =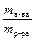 (´ 100%).
(´ 100%).
Массу вещества найдем по уравнению реакции:
m (Са(ОН)2) = М(Са(ОН)2) × 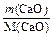 = 74 ×
= 74 ×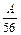 = 1,32А.
= 1,32А.
Масса раствора складывается из массы веществ, образовавших этот раствор (поскольку в результате реакции не выпадает осадок и не выделяется газ, ничего вычитать не требуется) A + B. Таким образом, w =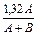 (´ 100%).
(´ 100%).
|
|
|
5. Смешали 11,2 л хлора и 22,4 л водорода. Найдите объемные доли газов в смеси после прохождения реакции.
Решение. Протекает реакция H2 + Cl2 = 2 HCl. Так как объемы газов пропорциональны их количествам веществ, то 1 объем водорода будет реагировать с 1 объемом хлора, при этом образуются 2 объема хлороводорода. Хлор в недостатке, он прореагирует полностью; 11,2 л водорода вступит в реакцию и еще 11,2 л останется. Хлороводорода получится 2 × 11,2 = 22,4 л.
Суммарный объем системы 11,2 + 22,4 = 33,6 л. Объемная доля водорода 11,2 / 33,6 = 0,33 (33%), хлороводорода 22,4 / 33,6 = 0,67 (67%), или
100 – 33 = 67%.
6. В сплаве содержится 40 % K и 60 % Na. Найдите мольные доли компонентов.
Решение. М(K) = 39, M(Na) = 23. Если в 100 г сплава содержится 40 г K, то это составляет 40 / 39 = 1,03 моль. 60 г натрия – это 60 / 23 = 2,61 моль. Общее количество вещества в 100 г сплава 1,03 + 2,61 = 3,64 моль. Отсюда мольные доли: калия 1,03 / 3,64 = 0,28 (28%), натрия 2,61 / 3,64 = 0,72 (72%), или 100 – 28 = 72%.
7. Соединение углерода с водородом содержит 75 % углерода по массе. Найдите формулу этого соединения.
Решение. Напишем формулу в общем виде: С х Н у. Масса углерода в молекуле этого вещества пропорциональна 12 х, водорода – у. Т. к. массовая доля углерода 75%, получаем: 12 х: у = 75: 25, отсюда х: у = 6,25: 25 = 1: 4. Искомая формула СН4.
8. Плотность газа по воздуху 0,55. Что это за газ?
Решение. Средняя молярная масса воздуха 29. Чтобы найти молярную массу газа, умножим 29 на плотность газа: 29 × 0,55 = 16. Эта молярная масса соответствует метану СН4, других вариантов нет.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 3431; Нарушение авторских прав?; Мы поможем в написании вашей работы!