
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамика полиприсоединения и поликонденсации
|
|
|
|
Следствием различия знаков изменения составляющих энергии Гиббса для процесса полимеризации является критическая температура Тcr, которая соответствует равновесному состоянию системы при которой полимер не м.б. получен.
Термодинамика полимеризации
С помощью знания термодинамики процесса можно определить:
· область изменения термодинамических факторов (температуры, давления и т.п.), в которой процесс синтеза данного полимера принципиально осуществим.
· влияние факторов (температуры, давления и т.п.) на сам ход процесса полимеризации в реальных условиях и на качество получаемого продукта.
Для обычных процессов полимеризации, протекающих при постоянном давлении, условием их осуществимости является уменьшение в ходе процесса энергии Гиббса ∆G, зависящего в свою очередь, от изменений в этом же процессе энтальпии ∆H и энтропии ∆ S:
∆G = ∆H + T∆S < О
Для процесса полимеризации ненасыщенных мономеров тепловой эффект реакции полимеризации (разница энергий рвущихся связей C=C) в газовой фазе равен: 200 кДж/моль (или около 100 кДж/моль на одну связь С-С). Заместители немного уменьшают это значение, но, надо знать, что эти реакции сильно экзотермичны.
В промышленности тепловой эффект полимеризации обычно выражают в кДж на 1 кг заполимеризованного мономера с учетом изменения агрегатного состояния в ходе процесса. Обычно принимается, что мономер является жидкостью, а полимер - твердым телом - аморфным или кристаллическим. Ориентировочные значения этих эффектов (кДж/кг) таковы: этилен - 3900, пропилен - 2480, формальдегид - 2350, винилхлорид - 1640, бутадиен - 1300, изопрен - 966, стирол - 670-714. Эти значения столь существенны, что многотоннажные производства ПЭВД одновременно является источником водяного пара высоких параметров.
|
|
|
Изменение энтропии ∆S определяется изменением в ходе реакции числа степеней свободы системы. Естественно, что для полимеризации ∆S < 0.
Зависимость изменения энтропии от фазового состояния полимера приводит к возможности управления надмолекулярной структурой образующегося полимера. Например, при проведении процесса полимеризации вблизи равновесных условий можно направлять его в сторону образования кристаллического (при концентрациях полимера, меньших соответствующих термодинамическому «насыщению») или аморфного (при «пересыщенности» раствора полимера) состояния.
∆G = АН - T∆S = О => Тcr = ∆Н/∆S
Физический смысл Тcr, заключается в том, это если температура смеси с концентрацией мономера [М] достигает Тcr,, то реакция останавливается вследствие достижения равновесного состояния.
Аналогия позволяет легче представить себе причины появления этой температуры: кристаллизация из раствора соли не будет иметь места, если он нагрет до температуры, при которой концентрация соли равна пределу ее растворимости в данном растворителе.
Измеряя предельную концентрацию мономера при различных температурах, можно получить зависимость предельной температуры для текущей концентрации мономера. Зависимость l/ Тcr от ln [М] близка к линейной.
Величина критической температуры сильно зависит от строения молекул мономера и полимера, их агрегатного состояния и т.п., и изменяется в широких пределах: от 624 К для этилена и до 392 К для формальдегида.
Ряд мономеров имеют столь низкую критическую температуру, что этo может оказывать влияние на практику их полимеризации. Например, низкими значениями обладают А-метилстирол (340 К = 67°С), ацетальдегид (351 К = 78°С), тетрагидрофуран (357 К = 84°С).
Критическая температура может, как увеличиваться, так и уменьшаться с ростом давления. Обычно ∆S < О и ∆ V < 0, и увеличение давления приводит к увеличению Тcr.Это, однако, становится заметным лишь при значениях давления порядка сотен МПа, в виду небольшого изменения объема в ходе реакции в конденсированной фазе.
|
|
|
Температура определяет положение равновесия и равновесный выход полимера. Существует максимум скорости реакции обратимой полимеризации при определенной температуре.
С критической температурой можно сравнить максимальную (адиабатическую) температуру, которая может быть достигнута реакционной смесью в ходе реакции полимеризации. Таким пределом является известная адиабатическая температура (Tad), достигаемая реакционной смесью при полном отсутствии теплообмена с окружающей средой. Тепловой эффект химической реакции в этом случае просто повышает теплосодержание реакционной смеси. Ясно, что при Tad > Тcr процесс становится невозможным термодинамически. При Tad = Тcr система стремится к равновесию, скорость реакции - к нулю, а мгновенная степень полимеризации - к единице. (см. Рис.2)
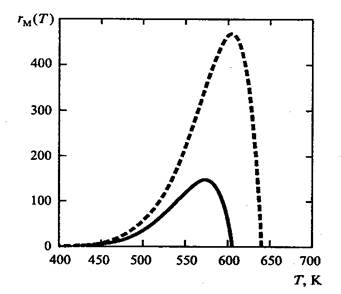
Рис. 2. Зависимость скорости обратимой экзотермической реакции полимеризации от температуры при различных концентрациях раствора мономера: 5 моль/л сплошная кривая, 7 моль/л - пунктирная.
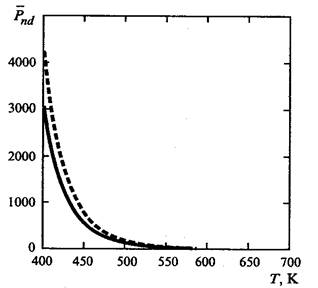
Рис.3. Зависимость среднечисловой степени полимеризации от температуры
Фазовые переходы в процессах полимеризации определяют не только положение критической температуры, но и оказывают сильное влияние на ММР образующегося полимера (см.Рис.3). Например, выделение в отдельную фазу нерастворимого в своем мономере ПВХ должно приводить к своеобразному «смещению» равновесия в сторону полимера по чисто кинетическим причинам из-за эффекта «замуровывания» части активных радикалов в твердом полимере.
Термодинамические характеристики реакций синтеза полимеров методами поликонденсации и полиприсоединения отличаются большим многообразием.
Реакции полиприсоединения (например, связанные с разрывом кратной связи - N =С= в изоцианатной группе или раскрытием эпоксидного цикла) являются экзотермическими и протекают с уменьшением энтропии, однако критическая температура для них обычно лежит значительно выше обычных условий их осуществления. Кроме того, в отличие от полимеризации, имеются другие возможности смещения равновесия в сторону образования полимера.
|
|
|
Реакции поликонденсации, протекающие с выделением низкомолекулярного побочного продукта (НМП), весьма сильно различаются как по изменению энтальпии (тепловому эффекту), так и по энтропии.
Процессы полиэтерификации многоосновных кислот полиатомными спиртами характеризуются небольшими тепловыми эффектами порядка от -10 до +10 кДж/моль и уменьшением энтропии на 40-80 Дж/(моль· К).
Например, тепловой эффект реакции синтеза диэтиленгликолевого эфира терефталевой кислоты оценивается в -8.4 кДж/моль, что приводит К некоторому уменьшению константы равновесия с ростом температуры: от - 0.5 при 220°С до -0.4 при 280°С.
Реакции образования метилольных производных фенолов, карбамида и меламина, сопровождаются выделением тeплоты и уменьшением энтропии (40-70 кДж/моль и 80-100 Дж/(моль· К) соответственно).
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1830; Нарушение авторских прав?; Мы поможем в написании вашей работы!