
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
А каков будет теплоотвод?
|
|
|
|
Пусть температура смеси Т будет выше температуры стенки То, т.е. Т > То. В этом случае смесь будет отдавать теплоту стенке, и вычислить такой тепловой поток можно по формуле Ньютона:
q_ = a (Т-То), кДж/м2×с
где a - коэффициент теплоотдачи, кДж/м2×град.
С учетом общей поверхности сосуда S получается следующее выражение для расхода теплоты:
q_= a(T-To)×S, кДж/c.
Анализ полученных выражений показывает, как и почему будет меняться тепловое состояние системы в зависимости от температуры стенки сосуда и самой горючей смеси. Графически q+ представляет собой экспоненциальную зависимость, а q_ - прямую линию (рис.2).
Рассмотрим состояние системы при температуре стенки T01 = const. Пусть Т будет меньше T01 (начало графика). Здесь приход теплоты выше расхода, т.е. q+ > q_, поэтому смесь будет нагреваться, и в точке А установится равновесие. В этой точке, естественно, химическая реакция продолжается, но при малейшем повышении температуры смеси система вновь вернется в эту точку, поскольку там (справа от точки А) расход теплоты выше прихода. При смещении влево система опять же вернется в точку А, поскольку здесь наоборот приход теплоты больше расхода. Таким образом, в точке А система находится в состоянии устойчивого равновесия, и реакция будет спокойно идти до полного расходования компонентов или ее вообще не будет.
Теперь повысим температуру стенок сосуда до Т02. Прямая теплоотвода сместится параллельно самой себе вправо, и кривая прихода будет касаться ее в единственной точке С. Вначале горючая смесь будет нагреваться от температуры Та до Тс, и система перейдет в точку С, установится равновесие (q+ = q_). При малейшем увеличении температуры смеси выше Тс система тут же сместится вправо, а там приход теплоты превышает расход. Поэтому смесь будет стремительно по экспоненциальному закону нагреваться до самовоспламенения. То есть произойдет тепловой взрыв. Следовательно, температура стенки Т02, для которой прямая отвода теплоты – касательная кривой выделения, является предельной для существования стационарного режима, т.е. критической температурам самовоспламенения. Как видно из рисунка, она несколько ниже истинной температуры самовоспламенения Тс. Для саморазогрева горючей смеси от температуры Т02 до Тс необходимо время, которое называется индукционным периодом теплового взрыва (самовоспламенения).
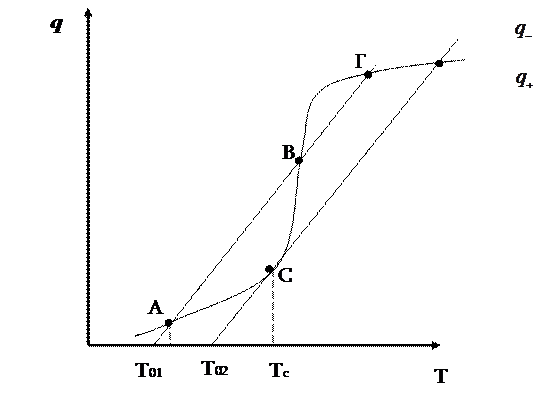
Рис.1.2. Изменение выделения q+ и отвода q_ теплоты
в зависимости от температуры.
Величина индукционного периода в ряде случаев достигает пяти и более секунд. Следует отметить, что реальные системы находятся либо под атмосферным, либо под повышенным давлением. Поэтому в них не реализуется в чистом виде только цепной или только тепловой механизм самовоспламенения. На практике в большинстве случаев механизм самовоспламенения смешанный, цепочечно-тепловой, но рассмотренные здесь закономерности остаются справедливыми и для такого смешанного механизма.
3. Температура самовоспламенения как показатель пожарной опасности, практическое значение и методы ее определения
Пожарная опасность - это возможность возникновения и развития пожара, заключенная в каком-либо веществе или процессе.
Показатель пожарной опасности - величина, которая количественно характеризует какое-либо свойство пожарной опасности.
Температура самовоспламенения - это наименьшая температура окружающей среды, при которой в условиях специальных испытаний наблюдается самовоспламенение вещества.
Температура самовоспламенения относится к числу важнейших показателей пожарной опасности. Ее используют при оценке пожаровзрывоопасности веществ, при определении группы взрывоопасности горючей смеси и т.д. Практическое определение температуры самовоспламенения основывается на следующих теоретических предпосылках (см. рис.2). В точке С устанавливается равенство прихода и расхода теплоты, т.е. q+ = q_. Подставив сюда соответствующие выражения для тепловыделения и теплоотвода, получим уравнение теплового баланса для точки С:
Qгop = V×ko×Cгop×Cок×exp(-E/RT) = a(T-To)×S
Перенесем объем сосуда V в правую часть уравнения:
Qгop×ko×Cгop×Cок×exp(-E/RT) = a(T-To)×S / V
Левая часть этого выражения представляет собой скорость выделения теплоты в единице объема горючей смеси, а правая - скорость отвода через поверхность стенок сосуда из этой же единицы объема. То есть выражение показывает, что температура самовоспламенения зависит от множества факторов: от размера и формы сосуда (S/V); от химических свойств горючего и его способности к окислению (тепловой эффект Qгop, энергия активации Е и константа скорости реакции ko, от концентрации реагирующих веществ (Cгop и Сок) и, наконец, от теплофизических свойств горючей смеси и материала стенки сосуда (коэффициент теплоотдачи a). Это свидетельствует о том, что температура самовоспламенения не является физической константой горючих веществ.
Как будет меняться температура самовоспламенения при изменении объема сосуда, т.е. при изменении отношения площади стенок к объему S/V? Это отношение называется_ удельной поверхностью и имеет размерность 1/м или м-1. Например, для куба с гранью а удельная поверхность будет равна
S/V = 6а2/а3 == 6/а
Предположим, что в уравнении теплового баланса меняется только температура в точке С. Тогда левая часть уравнения изменяться не будет, и соответствующая ей кривая тепловыделения останется на прежнем месте. Правая часть уравнения - прямая линия, которая касается кривой в точке С. Величина aS/V есть угловой коэффициент этой прямой илиtgb - угла ее наклона к оси абсцисс (см. рис.1.3)

Рис.1.3. Изменение теплового баланса горючей смеси
при увеличении объема сосуда.
Увеличим грань куба в три раза. Его удельная поверхность станет равной:
S / V = 6(3а)2 / (За)3 = 2 /а,
т.е. уменьшится в три раза, значит уменьшится и сам угол b. В этом случае прямая теплоотвода будет располагаться ниже предыдущей прямой, и точка С в месте с ней переместится в точку C1, а значит будет ниже и критическая температура самовоспламенения. Следовательно, с увеличением объема сосуда температура самовоспламенения снижается. Увеличить теплоотвод можно не только уменьшением объема горючей смеси, но и приданием ей соответствующей формы.
На рис.1.4 изображены равные объемы разной формы. При нагреве в кубе происходит самовоспламенение, а в пластине - нет.

Рис.1.4. Равновеликие объемы разной формы сосудов
с горючей смесью (размеры даны в метрах)
Температура самовоспламенения зависит от состава горючей смеси,
принимая минимальное значение при стехиометрическом соотношении
компонентов (рис.1.5). Эта зависимость используется для экспериментального определения Тс. Начиная с некоторых предельных значений, смеси как бедные, так и богатые не способны воспламеняться. Это подтверждается экспериментально. Например, кривая зависимости Тс = f(C) для оксида углерода имеет минимум при 20 %.
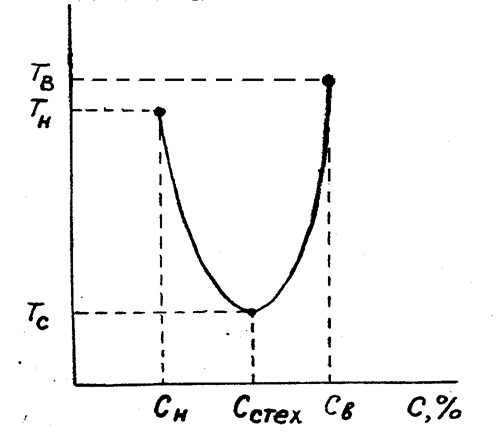
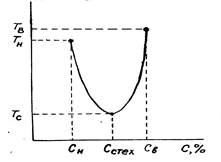
Рис.1.5. Зависимость температуры самовоспламенения
от состава смеси
Скорость реакции горения зависит от давления и катализаторов, поэтому температура самовоспламенения зависит также и от этих факторов (табл.1.1).
Таблица 1.1 Изменение температуры самовоспламенения в зависимости от давления
| Вещество | Тс, К при давлении р×10-5 Па: | |||||
| 1,013 | 5,065 | 10,13 | 15,18 | 20,26 | 25,23 | |
| Бензин | ||||||
| Бензол |
Катализаторы, как известно, делятся на положительные (ускоряющие) и отрицательные (замедляющие реакцию). Положительные катализаторы снижают температуру самовоспламенения, а отрицательные - повышают. Каталитическими свойствами могут обладать стенки сосуда, в котором находится горючая смесь. С увеличением каталитической активности материала стенки сосуда Тс снижается.
Температура самовоспламенения смеси горючих веществ обычно не подчиняется правилу аддитивности. Так, например, температура самовоспламенения смеси метанола и диэтилового эфира разного состава всегда ниже рассчитанной по правилу аддитивности.
Таким образом, приведенные данные показывают, что температура самовоспламенения действительно не является константой, а зависит от множества факторов. Истинное ее значение в точке С на рис.2 экспериментально можно определить только путем прямого измерения температуры. Однако современные средства измерений не позволяют пока это сделать с достаточной степенью точности, поскольку неизвестно, в какой именно точке объема горючей смеси возникает первоначальный очаг горения. Тепловая теория самовоспламенения подсказывает выход из данной ситуации. В точке касания С, с одной стороны, существует равенство тепловыделения и теплоотвода. С другой стороны, в точке С каждая функция является касательной к другой, т.е. производные по температуре от q+ и q_ также должны быть равны между собой В математической форме это будет иметь следующий вид:
Qгop×V×ko×Cгop×Cок×exp(-E/RTc)=a(T-To)-S
и для производных:
Qгop×V×ko×Cгop×Cок×exp(-E/RTc)×E/RTc2 = a×S
Разделив выражения получим:
RTc2/E = Tc - To.
Путем несложных математических преобразований из этого квадратного уравнения можно найти выражение для Тс, которое будет иметь вид:
Тс = То + RTc2 / Е
Из рис.2 видно, что при самовоспламенении смесь в сосуде нагревается от температуры То до Тс. Расчеты показывают, что разница между ними невелика. Например, для углеводородов она равна всего 30 °С.
Это обстоятельство используется на практике: за температуру самовоспламенения принимается наименьшая температура стенки сосуда, при которой происходит самовоспламенение.
В настоящее время температура самовоспламенения определена для многих веществ, и ее можно найти в справочной литературе. Однако не для всех. Для алканов, ароматических углеводородов и алифатических спиртов она может быть приближенно рассчитана по условной средней длине молекулы соединения. Метод расчета будет изучаться на практическом занятии.
Как оговаривалось ранее, температура самовоспламенения не является константой для конкретного вещества, а зависит от множества факторов таких как:
1. Объем реакционного сосуда (при увеличении объема реакционного сосуда температура самовоспламенения уменьшается);
2. Геометрическая форма сосуда (чем меньше удельная поверхность, т.е. отношение площади поверхности к объему сосуда [S/V], тем температура самовоспламенения ниже. При этом, среди всех геометрических форм сосудов при равных объемах, наименьшая температура самовоспламенения будет в сосуде в виде шара);
3. Состав горючей смеси, т.е. концентрация горючего и окислителя (график зависимости имеет вид параболы с вершиной в точке со стехиометрической концентрацией. Т.е. температура самовоспламенения смеси минимальна при стехиометрической концентрации горючего и окислителя);
4. Давление окружающей среды (с увеличением давления, температура самовоспламенения уменьшается);
5. Наличие катализаторов или ингибиторов
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1068; Нарушение авторских прав?; Мы поможем в написании вашей работы!