
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Розчини, що не містять іонів ( наприклад, водний розчин цукру, кремнезем, метану) називаються неелектролітами
Розчини, що проводять електричний струм (тобто містять іони) називають електролітами Носіями електричного заряду в електролітах є іони.
Водний розчин – електроліт
Іони, що існують у водному розчині, здатні переміщуватися в електричному полі, тобто при прикладенні до розчину різниці електричних потенціалів, через розчин буде проходити електричний струм. Цим водний розчин – електроліт – принципово відрізняється від чистої (деіонізованої) води, яка електричний струм не проводить, є діелектриком.
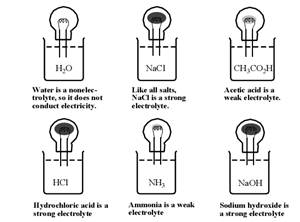
Згідно із константою дисоціації речовини у воді, розрізняють сильні та слабкі електроліти.
Процеси, що відбуваються із участю водного розчину, можна поділити на чотири групи
o Кислотно-лужні взаємодії
Прикладом може бути дисоціація вугільної кислоти
H2CO30 ↔ H+ + HCO3
o Комплексоутворення - прикладом може слугувати гідроліз ртуті
Hg2+ + H2O ↔ Hg(OH)+ + H+
o Окисно-відновні процеси у розчині чи між мінералом та розчиненими компонентами.
o Адсорбція/десорбція. Приклад: адсорбція Mn на поверхні глинистого мінералу:
ºS + Mn2+ ↔ ºS–Mn (де виразом ºS показуються сорбційні центри на поверхні мінералу)
o Розчинення/осадження, наприклад розчинення ортоклазу
KAlSi3O8 + H+ + 7H2O ↔ Al(OH)3 + K+ + 3H4SiO4
|
Дата добавления: 2014-01-07; Просмотров: 472; Нарушение авторских прав?; Мы поможем в написании вашей работы!