
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Газовые электроды
Газовый электрод представляет собой полуэлемент, состоящий из металлического проводника, контактирующего одновременно с соответствующим газом и с раствором, содержащим ионы этого газа. Конструирование газового электрода невозможно без участия проводника с электронной проводимостью. Требования к металлу в газовых электродах: 1) должен ускорять медленно устанавливающееся электродное равновесие, то есть служить катализатором электродной реакции; 2) потенциал металла в газовом электроде не должен зависеть от активности других ионов раствора, в частности, от активности собственных ионов металла; 3) должен быть инертным по отношению к другим возможным реакциям; 4) должен обеспечивать создание максимально развитой поверхности раздела между фазами, на которой могла бы протекать обратимая реакция ионизации газа. Всем этим требованиям лучше всего удовлетворяет платина, электролитически покрытая платиновой чернью (платинированная платина). Газовые электроды очень чувствительны к изменению состояния поверхности платины, особенно к отравлению ее каталитическими ядами.
Водородный электрод. Схема электрода
H+ êH2 êPt.
Электродная реакция
2Н+ + 2 е = Н2
 =
= 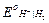 + 2,303
+ 2,303 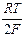 lg
lg 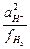 =
=
= 2,303 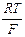 lg
lg  - 2,303
- 2,303 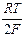 lg
lg 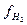
(так как 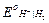 при всех Т принят равным нулю). При невысоких давлениях газообразного водорода (f ® р) летучесть можно заменить на давление:
при всех Т принят равным нулю). При невысоких давлениях газообразного водорода (f ® р) летучесть можно заменить на давление:
 = 2,303
= 2,303 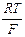 lg
lg  - 2,303
- 2,303 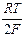 lg
lg 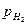 .
.
Таким образом, потенциал водородного электрода определяется не только активностью ионов Н+, но и парциальным давлением газообразного водорода, следовательно, водородный электрод (как и все газовые электроды) более сложен, чем электроды первого и второго рода, потенциалы которых зависят непосредственно от активности частиц одного сорта.
Когда парциальное давление водорода равно 1 атм, уравнение упрощается: 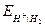 = - 2,303
= - 2,303 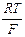 рН, то есть при определенных условиях потенциал водородного электрода дает непосредственное значение рН и, следовательно, его можно использовать как индикаторный электрод при определении рН в растворах кислот и щелочей любых концентраций, что очень существенно, так как другие индикаторные электроды (стеклянный, хингидронный, металлоксидные) можно использовать лишь в ограниченном интервале рН.
рН, то есть при определенных условиях потенциал водородного электрода дает непосредственное значение рН и, следовательно, его можно использовать как индикаторный электрод при определении рН в растворах кислот и щелочей любых концентраций, что очень существенно, так как другие индикаторные электроды (стеклянный, хингидронный, металлоксидные) можно использовать лишь в ограниченном интервале рН.
Другое важное применение газового водородного электрода: при поддержании постоянного значения рН и давления газообразного водорода его можно использовать как электрод сравнения на границе с любыми кислыми и щелочными растворами, причем диффузионный потенциал можно практически свести к нулю подбором соответствующего раствора в водородном электроде.
Кислородный электрод. Схема электрода
ОН– êО2 êPt
Электродная реакция
О2 + 2Н2О + 4 е = 4ОН–
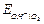 =
= 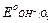 + 2,303
+ 2,303 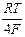 lg
lg 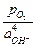 =
=
= 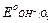 + 2,303
+ 2,303 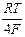 lg
lg  - 2,303
- 2,303 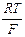 lg
lg 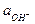 .
.
В величину 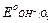 включена активность воды. При 25оС и
включена активность воды. При 25оС и  = 1 атм
= 1 атм
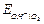 = 0,401 - 0,059 lg
= 0,401 - 0,059 lg 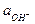 .
.
Однако реализовать обратимый кислородный электрод на практике весьма трудно. Это обусловлено способностью кислорода окислять металлы, даже платину, поэтому на основную электродную реакцию накладывается реакция, отвечающая металлоксидному электроду второго рода. Кроме того, часть кислорода восстанавливается на электроде не до ионов гидроксила, а до ионов перекиси водорода. Поэтому значения потенциала кислородного электрода, полученные опытным путем, обычно не совпадают с теоретическими, и кислородный электрод не используется на практике ни в качестве индикаторного электрода при определении рН, ни в качестве электрода сравнения, хотя теоретически и то и другое возможно.
Хлорный электрод. Реализация обратимого газового хлорного электрода Cl– êCl2 êPt связана со значительными трудностями. Теоретически электродная реакция здесь проста: Cl2 + 2 e = 2Cl–, и электродный потенциал можно описать уравнением
 =
= 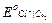 + 2,303
+ 2,303 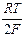 lg
lg  .
.
Однако на основной электродный процесс накладываются побочные реакции с участием хлора. Высокое положительное значение 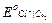 (+ 1,358 В при 25оС) затрудняет подбор устойчивого, не реагирующего с хлором материала электрода. Тем не менее при соблюдении определенных мер удалось получить опытные значения потенциалов хлорного электрода, совпадающие с теоретической величиной.
(+ 1,358 В при 25оС) затрудняет подбор устойчивого, не реагирующего с хлором материала электрода. Тем не менее при соблюдении определенных мер удалось получить опытные значения потенциалов хлорного электрода, совпадающие с теоретической величиной.
Сравнивая выражения для потенциалов газовых электродов, можно заметить, что при повышении давления соответствующего газа потенциал водородного электрода смещается в отрицательную сторону, а потенциалы кислородного и хлорного электродов – в положительную.
|
|
Дата добавления: 2014-01-07; Просмотров: 5881; Нарушение авторских прав?; Мы поможем в написании вашей работы!