
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Концентрация, моль/л
|
|
|
|
Рис. 5.2. Значения функции кислотности H0
для водных растворов кислот разной концентрации
Функция кислотности Н 0 не является универсальной характеристикой протонирующей способности растворов кислот. Это связано с несоблюдением равенства отношений
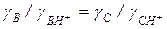
для серий индикаторов разной природы. Другую шкалу кислотности дает, в частности, функция НR, построенная по серии индикаторов, состоящих из замещенных арилкарбинолов:
 Аr(СН3)2СОН + Н+ Аr(СН3)2С+ + Н2О
Аr(СН3)2СОН + Н+ Аr(СН3)2С+ + Н2О
Для количественной характеристики способности основной среды отнимать протон у кислоты-субстрата пользуются функцией кислотности Н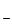 , построенной с помощью индикаторов ВН, представляющих собой замещенные С – Н-кислоты с общей формулой ArCH2CH (CN)СН3:
, построенной с помощью индикаторов ВН, представляющих собой замещенные С – Н-кислоты с общей формулой ArCH2CH (CN)СН3:
 BH + HO
BH + HO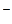 H2O + B
H2O + B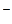 или BH B
или BH B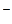 + H+ (5.45)
+ H+ (5.45)
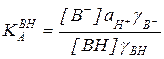
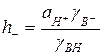
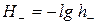
Шкала Н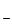 является продолжением шкалы рН в сторону повышения основности. На рис. 5.3 приведен для примера график зависимости Н
является продолжением шкалы рН в сторону повышения основности. На рис. 5.3 приведен для примера график зависимости Н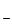 от состава и концентрации растворов оснований. Как следует из рисунка, щелочность реальных водных растворов NaOH и КОН возрастает быстрее, чем их концентрация. Это объясняют уменьшением активности воды в концентрированных растворах из-за разбавления ее щелочью и образования сольватов НО
от состава и концентрации растворов оснований. Как следует из рисунка, щелочность реальных водных растворов NaOH и КОН возрастает быстрее, чем их концентрация. Это объясняют уменьшением активности воды в концентрированных растворах из-за разбавления ее щелочью и образования сольватов НО (Н2О)n, в результате чего равновесие (5.45) сильнее сдвигается вправо.
(Н2О)n, в результате чего равновесие (5.45) сильнее сдвигается вправо.
Для кинетического описания реакций, катализируемых кислотами и основаниями, важными являются количественные данные о скоростях установления равновесий. Такие данные были получены для реакций:
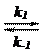 | |||
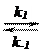 | |||
АН + Н2О Н3О+ + А В + Н2О ВН+ + НО
В + Н2О ВН+ + НО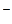
Рис. 5.3. Значения функции кислотности Н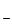 для
для
водных растворов щелочей
разной концентрации
Наибольшей константой скорости [109 - 1011 л/(моль×с)] обладают протолитические реакции у атомов О, N и S, если они протекают в термодинамически благоприятном направлении, например:
|
|
|
 Н3О+ + NH3 Н2O + NH
Н3О+ + NH3 Н2O + NH
Здесь скорость лимитируется диффузией реагентов друг к другу.
Для реакции:
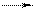 H2O + H2O H3O+ + HO
H2O + H2O H3O+ + HO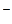
k1 = 10-6,4 л/(моль×с).
В отличие от этого, реакции С–Н-кислот и их анионов с водой, например:
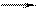 CH3NO2 + H2O
CH3NO2 + H2O 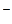 CH2NO2 + H3O+
CH2NO2 + H3O+

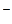 CH2NO2+ H2O CH3NO2 + HO
CH2NO2+ H2O CH3NO2 + HO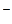
протекают на 6-10 порядков медленнее и могут оказаться лимитирующими при кислотно-основном катализе. Это объясняется необходимостью структурной реорганизации С–Н-кислот при протолитических реакциях.
Данные о скорости реакций кислот Льюиса с основаниями ограничены реакциями замещения воды основаниями во внутренней сфере ионов различных металлов. Так же как и скорости переноса протона, эти скорости меняются в очень широком интервале и зависят от природы металла и основания. Однако все они достаточно быстрые, и лишь немногие реакции (с участием Mg2+, Al3+, Fe3+) характеризуются константой скорости меньше 104 с-1.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 246; Нарушение авторских прав?; Мы поможем в написании вашей работы!