
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Напряжение поляризации (рабочее напряжение)
|
|
|
|
Параметры, определяющие ток электрода
Количество кислорода, диффундирующего к платине, и сила тока зависят от следующих параметров:
1. Парциального давления кислорода
2. Материала мембраны и ее толщины
3. Площади катода
4. Напряжения поляризации
5. Температуры
6. Скорости потока жидкости у поверхности электрода.
Напряжение поляризации Uп (рабочее напряжение) выбирается из условия, что кислород полностью восстанавливается, в то время как другие газы не оказывают влияния на величину тока. Рабочее напряжение следует стабилизировать в максимально возможной степени. Кроме стабилизации Uп важным является выполнение следующих условий:
- электрическое сопротивление пленки электролита не должно превышать определенной величины, чтобы избежать значительного скачка напряжения на нем
- площадь анода должна быть достаточно большой для того, чтобы избежать его поляризации током электрода.
Температурная зависимость тока электрода при постоянном парциальном давлении кислорода определяется исключительно температурной зависимостью проницаемости мембраны, а не параметров электрохимический реакции.
Зависимость показаний от скорости потока жидкости. Для большинства кислородных электродов сила тока в растворе без перемешивания всегда ниже силы тока в потоке жидкости. Потребление кислорода электродом приводит к обеднению приповерхностного слоя на наружной стороне мембраны (снижению концентрации кислорода). В зону обеднения кислород из раствора поступает за счет диффузии. Если ток электрода велик, то поступление кислорода не обеспечивается диффузией. Это приводит к снижению тока, по сравнению с тем, который должен был бы соответствовать условиям в растворе. В перемешиваемых же растворах кислород поступает к поверхности не только за счет диффузии, но также и в результате доставки с потоком жидкости. В этом случае снимается обеднение/истощение приповерхностного слоя кислородом. Значительная зависимость силы тока от скорости перемешивания жидкости наблюдается в основном у электродов с большой площадью катода, тонкими и высокопроницаемыми мембранами, т.е. в тех случаях, когда ток электрода значителен.
В электродах фирмы Ingold, имеющих тонкую тефлоновую мембрану, определяющую величину тока, на поверхности расположена относительно толстая силиконовая мембрана. Этот материал характеризуется высокой проницаемостью для кислорода и действует поэтому как резервуар, накапливающий кислород. Двойная композиции мембраны "силикон-тефлон" является эффективным буфером, компенсирующим возмущения, вызванное нестабильностью гидродинамического потока.
Время ответа. Время ответа Tо кислородных электродов определяется толщиной и типом газопроницаемой мембраны:
x2/D,
где х – толщина мембраны, D – коэффициент диффузии.´Tо = const
Тонкие и высокопроницаемые мембраны позволяют получить электроды с малым временем ответа.

| Рис. 11. Схема работы электрода Кларка (глюкозного биосенсора): 1 - исследуемый раствор, 2 - корпус биосенсора, 3 - внешняя мембрана, 4 - слой глюкозооксида, 5 - внутренняя газопроницаемая мембрана, 6 - платиновый электрод (проволока) для восстановления кислорода, 7 - усилитель сигнала, 8 - самописец (дисплей, цифровой или световой указатель и т. д.) |
Таблица. Характеристики некоторых глюкозоанализаторов. Прим.:Во всех глюкозоанализаторах использован фермент глюкозоксидаза. * Дополнительно используется медиатор для переноса электронов.
| Фирма, прибор | Диапазон концентраций, ммоль/л | Объем пробы, мкл | Частота измерений, проб/ч | Погрешность, % | Стабильность |
| Неавтоматизированные анализаторы | |||||
| «Эксан Г» Россия | 0,5...30 | ||||
| Yellow Springs Instruments (США), модель 23А | 0,5...50 | 300 измерений | |||
| Seres (Франция), Enzymat | 1...22 | 500 измерений | |||
| Solea-Tacussel (Франция), глюкозный электрод | 0,0001...1,0 | 1000 измерений | |||
| Hoffman la Roshe (Швейцария) Глюкозоанализатор 5410* | 2,.5...27,5 | t изм 60 с | 1,5 | 8 нед. | |
| Fuji Electric (Япония), Gluco 20A | 0...27 | 500 измерений | |||
| Analytical instruments (Япония) Glucorder-E | 0...55,5 | 20...40 | 120...150 | 2,0 | |
| Автоматические проточные анализаторы | |||||
| Daiichi (Япония), Auto&Stat GA1110 | 1...40 | 100...250 | 1.0 | ||
| Карлов университет (Чехия) | 0.006...5,0 | 3,5 | 30 дн. | ||
| Приборы непрерывного действия | |||||
| Life Science Instr, Div. Miles (США, Биостатор GCIIS | до 27,5 | 2 мин | 50 ч | ||
| Университет г. Осака, медицинский факультет | 2,85...22,0 | 3 дн. |
б) Определение концентрации этилового спирта. В основу функционирования ферментных электродов первого поколения, например электрода для определения этилового спирта, была положена природная ферментативная реакция:
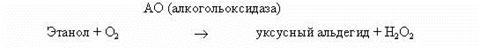
Реакция окисления этанола в присутствии алкогольдегидрогеназы: этанол + O2 + Алкогольдегидрогеназа -> CH3CHO + NADH + H+.
Аналогичный пример для детекции глюкозы уже был использован ранее для иллюстрации применения различных принципов преобразования сигнала при создании биосенсоров. В данном случае эта реакция приведена для демонстрации принципа использования электрода Кларка для регистрации концентрации этанола в сенсоре на основе алкогольоксидазы (АО, фермент класса оксидаз) и измерения потребления кислорода – Рис. ниже. В процессе окисления спирта происходит снижение уровня кислорода в зоне иммобилизованного фермента; степень снижения определяется концентрацией этанола и является основой для его количественной оценки.
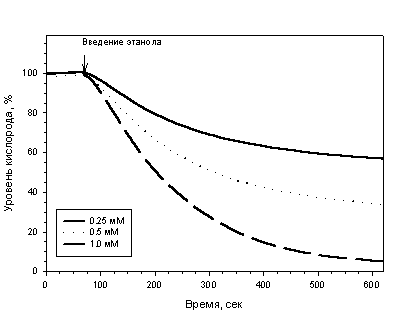
| Рис. Зависимость сигналов ферментного сенсора от времени для различных концентраций этанола (кюветный способ измерения, показаны сигналы для концентраций этанола 0.25, 0.5 и 1.0 мМ). При повышении концентрации спирта в пробе возрастает степень снижения уровня кислорода. При высокой концентрации (1 мМ) уровень кислорода в рецепторном элементе снижается практически до нуля. |
в) Оценка действия целлюлозных ферментов. Для измерения активности целлюлаз, катализирующих разложение целлюлозы применяются амперометрические ИП с вращающимися платиновыми электродами, запаянными в стеклянную трубку (скорость вращения около 600 об/мин). При понижении вязкости растворов целлюлозных полимеров ток ИП увеличивается.
г) Амперометрия применяется также для измерения концентрации аминокислот.
Перекисный электрод. Возможно применение ион-селективного электрода для определения пероксида водорода. Такой метод чувствительнее в 100–1000 раз, чем применение кислородного электрода.
Распространенным типом амперометрического преобразователя является электрод для измерения содержания перекиси водорода (Н2О2) в среде. Перекись является неустойчивым соединением и на свету спонтанно разлагается с образованием воды и молекулярного кислорода: 2H2O2 -> 2H2O + O2 (спонтанная реакция разложения перекиси на свету). Измерение перекиси производится электрохимически. Известны два процесса электрохимической трансформации молекулы перекиси. При подаче на электрод потенциала + 0,682 В относительно присутствующего в растворе электрода сравнения происходит окисление перекиси водорода: H2O2 à O2 + 2H+ + 2e-. Регистрация данной реакции является основой измерения в большинстве биосенсоров, в состав которых входят ферменты, генерирующие перекись. При потенциале + 1.77 В происходит восстановление перекиси в соответствии с реакцией: H2O2 +2H+ + 2e- -> 2H2O.
Можно выделить несколько причин применения перекисного электрода при конструировании биосенсоров. Перекись образуется в результате окисления органических соединений оксидазами, т.е. является продуктом реакции окисления. Первая причина состоит в том, что при прочих равных условиях измерение продукта реакции позволяет более корректно описать количественно процесс биохимического окисления с точки зрения выполнения дальнейшего анализа, чем регистрация потребления одного из реагентов процесса окисления (это положение является общей точкой зрения, вместе с тем, не бесспорной). В данном случае как контрпример подразумевается регистрация потребления кислорода, как одного из реагентов биохимической реакции. Вторая, существенная причина, состоит в том, что в различных образцах содержание кислорода может варьировать, что потенциально приводит к ошибкам измерения; с этой точки зрения более правильным является регистрация образующейся перекиси водорода. Далее, достаточно существенным аргументом в пользу применения перекисных электродов является то, что разработаны электроды, которые по конструкции в большинстве случаев значительно проще, чем кислородные. Так, суть перекисные электроды не требуют их заполнения электролитом, не требуют использования специальных мембран, т.е. для функционирования перекисного электрода наличие мембраны как таковой не требуется, если же на основе перекисного электрода формируют биосенсор, то на электроде размещают лишь мембрану, содержащую иммобилизованный биоматериал и ее назначением является фиксация биоматериала. Методическая сторона вопроса всегда является важной при создании сенсоров. В этой связи
Схематически вид перекисного электрода для регистрации реакции окисления глюкозы приведен на рис. ниже. Присутствующая в пробе глюкоза окисляется глюкозооксидазой. Продуктом реакции является глюконовая кислота и перекись водорода. Перекись детектируется электрохимически перекисным электродом. Количество образующейся перекиси пропорционально концентрации глюкозы, в связи с чем сигнал, генерируемый перекисным электродом, пропорционален концентрации глюкозы в образце.
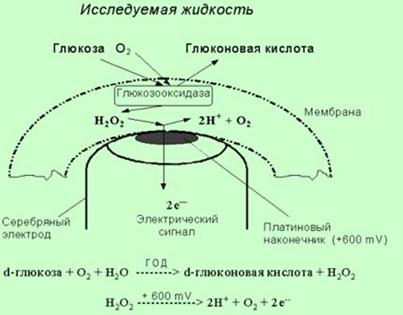
Рис. Амперометрический биосенсор на основе перекисного электрода для регистрации глюкозы.
Отметим еще одну существенную причину, позволяющую отдавать предпочтение применению перекисных электродов – современная технология изготовления тонкопленочных структур, используемая для производства клавиатур компьютеров, калькуляторов и т.д. - позволяет использовать ее основные принципы и устройства для выпуска перекисных электродов крупными партиями, что значительно снижает их стоимость. Электроды, производящиеся по данной технологии, носят название "электроды, полученные матричной печатью" (английская терминология – screen printed electrodes). Имеется еще один существенный довод в пользу применения перекисных электродов, полученных матричной печатью, в биосенсорах – существующие технологии позволяют встраивать биологический материал - ферменты, клетки - в состав электрода непосредственно в процессе технологического цикла его изготовления. Это является крайне важным моментом в изготовлении биосенсоров и приводит к производству высокостабильных, сохраняющихся длительное время полуфабрикатов, пригодных для быстрого изготовления биосенсоров. Структура электрода, получаемого матричной печатью, схематически показана на рис. ниже.
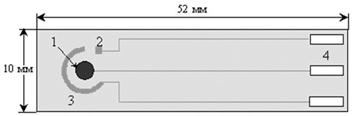
Рис. Схематическое представление электрода, изготовленного матричной печатью. 1 – измерительный электрод, формируется нанесением проводящего материала на диэлектрическую подложку и содержит иммобилизованный биоматериал (в качестве проводящего материала используется золото, платина, графит); 2 – электрод сравнения, Ag/AgCl электрод (площадь 1 мм2); 3 – вспомогательный электрод (Ag); 4 – контакты для подключения электрода в измерительную цепь.
Суммируя достоинства перекисного электрода, как преобразователя биосенсоров, отметим, что указанное связано с простотой метода встраивания фермента в электрод при его изготовлении, создании миниатюрных электродов, простотой конструкции и низкой стоимостью при изготовлении крупных партий.
Наряду с достоинствами способ регистрации биохимических реакций по детекции перекиси водорода имеет определенные недостатки. 1) В биологических препаратах присутствуют вещества, которые влияют на выход продукта реакции H2О2 (аскорбиновая кислота, мочевая кислота и т. п.). Для сведения к минимуму этого эффекта иногда мембранам электродов сообщают заряд, отталкивающий мешающие вещества. 2) Из-за отсутствия защитной мембраны электрода зачастую происходит загрязнение платины, из которой формируют измерительный перекисный электрод, что также снижает практическую ценность этого типа преобразователя.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2903; Нарушение авторских прав?; Мы поможем в написании вашей работы!