
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Дегазация чугуна
|
|
|
|
Дегазацию жидкого чугуна осуществляют, прежде всего, для удаления из него избыточного водорода. Но этот процесс сопровождается также рафинированием расплава от кислорода. Последнее в основном связано с удалением из расплава химически связанного кислорода в виде неметаллических (оксидных) частиц.
Для дегазации чугуна опробованы различные методы: продувка инертными газами (аргоном и азотом), вакуумирование, ультразвуковая обработка и др. Наиболее технологичным и достаточно эффективным является метод продувки расплава аргоном или азотом в ковше. При продувке достигается комплексный эффект обработки, который включает рафинирование чугуна от растворенных газов и неметаллических включений, а также гомогенизацию расплава по химическому составу и температуре.
При продувке чугуна инертным газом достигаемый эффект дегазации (∆[%H]∑) представляет собой суммарный результат протекания трех процессов (Рис. 3.7.8) [3]:
∆ [%H]∑ = ([%H]нач – [%H]кон)∙100/[%H]нач= ∆[%H]F+(∆[%H]Ar + ∆ [%H]CO), (3.7.28)
где ∆[%H]F – вклад в эффект дегазации процесса (I) прямого выделения водорода через открытую поверхность (зеркало) расплава в ковше;
∆[%H]Ar - вклад в эффект дегазации процесса (II) экстракции водорода в пузырьки вдуваемого газа (аргона или азота);
∆[%H]CO - вклад в эффект дегазации процесса (III) дополнительной экстракции водорода пузырьки монооксида углерода.
Монооксид углерода СО образуется в результате протекания реакции углеродного раскисления чугуна [C] + [O] = {CO}. Этому способствует формирование в объеме расплава пузырьковых полостей вдуваемого газа (Ar или N2), в которых парциальное давление моноокисда углерода РСО ≈ 0. Эта реакция реализуется на поверхности пузырьков, поэтому выделяющийся монооксид образует газовую смесь с вдуваемым газом и фактически увеличивает объем (расход) рафинирующего газа до V∑ = VAr + VCO.
|
|
|
Эффект дегазации, обусловленный прямой экстракцией водорода с зеркала расплава в ковше, можно оценить по выражению (3.7.29):
∆ [%H]F =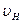 ∙ FMe-Газ ∙ tобр =
∙ FMe-Газ ∙ tобр = 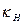 ∙ [%H]2 ∙ FMe-Газ ∙ tобр (3.7.29)
∙ [%H]2 ∙ FMe-Газ ∙ tобр (3.7.29)
где 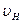 - скорость удаления водорода с единицы поверхности раздела «металл-газ», %/(м2 ∙ с);
- скорость удаления водорода с единицы поверхности раздела «металл-газ», %/(м2 ∙ с);
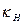 - константа скорости, 1/(
- константа скорости, 1/(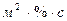 );
);
FMe-Газ, ковш – площадь зеркала жидкого чугуна в ковше, м2;
tобр – продолжительность продувки чугуна в ковше, с.
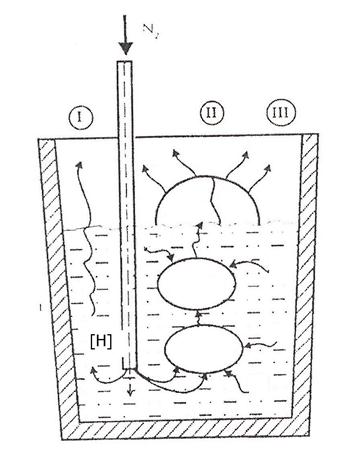
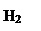
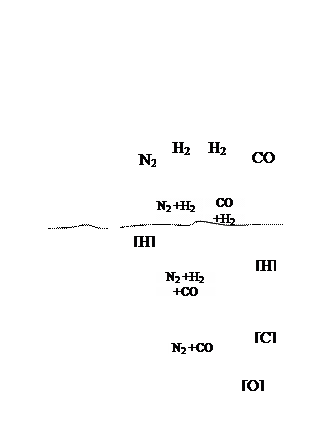
Рис. 3.7.8. Схема выделения водорода из жидкого чугуна.
Количество водорода, удаляемого с пузырьками вдуваемого газа и образующегося монооксида углерода, эквивалентно их расходу. Начальные и конечные концентрации водорода в чугуне связаны с расходом рафинирующего газа следующим соотношением:
VAr = 1/η ∙112 ∙ PAr ∙ (KH / fH) 2 ∙ (1/[H]кон – 1/ [H]нач), (3.7.30)
VAr = 1/η ∙112 ∙ PCO ∙ (KH / fH) 2 ∙ (1/[H]кон – 1/ [H]нач), (3.7.31)
где VAr – удельный расход вдуваемого газа, м3/т;
η - коэффициент полезного действия продувки;
PAr – давление вдуваемого газа, 10-5 Па;
PCO – давление вдуваемого газа, 10-5 Па;
KH – константа равновесия реакции ½ Н2 = [H], lg KH = - 1900 / T – 4,077;
fH – коэффициент активности водорода в чугуне;
[H]кон и [H]нач –содержание водорода в чугуне в конце и вначале продувки, %.
Оценки показывают [3], что общий эффект дегазации при кратковременной (≈ 3-5 мин) продувке составляет 20-40 %. При этом различные процессы вносят разный вклад на эффект дегазации при продувке чугуна в ковше:
а) доля водорода ∆ [%H]F, удаляющегося за счет прямого выделения через открытое зеркало расплава составляет 35-45 % (отн.) от общего эффекта дегазации;
б) доля водорода ∆ [%H]Ar, удаляющегося с пузырьками вдуваемого газа, составляет 50-60 % (отн.).
|
|
|
в) доля водорода (∆[%H]CO, дополнительно удаляющегося с пузырьками вдуваемого газа за счет его разбавления монооксидом углерода, не превышает 5-7 % (отн.).
Коэффициент полезного действия η при продувке чугуна составляет 0,3 – 0,4. Это обусловлено, прежде всего, низкой скоростью экстракции водорода 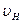 , которая из-за относительно низкой температуры обработки чугуна протекает в кинетическом режиме (См. Раздел 3.7.2). Кроме того, значение η ограничено кратковременностью контакта расплава с пузырьками вдуваемого газа вследствие быстрого их всплывания в ковшах небольшой вместимости.
, которая из-за относительно низкой температуры обработки чугуна протекает в кинетическом режиме (См. Раздел 3.7.2). Кроме того, значение η ограничено кратковременностью контакта расплава с пузырьками вдуваемого газа вследствие быстрого их всплывания в ковшах небольшой вместимости.
Эффективность дегазации жидкого чугуна при продувке его инертным газом может быть повышена, если обеспечить увеличение поверхности и длительности контакта расплава с вдуваемым газом. Обе эти задачи решаются при введении вдуваемого газа в расплав в виде мелких газовых пузырьков, имеющих высокую удельную поверхность и малую скорость всплывания. Для этого рафинирующий газ инжектируют в жидкий чугун в виде тонких высокоскоростных струй, диспергирующихся в расплаве на множество мелких пузырьков.
3.7.6. Раскисление чугуна
Растворенный кислород, как отмечалось выше, оказывает отрицательное влияние на формирование структуры чугуна, дезактивируя имеющиеся центры его кристаллизации. Поэтому отрицательное влияние растворенного кислорода нейтрализуют путем перевода его в химически связанное состояние. Этот процесс называют раскислением.
Для жидкого железа раскислителем может быть любой элемент, имеющий большее в сравнении с ним термодинамическое сродство с кислородом. Но в жидком чугуне содержатся углерод (до 3,0-3,5 %), кремний (до 1.5-2.5 %) и марганец (до 0,6-1,1 %), которые сами являются раскислителями. Вследствие этого обычно жидкий чугун представляет собой достаточно хорошо раскисленный расплав, поэтому его, как правило, специально не раскисляют. Однако, в некоторых случаях для предотвращения дефектности отливок (См. Раздел 3.7.4) необходимо обеспечить глубокое раскисление чугуна. Кроме того, процесс раскисления сопутствует процессу модифицирования чугуна.
Так, при производстве отливок из серого чугуна расплав подвергают графитизирующему модифицированию. Для этого используют ферросилиций ФС75, силикокальций или комплексные сплавы на их основе, дополнительно содержащие такие сильные элементы-раскислители как Ca, Ba, Mg, Al, Ti, Zr, Ce и др. [1]. Соответственно, содержание растворенного кислорода в немодифицированном или модифицированном только ферросилицием чугуне определяется (см. Раздел 3.2) преимущественно кремний-углеродным комплексом. В других случаях степень раскисленности чугуна определяется остаточным содержанием в нем наиболее сильного раскислителя R (Ca, Ba, Mg, Al, Ti, Zr, Ce и др.).
|
|
|
При производстве отливок из высокопрочного чугуна для сфероидизации графитной фазы расплав обрабатывают модификаторами, содержащими Mg, Ca, Y и Ce (РЗМ) [1], которые являются сильными раскислителями. Поэтому степень раскисленности расплава высокопрочного чугуна с шаровидным и вермикулярным графитом определяется остаточным содержанием сфероидизирующих элементов R (Mg, Ca, Y, Ce и др. РЗМ).
При производстве отливок из ковкого чугуна для предотвращения выделения графита при первичной кристаллизации и сокращения продолжительности отжига расплав, наряду с Bi, Sb, S и Te, модифицируют элементами, имеющими большое сродство к кислороду - Al и B, а также Mg и Y (для сфероидизации графита отжига) [1]. Вследствие этого степень раскисленности расплава ковкого чугуна также определяется остаточным содержанием в нем элементов модификаторов R (Al, B, Mg, Y и др.).
Термодинамика процесса раскисления жидкого чугуна различными элементами описывается общим уравнением:
m [R] + n [O] = (RmOn) (3.7.32)
Из выражения константы равновесия данной реакции получаем:
lg [%O] = 1/n (- lg 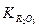 – m lg
– m lg 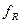 - m lg [%R] – n lg
- m lg [%R] – n lg 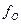 , (3.7.33)
, (3.7.33)
где [%O] – массовая доля кислорода, %;
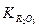 - константа равновесия реакции (3.7.32);
- константа равновесия реакции (3.7.32);
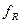 и
и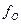 - коэффициенты активности элементов - раскислителей R (Ca, Ba, Mg, Al, Ti, Zr, Ce и др.) и кислорода в чугуне соответственно, численные значения которых определяются выражениями:
- коэффициенты активности элементов - раскислителей R (Ca, Ba, Mg, Al, Ti, Zr, Ce и др.) и кислорода в чугуне соответственно, численные значения которых определяются выражениями:
lg 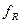 =
= 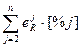 и lg
и lg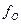 =
=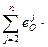 [% j ] ; (3.7.34)
[% j ] ; (3.7.34)
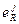 - параметры взаимодействия элемента R с компонентами чугуна j (C, Si, Mn, S, P и легирующими элементами) первого порядка;
- параметры взаимодействия элемента R с компонентами чугуна j (C, Si, Mn, S, P и легирующими элементами) первого порядка;
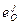 - параметры взаимодействия кислорода с компонентами чугуна j первого порядка.
- параметры взаимодействия кислорода с компонентами чугуна j первого порядка.
|
|
|
В табл. 3.7.5 приведены значения констант реакции раскисления (3.7.32) для различных элементов - раскислителей R, а в табл. 3.7.6 и 3.7.7 – значения параметров взаимодействия 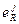 и
и 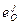 .
.
Таблица 3.7.5. Температурная зависимость констант реакций раскисления (3.7.32) для различных элементов-раскислителей R
| Реакция раскисления | Значения коэффициентов A и B зависимости lg K = A/T + B | Примечание | |
| [Si] + 2 [O] = (SiO2) | 30 720 | - 11,76 | [Si] > 0,2 % |
| [C] + [O] = {CO] | 1 168 | 2,07 | |
| 2 [Al] + 3 [O] = (Al2O3) | 64 900 | - 20,63 | |
| [Ti] + 2 [O] = (TiO2) | 30 900 | - 10,40 | [Ti] < 0,01 % |
| 3 [Ti] + 5 [O] = (Ti3O5) | 87 170 | - 31,08 | [Ti] = 0,01 – 0,2 % |
| 2 [Ti] + 3 [O] = (Ti2O3) | 28 950 | - 7,42 | [Ti] = 0,2 – 4 % |
| [Ti] + [O] = (TiO) | 17 860 | - 6,55 | [Ti] > 5 % |
| [Ca] + [O] = (CaO) | 33 865 | - 7,60 | |
| [Ba] + [O] = (BaO) | 35 000 | - 10,33 | |
| [Mg] + [O] = (MgO) | 24 890 | - 7,3 | |
| 2 [Ce] + 3 [O] = (Ce2O3) | 76 000 | - 21,00 | |
| 2 [La] + 3[O] = (La2O3) | 77 300 | - 20,79 | |
| 2 [Y] + 3 [O] = (Y2O3) | 72 000 | - 17,58 | |
| [Mn] + [O] = (MnO) | 15 200 | - 6,78 | |
| 2 [V] + 3 [O] = (V2O3) | 42 610 | - 16,86 | [V] > 0,3 % |
| 2 [Cr] + 3 [O] = (Cr2O3) | 43 140 | - 18,63 | |
| [Nb] + 2 [O] = (NbO2) | 28 780 | - 11,83 | [Cr] = 6 – 16 % |
| [Zr] + 2 [O] = (ZrO2) | 43 340 | - 12,07 | [Nb] > 0,2 % |
| [Fe] + [O] = (FeO) | 6 317 | - 2,734 |
Таблица 3.7.6. Параметры взаимодействия элементов R с компонентами чугуна, 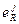
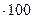
| Элемент R | Компоненты чугуна «j» | ||||||||||
| Cх | Si | Mn | Ni | Cu | Co | Mo | Cr | V | P | S | |
| Al | 0,34 | 0,56 | - | - | - | - | - | - | - | - | |
| B | 0,90 | 7,8 | - | - | - | - | - | - | - | - | 4,8 |
| C | 4,9 | - 1,2 | 1,2 | 1,6 | 0,76 | - 0,83 | - 2,4 | - 7,7 | 5б1 | 4,6 | |
| Ca | - 5,1 | - 9,7 | - | - 4,4 | - | - | - | - | - | - | - |
| Ce | - 43 | 0,21 | - | - | - | - | - | - | - | - | |
| Cr | - 3,70 | - 0,43 | - | 0,02 | 1,6 | - 1,9 | 0,18 | - 0,03 | - | - 5,3 | - 2 |
| La | - 6,60 | - | - | - | - | - | - | - | - | - | - |
| Mg | 4,70 | - 0,04 | - 2,6 | - | - | - | 0,83 | - | - | - 138 | |
| Mn | - 2,7 | - | - | - | - | - | - | - 0,35 | - 4,8 | ||
| Mo | - 3,7 | - | - | - | - | - | - | - 0,03 | - | - | - 0,05 |
| Si | 4,90 | 0,2 | 0,5 | 1,4 | - | - | - 0,03 | 2,5 | 5,6 | ||
| Ti | - | - | - | 0,009 | - | - | - | 0,022 | - | - | - 11 |
| V | -4,90 | 4,2 | - | - | - | - | - | - | 1,5 | - | - 2,8 |
| Zr | - | - | - | - | - | - | - | - | - | - | - 16 |
х ) Для насыщенного по углероду раствора
Таблица 3.7.7. Параметры взаимодействия кислорода 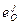
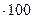 с компонентами чугуна
с компонентами чугуна
| J | Al | B | C | Ca | Ce | Co | Cr | Cu | La | Mg |
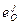
| - 390 | - 260 | - 45 | - 6180 | - 57,5 | 0,8 | - 4 | - 1,3 | - 57 | - 198 |
Таблица 3.7.7. (Продолжение)
| j | Mn | Mo | Ni | O | P | S | Si | Ti | V | Zr |
| - 2,1 | 0,35 | 0,6 | - 20 | - 13,3 | - 13,1 | - 60 | - 30 | - 44 |
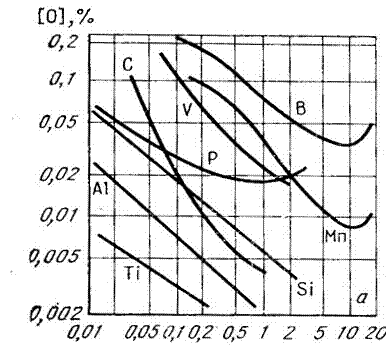
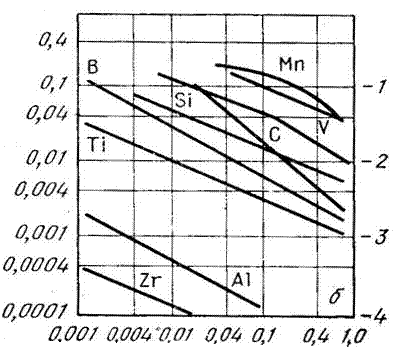
На рис. 3.7.9 показана раскислительная способность элементов в чистом железе и влияние растворенных элементов на активность в нем кислорода. Наибольшей раскислительной способностью отличаются бор, титан, алюминий и цирконий. Более высокую по сравнению с титаном и алюминием рскислительную способность имеют Ca, Ba, Mg и РЗМ (Ce, La, Y).
R, %
а)
 a [O] lg a [O]
a [O] lg a [O]
aR
б)
Рис. 3.7.9. Раскислительная способность элементов в чистом железе (а)
и влияние растворенных элементов на активность кислорода (б).
Процесс раскисления жидкого чугуна согласно реакции (3.7.32) протекает с выделением неметаллической фазы RmOn. Последнее происходит через формирование в жидком металле центров (зародышей) кристаллизации. Такие зародыши могут иметь гомогенную или гетерогенную природу. В том и другом случае для начала процесса необходима движущая сила, которой для реакции раскисления (3.7.32) является степень химического пересыщения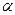 :
:
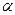 =
= 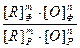 (3.7.35)
(3.7.35)
где индексами “ф” и “р” обозначены фактические и равновесные содержания растворенных в жидком металле раскислителя R и кислорода, %.
Показано, что для зарождениея неметаллической фазы RmOn параметр 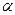 должен составлять величину порядка 10-100 и более. Однако фактически центры кристаллизации зарождаются и при меньших значениях степени химического пересыщения. Это обусловлено тем, что в начале процесса зародыши представляют собой неметаллическую фазу, сильно обогащенную оксидом железа (FeO)x(RmOn)(1-x). Со временем значение «x» уменьшается, доля FeO снижается и состав выделяющейся неметаллической фазы становится близким к равновесному. Процесс роста неметаллической фазы происходит при меньшей степени пересыщения расплава. Наряду с ростом каждой неметаллической частицы происходит и укрупнение их за счет взаимного столкновения в результате переноса частиц по различным траекториям под действием термо-конвективных, гравитационных, центробежных и прочих сил. Сформировавшиеся неметаллические частицы всплывают и ассимилируются со шлаком или остаются в расплаве и проявляются затем в отливках в виде оксидных неметаллических включений.
должен составлять величину порядка 10-100 и более. Однако фактически центры кристаллизации зарождаются и при меньших значениях степени химического пересыщения. Это обусловлено тем, что в начале процесса зародыши представляют собой неметаллическую фазу, сильно обогащенную оксидом железа (FeO)x(RmOn)(1-x). Со временем значение «x» уменьшается, доля FeO снижается и состав выделяющейся неметаллической фазы становится близким к равновесному. Процесс роста неметаллической фазы происходит при меньшей степени пересыщения расплава. Наряду с ростом каждой неметаллической частицы происходит и укрупнение их за счет взаимного столкновения в результате переноса частиц по различным траекториям под действием термо-конвективных, гравитационных, центробежных и прочих сил. Сформировавшиеся неметаллические частицы всплывают и ассимилируются со шлаком или остаются в расплаве и проявляются затем в отливках в виде оксидных неметаллических включений.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2551; Нарушение авторских прав?; Мы поможем в написании вашей работы!