
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Примеры построения названий по систематической номенклатуре
|
|
|
|
КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Резонансная стабилизация.
Резонансная стабилизация.
Стерический фактор стабилизации.
Стабилизация интермедиатов.
· Свободные радикалы.
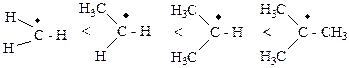

· Карбкатионы, карбанионы.
Индуктивная стабилизация (газовая фаза)

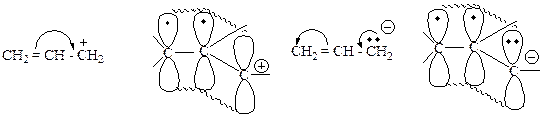
Классификация ( лат. classis – разряд, facere – делать) – распределение органических соединений по рядам, группам, классам в зависимости от их классификационных признаков.
Существующая классификация органических соединений основана, прежде всего, на структуре углеводородного скелета и характере функциональных групп. Классификацию органических соединений по основным признакам можно представить в виде схемы (рис.19).
Первым классификационным признаком является структура углеродного скелета углеводородного фрагмента молекулы. По этому признаку органические соединения делятся на следующие ряды:
· ряд ациклических соединений;
· ряд карбоциклических соединений;
· ряд гетероциклических соединений.
Ациклические соединения [гр. a…, an – частица отрицания] – органи-ческие соединения, в молекулах которых отсутствуют циклы и все атомы углерода соединены между собой в прямые или разветвленные открытые цепи. Иногда их называют алифатическими (гр. alefair – жир), поскольку к этому классу относят жиры и жирные кислоты а также алициклические соединения – циклоалканы, циклоолефины, циклодиены, циклодиины.

Рисунок 19 – Основные классы органических соединений
Структура углеводородного скелета может быть линейной и замкнутой в цикл. Прямая цепь углеродных атомов – цепь последовательно соединенных атомов. Разветвленная цепь углеродных атомов – цепь непоследовательно соединенных атомов: от средних атомов прямой цепи отходят прямые цепи.
|
|
|
Различают две основные группы ациклических соединений:
· насыщенные (предельные), у которых в углеводородном фрагменте все атомы углерода связаны между собой только простыми связями (1);
· ненасыщенные (непредельные), у которых между атомами углерода в углеводородном фрагменте, кроме простых (одинарных) связей, имеются также двойные или тройные связи.
Циклические соединения подразделяются на карбоциклические, циклы которых состоят только из атомов углерода, и гетероциклические, в состав циклов которых, кроме атомов углерода входят атомы других элементов – гетероатомы (O, N, S и др. ).
Карбоциклические соединения – органические соединения, характери-зующиеся наличием колец (циклов) из атомов углерода. Карбоциклические соединения подразделяются на:
· алициклические соединения;
· ароматические соединения.
Гетероциклические соединения – органические соединения, в цикле которых, кроме атомов углерода, содержатся гетероатомы, способные образовать не менее двух ковалентных связей (N, O, S).
Вторым классификационным признаком является электронное строение молекулы. По этому признаку органические соединения подразделяются на:
· алифатические соединения
· ароматические соединения
Третьим классификационным признаком является характер функциональной группы, определяющей функциональный класс.
Функциональный класс – группа соединений, объединяемых общей функциональной группой.
При замене в углеводороде (R–H) атомов водорода на другие атомы или функциональные группы (Х) образуются новые классы органических соединений (R–Х), характер которых определяют функциональные группы.
Функциональная группа – гетероатом или группа атомов неуглеводо-родного характера, определяющих принадлежность к определенному функциональному классу и обуславливающая важнейшие свойства этого класса (табл. 6).
|
|
|
Таблица 6 – Функциональные производные углеводородов
| Функциональная группа | Название группы | Название класса | Общая формула |

| функциональной группы нет | алканы | СnH2n+2 |
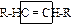
| двойная связь (усл. функция) | алкены | СnH2n |

| тройная связь (усл. функция) | алкины | СnH2n-2 |

| функциональной группы нет | арены | СnH2n-6 |
| Hal– (F–,Cl–,Br–,I–) | галогено – | галогениды | R–Hal |
| OH– | гидрокси – | спирты | R–OH |
| OR– | алкокси – | простые эфиры | R–OR |
| –O– | эпокси – | эпокси | R–O–R |
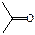
| карбонильная | альдегиды, кетоны | 
|
| –COOH | карбоксильная | карбоновые кислоты | R–COOH |
| Продолжение таблицы 6 | |||
| –COOR | сложноэфирная | сложные эфиры | R–COOR |
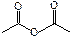
| ангидридная | ангидриды кислот | 
|
| –O–O– | пероксидная | пероксиды | R–O–O–R |

| карбонилгалогенидная | галогенангидриды кислот | 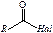
|

| карбамидная | амиды кислот | 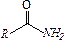
|
| –NH2 | амино – | первичные амины | R–NH2 |
| –NH– | имино – | вторичные амины | R–NH–R |
| >N– | аза – | третичные амины | R3N |
| –NO2 | нитро – | нитросоединения | R–NO2 |
| –C≡N | карбонитрильная (циано –) | нитрилы (цианиды) | R–C≡N |
| –NH–NH2 | гидразино – | гидразины | R–NH– NH2 |
| –N=N– | азо – | азосоединения | R–N=N–R |
| –N+≡N | диазо – | диазосоединения | R–N+≡N |
| –SH | тиоспиртовая (сульфгидридная) | тиолы (меркаптаны) | R–SH |
| –SR | тиоэфирная (алкилтио –) | тиоэфиры (сульфиды) | R–SR |
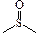
| сульфоксидная | сульфоксиды | 
|
| –SO3H | сульфо – | сульфокислоты | R–SO3H |
| Э (S, N, O …) | элементо – | элементорганические соединения | R–Э |
| Me (Na, Li …) | металло – | металлорганические соединения | R– Me |
Монофункциональные соединения – соединения с одной функциональной группой, например:

Кроме монофункциональных углеводородов, имеются самые разнообразные полифункциональные производные с несколькими одинаковыми или разными функциональными группами.
Гомофункциональные соединения – соединения с несколькими одинаковыми функциональными группами, например:

Гетерофункциональные соединения – соединения с несколькими разными функциональными группами, например:

Гомологический ряд [гр. homologia – согласие] – группа родственных органических соединений с одинаковыми функциональными группами и однотипной структурой, отличающихся между собой на одну или несколько метиленовых групп (–СН2–) в составе углеводородного фрагмента молекулы и обладающих сходными химическими свойствами.
|
|
|
Гомологическая разность – (СН2) n, где n = 1, 2, 3 и т. д.
Изологический ряд – группа углеводородов и их производных с одинаковым числом углеродных атомов в радикале и тождественными функциональными группами, но с различной степенью ненасыщенности, т. е. с возрастающим в каждом изологическом ряду количеством кратных связей в радикале.
Изологическая разность – (2 Н) n, где n = 1, 2
Генетический ряд – группа органических соединений с одинаковым углеводородным радикалом в молекуле, но с различными функциональными группами.
Классификация органических соединений позволяет не только систематизировать многочисленные органические соединения, но и является фундаментом для создания правил построения названий любого органического соединения исходя из его классической структурной формулы.
Номенклатура органических соединений. Номенклатура (лат. nomencklatura – роспись имен) это система правил построения названия соединения. Огромное число органических соединений, сложность и многообразие их строения обуславливают сложность их номенклатуры. По мере развития органической химии было предложено несколько различных систем номенклатуры.
Исторически первой возникла тривиальная номенклатура (лат. trivialis – обыкновенный). Органические соединения получали случайные названия, в которых отражались либо природные источники получения (яблочная кислота, муравьиная кислота, винный спирт), либо заметные свойства (гремучая кислота) и т. д.
С ростом числа органических соединений появилась необходимость в разработке четких и однозначных правил их названия.
Рациональная номенклатура связывает название вещества с его строением и классом. Соединение рассматривается как продукт усложнения простейшего представителя данного класса. Рациональное название очень наглядно в случае простых соединений, однако, по мере усложнения строения возможности рациональной номенклатуры, исчерпываются.
|
|
|
Для того чтобы назвать соединение по рациональной номенклатуре необходимо:
· определить класс называемого соединения;
· выбрать в соединении основу (табл. 7);
· назвать окружающие заместители;
· составить название, начиная с названий простых заместителей к более сложным, заканчивая названием основы.
Таблица 7 – Основы рациональных названий и окончаний в систематической номенклатуре некоторых классов органических соединений
| Класс называемого соединения | Основа рационального названия | Окончание в систематической номенклатуре |
| алканы | 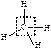 метан
метан
| -ан |
| алкены | 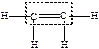 этилен
этилен
| -ен |
| алкины |  ацетилен
ацетилен
| -ин |
| спирты |  карбинол
карбинол
| -ан + ол |
| альдегиды |  уксусный альдегид
уксусный альдегид
| -ан + аль |
| кетоны | 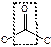 кетон
кетон
| -ан + он |
| карбоновые кислоты | 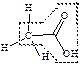 уксусная кислота
уксусная кислота
| -ан +овая кислота |
В качестве заместителей могут выступать как функциональные группы, так и углеводородные остатки. Углеводородный радикал – остаток молекулы углеводорода, из которого формально удалили один или несколько атомов водорода, оставив свободными соответственно одну или несколько валентностей.
Название углеводородных радикалов состоит из:
· префикса, указывающего на порядок соединения атомов углерода в радикале;
· корня (основы), отражающего число углеродных атомов;
· суффикса: -ил – для одновалентных радикалов;
-илен – для двухвалентных вицинальных радикалов;
-илиден – для двухвалентных геминальных радикалов;
-илидин – для трехвалентных геминальных радикалов.
Углеводородные остатки могут быть первичными, вторичными и третичными, в зависимости от типа атома углерода, имеющего свободную валентность.
Двухвалентные углеводородные остатки образуются при отнятии от углеводорода двух атомов водорода, при этом свободные валентности могут располагаться как у одного атома углерода так и у разных (табл.8).
В рациональной номенклатуре допускается несколько равноправных названий для одного соединения в зависимости от выбранной основы.
Таблица 8 – Углеводороды и углеводородные остатки
| Углеводород и его название | Углеводородные остатки | ||
| формула | Тривиальные названия | Характер радикала | |
| СnH2n+2 алкан | СnH2n+1– | алкил | |
| СH4 метан | СH3– | метил | |
| СH3–СH3 этан | СH3–СH2– | этил | первичный |
| СH3–СH2–СH3 пропан | СH3–СH2–СH2– | пропил | первичный |
| (СH3)2СН– | изо пропил | вторичный | |
| СH3–(СH2)2–СH3 бутан | СH3–СH2–СH2–СH2– | н -бутил | первичный |
| СH3–СH(СH3)–СH3 изобутан | СH3–СН(СH3)–СH2– | изо бутил | первичный |
| СH3–СН2–(СH3)СH– | вторичный бутил | вторичный | |
| (СH3)3С– | третичный бутил | третичный | |
| СH3–(СH2)3–СH3 | СH3–(СH2)3–СH2– | н -пентил (амил) | первичный |
| изопентан | СH3–СН(СH3)–СH2–СH2– | изо пентил | первичный |
| СH3–СH2–СН(СH3)–СH2– | втор. пентил | первичный | |
| СH3–СH2–СH2–(СH3)СН– | втор. пентил | вторичный | |
| неопентан | (СH3)3С–СH2– | нео пентил | первичный |
| СnH2n алкен | СnH2n -1– | алкенил | |
| Продолжение таблицы 8 | |||
| СH2=СH2 этен | СH2=СH– | этенил | первичный |
| СH3–СH=СH2 пропен | СH2=СH–СH2– | пропенил – 2 (аллил) | первичный |
| СH3–СH=СH– | пропенил | первичный | |
| СnH2n -2 алкин | СnH2n -3– | алкинил | |
| СH≡СH этин | СH≡С– | этинил | первичный |
| СH3–С≡СH пропин | СH3–С≡С– | пропинил | первичный |
| СH≡С–СH2– | пропинил – 2 (пропаргил) | первичный | |
| СnH2n -6 арен | СnH2n -7 | арил | – |
| С6H6 | С6H5– | фенил | – |
| С6H5–СH3 толуол | С6H5–СH2– | бензил | первичный |
| СH3–С6H4– | толуидил (о –, п –, м –) | – | |
| СH4 метан | –СH2– | метилен | – |
| СH2=СH2 этен | СH2=С< | винилиден | – |
Префикс – приставка (лат. praefixum от prae – впереди + fixus – прикрепленный). Префиксы н-, втор.-, трет.- выделяются курсивом, от основания отделяются дефисом.
Префиксы, напечатанные курсивом, не учитываются при расстановке заместителей в названии в алфавитном порядке.
Курсивом выделяются:
· префиксы: н-, втор.-, трет.-, цис-, транс-, D-, L-, R-, S-, E-, Z-, син-, анти-, эндо-, экзо-, гош-;
· буквенные локанты: α-, β-, γ- и т. д. орто (о-), мета (м-), пара, (п-), N.
Буквы латинского алфавита предшествуют буквам греческого алфавита.
Дефис (лат. divisio – разделение) – короткая соединительная черточка между двумя словами. Применяется для отделения от названия основы цифровых и буквенных локантов, префиксов, выделенных курсивом.
Умножающие префиксы:
· ди-, три-, тетра-, пента- и т. д. применяются для обозначения числа одинаковых незамещенных радикалов, например триэтиламин;
· бис-, трис-, тетракис-, пентакис- и т.д. применяются для обозначения числа идентичных одинаково замещенных радикалов, например бис-(2-хлорэтил)амин, трис-(2-хлорэтил);
· би-, тер-, квартер- употребляются для указания числа идентичных колец, соединенных друг с другом связью.
Вицинальный радикал (лат. vicinus – соседний): свободные валентности находятся у соседних атомов углерода.
Геминальный радикал (лат. geminus – близнецы): свободные валент-ности находятся у одного и того же атома углерода.
Примечание. Геминальный двухвалентный радикал:
· –СН2– обозначается суффиксом -илен (метилен);
· –СН2–СН2–СН2– называется триметилен;
· –СН2(СН3)СН– обозначается суффиксом -илен (пропилен).
Систематическая номенклатура. В 1892 г. появилась Женевская номенклатура. Позже ее положения были переработаны в Льежскую номенклатуру (1930 г.). В 1957 г. были приняты правила IUPAC (International Union of Pure and Applied Chemistry).
В рамках этой номенклатуры соединения рассматриваются как продукты усложнения нормальных предельных углеводородов либо замещенных циклов, получаемых путем замещения атомов водорода какими-либо структурными фрагментами. Характер заместителя указывается приставкой (префиксом) или окончанием. Для уточнения положения производится нумерация атомов основы (локантов).
Способы построения названия в номенклатуре IUPAC (на примере ациклического соединения):
· выбрать основу, в качестве которой избирается самая длинная цепь углеродных атомов, в которой содержатся функциональные группы и кратные связи;
· пронумеровать основу, начиная с наиболее замещенного конца. Начало нумерации определяет старшая функциональная группа, затем кратная связь и углеводородный заместитель. По уменьшению старшинства некоторые функциональные группы располагаются следующим образом:
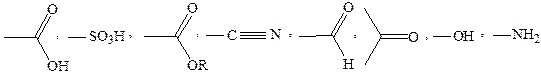
· составить название, включающее название заместителей в алфавитном порядке, название главной цепи, окончание, характерное для кратной связи и старшей функциональной группы. Положение заместителей и функциональной группы указывается цифрами, их количество – греческими числительными.
1. 2-амино-4-метилтиобутановая кислота:

2. 3-метил-4-хлорформил-этил-бутаноат:
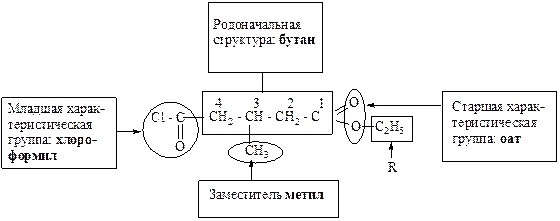
3. 4-амино-2-гидроксибензолкарбоновая кислота:
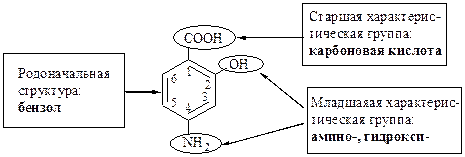
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2454; Нарушение авторских прав?; Мы поможем в написании вашей работы!