
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Эксплуатация кислотных и щелочных аккумуляторов
|
|
|
|
6.5.1. Устройство и принцип действия кислотного аккумуляторного элемента.
Электролитическая диссоциация – это распад молекул серной кислоты под действием молекул воды. H2ЅO4 2Н+ + ЅO4− −, в результате в воде образуются ионы независимо, есть ли в растворе пластины. В целом раствор электрически нейтральный. Если этот раствор - электролит, залить в конструкцию, состоящую из набора положительных и отрицательных пластин, разделенных секторами и помещенных в эбонитовую емкость, закрытую крышкой с выводами положительных пластин и отрицательных пластин, получим элемент положительного аккумулятора.
Образование ионов в электролите
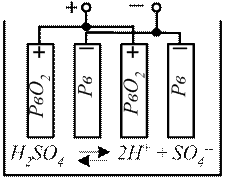 В результате взаимодействия электролита с атомами свинца отрицательной пластины некоторое количество атомов свинца ионизируется. При этом двухзарядные положительные ионы свинца переходят в электролит, а на поверхности отрицательной пластины от каждого атома свинца остается по два электрона, поэтому отрицательная пластина заряжена отрицательно относительно электролита. В результате взаимодействия активного вещества пластины с электролитом на обеих пластинах образуются электрические заряды.
В результате взаимодействия электролита с атомами свинца отрицательной пластины некоторое количество атомов свинца ионизируется. При этом двухзарядные положительные ионы свинца переходят в электролит, а на поверхности отрицательной пластины от каждого атома свинца остается по два электрона, поэтому отрицательная пластина заряжена отрицательно относительно электролита. В результате взаимодействия активного вещества пластины с электролитом на обеих пластинах образуются электрические заряды.
Рис.6.5. Устройство кислотного аккумулятора
На положительной - четырехзарядные ионы свинца, на отрицательной - электроны.
Такое состояние элемента может находиться теоретически сколь угодно долго, пока не будет замкнута цепь на потребитель электроэнергии. Как только замкнем цепь электроны с отрицательной пластины перемещаются к положительной пластине по внешней цепи. Каждый атом свинца отрицательной пластины отдает два электрона. Они переходят на положительную пластину и соединяются с (Pb++++), образуя ион свинца (Pb++) двухзарядный, который соединяясь с положительным остатком ЅO4¯ ¯ образует молекулу сульфата свинца (PbЅO4). Так как растворимость сульфата мала, то раствор становится перенасыщенным и сульфат выпадает на (+) пластине в виде кристаллов, одновременно около положительной пластины образуются молекулы воды PbO2 + 4Н + ЅO4¯ ¯+2е- → PbЅO4+2Н2О
|
|
|
На отрицательной пластине Pb++ + ЅO4¯ ¯−2е- → PbЅO4
| Двуокись свинца | До разряда | разряд | После разряда | |||

| 
| |||||
| PbO2 + Pb + 2Н2ЅO4 | → | Pb ЅO4 + Pb ЅO4 + 2Н2O | ||||
| + | − | Электролит и вода | ← | + | − | вода и электролит |
 Пл. Пл.
| Пл. |  Пл. Пл.
| Пл. | |||
| заряд | 
| |||||
| После разряда | До разряда |
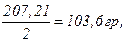 Каждый элемент обладает емкостью в АЧ. Это количество электричества, отдаваемого элементом до конечного разряда 1,8В. Емкость зависит от количества активных веществ. При прохождении количества электричества, равному одному фарадею на образование сульфата свинца у отрицательной пластины будет израсходовано 103,6 гр свинца. 1Фарадей-26,8 А.Ч. атомный и молекулярный вес свинца равен 207,21 а в реакции у отрицательных пластин участвуют два электрона, то грамм эквивалент свинца равен
Каждый элемент обладает емкостью в АЧ. Это количество электричества, отдаваемого элементом до конечного разряда 1,8В. Емкость зависит от количества активных веществ. При прохождении количества электричества, равному одному фарадею на образование сульфата свинца у отрицательной пластины будет израсходовано 103,6 гр свинца. 1Фарадей-26,8 А.Ч. атомный и молекулярный вес свинца равен 207,21 а в реакции у отрицательных пластин участвуют два электрона, то грамм эквивалент свинца равен
а при отдаче 1 А.Ч. в 26,8 раза свинца будет меньше, т.е.3,6 г.
Таким же образом можно найти, что при отдаче 1 А.Ч. из положительной пластины на образование сульфата свинца будет израсходовано 4,46 г двуокиси свинца, а в электролите из 3,66 г образуется 0,672 г воды.
Номинальное напряжение 1 элемента составляет 2,1 В рабочее напряжение в начале разряда быстро достигает 2 В, затем постепенно снижается до конечного = 1,8 В. Если продолжать разряд, оно дойдет до 0.
6.5.2. Общие правила эксплуатации кислотных аккумуляторных батарей
1. Поддерживать уровень электролита 12÷15м
2. Не допускать разряд ниже 1,75 В.
3. Заряд производить до полной емкости
4. Регулярно производить перезаряды аккумулятора.
5. Не допускать пребывание аккумулятора в полуразряженном состоянии.
|
|
|
6. Регулярно очищать поверхность аккумулятора от грязи и окислов.
очищать поверхность аккумулятора от грязи и окислов.
7. Не допускать загрязнения электролита.
8. Не допускать перезарядки и не заряжать током выше нормированного.
9. Заливать электролит плотностью, рекомендованной для данного климатического пояса эксплуатации.
10. Не допускать во время заряда повышение температуры аккумуляторной батареи свыше +45ºС. Необходимо прерывать заряды и давать аккумулятору остыть до +30ºС.
11. Эксплуатационная плотность электролита определяется приведенной к +15ºС и должна отличаться не более чем на ±50.
12. После заливания электролита в аккумулятор дать ему постоять 4-6 часов.
13. Зарядный ток определяется по таблицам в зависимости от емкости аккумуляторной батареи.
14. При зарядке аккумуляторной батареи в судовых условиях предварительно включается вентиляция.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 1354; Нарушение авторских прав?; Мы поможем в написании вашей работы!