
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Коагуляция и дзета-потенциал
|
|
|
|
Различают два вида коагуляции коллоидных растворов электролитами − концентрационную и нейтрализационную.
Концентрационная коагуляция связана с увеличением концентрации электролита, не вступающего в химическое взаимодействие с компонентами коллоидного раствора. Такие электролиты называют индифферентными; они не имеют ионов, способных достраивать ядро мицеллы и вступать в реакцию с потенциалопределяющими ионами. При увеличении концентрации индифферентного электролита диффузный слой противоионов мицеллы сжимается, переходя в адсорбционный слой. В результате уменьшается электрокинетический потенциал, и он может стать равным нулю. Такое состояние коллоидной системы называется изоэлектрическим. С уменьшением электрокинетического потенциала агрегативная устойчивость коллоидного раствора снижается и при критическом значении дзета-потенциала начинается коагуляция. Термодинамический потенциал при этом не изменяется.
При нейтрализационной коагуляции ионы прибавляемого электролита нейтрализуют потенциалопределяющие ионы, уменьшается термодинамический потенциал и соответственно уменьшается и дзета-потенциал.
|
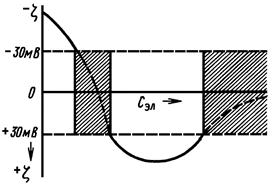
| Рис. 22.1 Чередование зон устойчивости (заштрихованы) при введении в золь электролита. |
Когда в коллоидные системы вводят порциями электролиты, содержащие многозарядные ионы с зарядом, противоположным заряду частицы, золь сначала остаётся устойчивым, затем в определённом интервале концентраций происходит коагуляция, далее золь снова становится устойчивым и, наконец, при высоком содержании электролита опять наступает коагуляция, уже окончательно. Подобное явление могут вызывать и объёмные органические ионы красителей и алкалоидов.
|
|
|
Рассмотрим механизм этого явления (рис. 22.1)
Вначале содержание введённого электролита многозарядных ионов недостаточно, чтобы скоагулировать золь; при этом дзета-потенциал частиц выше критического его значения. Дальнейшее добавление электролита приводит к тому, что его ионы начинают проявлять коагулирующее действие. Указанный интервал концентраций отвечает значениям электролитического потенциала частиц от критического дзета-потенциала ζкр одного знака до ζкр противоположного знака. При последующем добавлении многозарядных ионов начинается перезарядка коллоидных частиц, и золь становится опять устойчивым. В этой зоне дзета-потенциал снова выше критического значения, но его знак обратен знаку дзета-потенциала частиц исходного золя. Если продолжать добавлять электролит, то многозарядные ионы снова и окончательно коагулируют золь.
Влияние различных концентраций многозарядных ионов было отмечено давно, и оно получило название явления неправильных рядов. В то время перезарядка частиц золей была мало исследована и только потом выяснилось, что чередование зон устойчивости и неустойчивости при добавлении многозарядных ионов вполне закономерно и поэтому термин неправильные ряды должен рассматриваться как условный.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2945; Нарушение авторских прав?; Мы поможем в написании вашей работы!