
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Второе начало термодинамики. При расширении газ совершает положительную работу за счет убыли своей внутренней энергии, т.е
Лекция
При расширении газ совершает положительную работу за счет убыли своей внутренней энергии, т.е. газ остывает в ходе адиабатического расширения. При адиабатическом сжатии, когда работа газа отрицательна, газ повышает свою температуру, т.е. нагревается.
1. Если в газе протекает адиабатический процессе, то изменяются все три параметра состояния – давление, температура и объем. Выведем уравнение состояния газа при адиабатических процессах, воспользовавшись первым началом термодинамики проделав ряд математических действий.
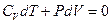
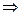

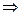

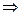
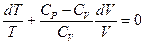
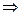

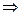 после интегрирования получаем
после интегрирования получаем
 ,
,
где C – произвольная постоянная интегрирования;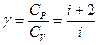 - показатель адиабаты или коэффициент Пуассона.
- показатель адиабаты или коэффициент Пуассона.
Окончательно после потенцирования получаем уравнение, которое связывает два параметра состояния газа (температуру и объем) в адиабатическом процессе:
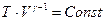 .
.
Используя уравнение состояния идеального газа  , если
, если  и заменяя либо температуру газа, либо его объем в полученном уравнении адиабаты, легко получить уравнения, связывающие давление – объем и давление – температуру:
и заменяя либо температуру газа, либо его объем в полученном уравнении адиабаты, легко получить уравнения, связывающие давление – объем и давление – температуру:

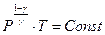 .
.
Таким образом, получено три уравнения адиабаты, которые попарно связывают параметры состояния.
2. Диаграмма состояния в координатах 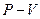 имеет вид (Рис.7):
имеет вид (Рис.7):

3. Величина работы адиабатического процесса может быть легко вычислена по уравнению: 
4. Первое начало термодинамики для адиабатического процесса имеет вид:

5. Теплоемкость при адиабатическом процессе равна нулю, так как 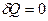 .
.
Стоит обратить внимание на уравнение адиабаты  , связывающее давление и объем, и сравнить его с уравнением изотермы
, связывающее давление и объем, и сравнить его с уравнением изотермы  . Сделаем это, изобразив оба процесса на графике в координатах
. Сделаем это, изобразив оба процесса на графике в координатах  (Рис.8).
(Рис.8).

Адиабата идет круче, чем изотерма. Объясняется это тем, что при адиабатическом сжатии увеличение давления газа обусловлено не только уменьшением объема, как при изотермическом сжатии, но и повышением температуры газа. При адиабатном расширении газа его температура понижается и поэтому давление газа падает быстрее, чем при изотермическом расширении. По Рис.8 видно, что адиабата идет круче, чем изотерма как при расширении газа от 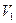 до
до 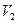 , так при его сжатии от
, так при его сжатии от 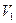 до
до 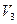 . Это говорит о том, что работа газа при адиабатическом расширении меньше чем при изотермическом процессе, а при сжатии газа наоборот.
. Это говорит о том, что работа газа при адиабатическом расширении меньше чем при изотермическом процессе, а при сжатии газа наоборот.
Ранее было отмечено, что теплота и работа – это характеристики процесса, а внутренняя энергия – функция состояния, т.е. её значение не зависит от типа процесса. Рассмотрение изопроцессов показало, что теплоемкость, как теплота и работа, является характеристикой процесса.
Прежде, чем переходить к изложению второго начала термодинамики, необходимо рассмотреть круговые процессы. Круговым процессом, или циклом, называется такой процесс, в результате которого термодинамическое тело возвращается в исходное состояние. В диаграммах состояния 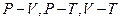 круговые процессы изображаются в виде замкнутых кривых – начало кругового процесса и его конец на диаграмме изображаются одной и той же точкой. Круговые процессы лежат в основе работы всех тепловых машин: двигателей внутреннего сгорания, газовых, паровых, холодильных машин. Поэтому изучение циклов является важнейшей задачей физики.
круговые процессы изображаются в виде замкнутых кривых – начало кругового процесса и его конец на диаграмме изображаются одной и той же точкой. Круговые процессы лежат в основе работы всех тепловых машин: двигателей внутреннего сгорания, газовых, паровых, холодильных машин. Поэтому изучение циклов является важнейшей задачей физики.
Внутренняя энергия газа зависит только от температуры газа, т.е. от его состояния. Следовательно, полное изменение внутренней энергии газа при круговом процессе равно нулю (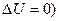 . По первому началу термодинамики все подведенное к системе тепло расходуется на работу газа:
. По первому началу термодинамики все подведенное к системе тепло расходуется на работу газа:
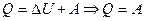 ,
,
где  - общее количество теплоты, сообщенной газу в круговом процессе,
- общее количество теплоты, сообщенной газу в круговом процессе,  - работа газа в этом процессе.
- работа газа в этом процессе.
Циклы бывают прямые и обратные. В прямом цикле 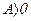 и
и 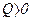 , т.е. в прямом цикле газ совершает положительную работу за счет сообщенной ему теплоты. Она измеряется заштрихованной площадью на Рис.1.
, т.е. в прямом цикле газ совершает положительную работу за счет сообщенной ему теплоты. Она измеряется заштрихованной площадью на Рис.1.

В обратном цикле над газом совершается работа, т.е. она отрицательна ( ), а числен- но измеряется также заштрихованной площадью на Рис.2.
), а числен- но измеряется также заштрихованной площадью на Рис.2.
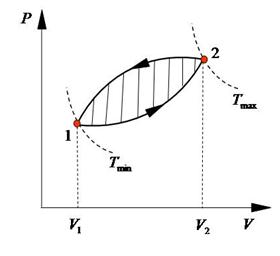
В этом случае от газа отводится количество теплоты, эквивалентное работе.
В тепловом двигателе рабочее тело (газ) совершает прямой цикл, а в холодильной машине – обратный цикл.
Рассмотрим один из важнейших циклов – Цикл Карно. Этот цикл сыграл огромную роль в развитии термодинамики и теплотехники, так как позволил подойти к анализу коэффициента полезного действия тепловых машин.
Цикл Карно
Цикл Карно – идеальный цикл, так как рабочим телом является идеальный газ. Цикл Карно состоит из двух изотерм и двух адиабат - Рис.3.

В любом термодинамическом цикле, включая цикл Карно, есть нагреватель, когда система получает энергию в виде теплоты, и холодильник, где рабочее тело, т.е. газ, отдает тепло, чтобы возвратиться в исходное состояние и вновь совершить работу.
Рассчитаем коэффициент полезного действия идеальной тепловой машины, действующей по прямому циклу Карно, используя первое начало термодинамики и уравнение состояния идеального газа. После того, как газ приведен в исходное состояние (на диаграмме точка 1), рабочее тело, т.е. газ, проходит ряд процессов.
Процесс 1-2 – изотермический (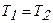 ). Следовательно,
). Следовательно, 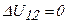 и по первому началу термодинамики получается, что газ расширяясь все полученное тепло расходует на работу, которую он совершает при своем расширении, т.е.
и по первому началу термодинамики получается, что газ расширяясь все полученное тепло расходует на работу, которую он совершает при своем расширении, т.е. 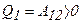 , где:
, где:
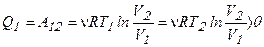 . (6.1)
. (6.1)
Процесс 2-3 – адиабатический, на этом процессе система не обменивается теплом с окружающей средой - 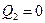 . По первому началу термодинамики газ совершает работу за счет изменения своей внутренней энергии:
. По первому началу термодинамики газ совершает работу за счет изменения своей внутренней энергии:
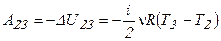 . (6.2)
. (6.2)
Поскольку газ расширяется на этапе 2-3, то 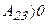 и, следовательно, температура газа понижается -
и, следовательно, температура газа понижается - 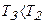 .
.
Процесс 3-4 – изотермический (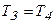 ) и
) и 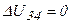 . Газ на этапе 3-4 сжимается и работа, которую он совершает, отрицательна, следовательно, на этом процессе теплота, которую отбирают у газа, будет также отрицательна:
. Газ на этапе 3-4 сжимается и работа, которую он совершает, отрицательна, следовательно, на этом процессе теплота, которую отбирают у газа, будет также отрицательна:
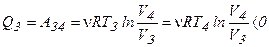 . (6.3)
. (6.3)
Процесс 4-1 – адиабатический, т.е. 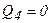 ; по первому началу имеем:
; по первому началу имеем:
 (6.4)
(6.4)
Поскольку газ сжимается на этапе 4-1, то 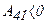 и, следовательно, т емпература газа повышается -
и, следовательно, т емпература газа повышается - 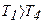 .
.
Рассмотрев все изопроцессы, входящие в цикл Карно, рассчитаем коэффициент полезного действия этого цикла:
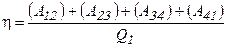 , (6.5)
, (6.5)
где в числителе учтена работа, совершаемая идеальным газом на всех участках цикла, а в знаменателе - количество теплоты полученной газом. Подставим в это уравнение ранее записанные соотношения:
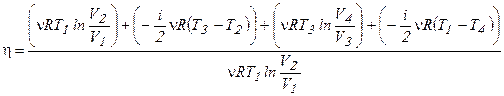 . (6.6)
. (6.6)
Учитывая, что 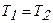 и
и 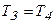 , а также, что
, а также, что 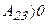 и
и 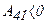 , приходим к выводу – работы на участках 2-3 и 4-1 численно равны и противоположны по знаку. Выражение для КПД принимает вид:
, приходим к выводу – работы на участках 2-3 и 4-1 численно равны и противоположны по знаку. Выражение для КПД принимает вид:
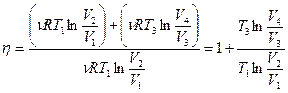 . (6.7)
. (6.7)
Чтобы упростить полученное выражение, воспользуемся уравнением адиабаты - 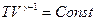 и применим его для процесса 2-3 -
и применим его для процесса 2-3 - 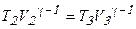 и процесса 4-1 -
и процесса 4-1 - 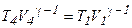 затем запишем эти уравнения в ином виде:
затем запишем эти уравнения в ином виде:
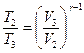 ;
; 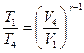 . (6.8)
. (6.8)
Сравнив последние уравнения, можно записать:

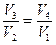
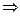
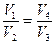
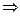
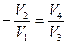 . (6.9) Окончательно для коэффициента полезного действия получаем выражение:
. (6.9) Окончательно для коэффициента полезного действия получаем выражение:
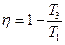 , (6.10)
, (6.10)
где  - температура нагревателя,
- температура нагревателя, 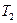 - температура холодильника.
- температура холодильника.
Уравнению для КПД цикла Карно можно придать и другой вид:
 , (6.11)
, (6.11)
где  - теплота, полученная от нагревателя;
- теплота, полученная от нагревателя; 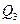 - теплота, отданная холодильнику.
- теплота, отданная холодильнику.
Проанализируем полученное уравнение:
- совершенно очевидно, что КПД идеальной тепловой машины, работающей по циклу Карно, всегда меньше единицы;
- повысить КПД можно двумя путями: либо повысить температуру нагревателя, либо понизить температуру холодильника; оба способа требуют солидных капитальных затрат и при этом не обеспечивают значительного прироста КПД;
- кроме того, необходимо отметить, что рассмотрение цикла Карно показывает, что процессы расширения газа 1-2 и 2-3 протекают самопроизвольно, а процессы сжатия газа 3-4 и 4-1 – нет; встает вопрос - почему какие-то процессы протекают самопроизвольно и какая величина может быть критерием самопроизвольного протекания процесса.
|
|
Дата добавления: 2014-01-07; Просмотров: 1383; Нарушение авторских прав?; Мы поможем в написании вашей работы!