
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Анодный и катодный процессы при электрохимической коррозии
|
|
|
|
При электрохимической коррозии выделяют два взаимосвязанных процесса: анодный и катодный.
v Анодный процесс – окисление металла, проходит на участках изделий с меньшим потенциалом в данной среде. Анодные участки разрушаются.
v Катодный процесс – восстановление окислителя, находящегося в растворе или расплаве электролита, происходит на участках изделий с бóльшим потенциалом в данной среде. Катодные участки химически не изменяются. Они служат проводниками электронов от анодных участков к окислителю, чем усиливают коррозию анодных участков. Более подробно это будет рассмотрено далее на конкретных примерах.
Окислители при коррозии принято называть деполяризаторами. Коррозию с участием наиболее распространенных окислителей – растворенного кислорода и ионов водорода (кислоты или воды) соответственно называют коррозией с кислородной и водородной деполяризацией. Уравнения катодных процессов приведены в таблице.
| Уравнения катодного процесса при коррозии | |
| с водородной деполяризацией (в отсутствие растворенного О2) | с кислородной деполяризацией в присутствии растворенного О2) |
| кислая среда | |
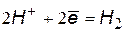 (1) (1)
| 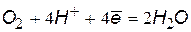 (3) (3)
|
| нейтральная и щелочная среда | |
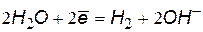 (2) (2)
| 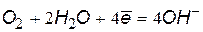 (4) (4)
|
Окислительно-восстановительные потенциалы кислорода и водорода в различных средах (точнее, соответствующих окислительно-восстановительных пар) указаны в таблице.
| Кислая среда (рН = 0) | Нейтральная среда (рН = 7) | Щелочная среда (рН = 14) | |||
| Oк/Вс | Е0, В | Oк/Вс | Е0, В | Oк/Вс | Е0, В |
| 2H+/H2 | 0,00 | 2H2O/H2 | -0,41 | 2H2O/H2 | -0,83 |
| O2/2H2O | +1,22 | O2/4OH– | +0,81 | O2/4OH– | +0,40 |
Окислительные свойства кислорода выше окислительных свойств иона водорода (или воды). В присутствии кислорода в растворе коррозия необязательно будет проходить за счет кислородной деполяризации, так как концентрация растворенного кислорода, как правило, невелика. Установлено, что при рН³7, т.е. в нейтральных и щелочных растворах, процесс обычно протекает с кислородной деполяризацией - уравнение (4), в кислых средах – преимущественно с водородной деполяризацией - уравнение (1).
|
|
|
Коррозия, как и любой окислительно-восстановительный процесс, может осуществляться только при условии, что потенциал окислителя больше потенциала восстановителя (металла анодных участков).
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 1854; Нарушение авторских прав?; Мы поможем в написании вашей работы!