
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электролитическая диссоциация. Электролиты и неэлектолиты. Теория сильных электролитов. Ионная сила растворов. Водородный показатель. Произведение растворимости. Гидролиз солей
|
|
|
|
В первой половине XIX в. М. Фарад ей ввел понятие об электролитах и неэлектролитах.
Электролиты – это вещества, растворы и расплавы которых проводят электрический ток.
Неэлектролиты - это вещества, растворы и расплавы которых не проводят электрический ток.
Частицы, которые проводят ток в растворе – это ионы. Они образуются из твердых веществ при их растворении.
Ионы – заряженные частицы: Cl-, Cu2+, NO3-
Катионы – ионы с зарядом +
Анионы – ионы с зарядом –
Для объяснения свойств водных растворов электролитов шведский ученый С. Аррениус (1859—1927) в 1887 г. предложил теорию электролитической диссоциации.
Согласно этой теории, при растворении в воде электролиты распадаются на свободные ионы. Этот процесс назвали электролитической диссоциацией.
Процесс распада электролитов на ионы в процессе растворения или расплавления называется ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИЕЙ.
Неэлектролитами является большинство органических веществ (спирты, эфиры, альдегиды, углеводороды, углеводы).
Как происходит процесс растворения электролита?
Молекулы воды являются дипольными, т.е. один конец молекулы заряжен отрицательно, другой - положительно. Молекула отрицательным полюсом подходит к иону натрия, положительным - к иону хлора; окружают ионы со всех сторон и вырывают из кристалла, причём, только с его поверхности. Свободные ионы, оказавшиеся в водном растворе окружаются полярными молекулами воды: вокруг ионов образуется гидратная оболочка, т.е. протекает процесс гидратации.
При растворении молекулы с ковалентной полярной связью, молекулы воды, окружив полярную молекулу, сначала растягивают связь в ней, увеличивая её полярность, затем разрывают её на ионы, которые гидратируются и равномерно распределяются в растворе.
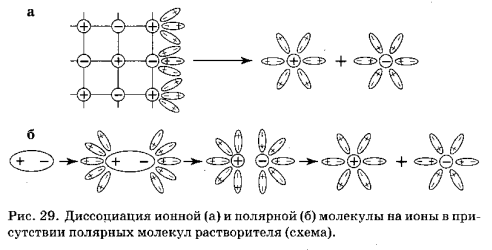
При расплавлении, когда происходит нагревание кристалла, ионы начинают совершать интенсивные колебания в узлах кристаллической решётки, в результате чего она разрушается, образуется расплав, который состоит из ионов.
Характеристикой глубины протекания процесса диссоциации является степень диссоциации.
Степень диссоциации – это отношение числа продиссоциировавших молекул к общему числу молекул растворённого электролита:
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 496; Нарушение авторских прав?; Мы поможем в написании вашей работы!