
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гальванические элементы (первичные элементы). 1. Закон України “Про підприємництво”, 1991
|
|
|
|
ПЕРВИЧНЫЕ ИСТОЧНИКИ ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ
СПИСОК РЕКОМЕНДОВАНОЇ ЛІТЕРАТУРИ
1. Закон України “Про підприємництво”, 1991.
2. Закон України “Про власність”, 1991.
3. Закон України “Про підприємства”, 1991.
4. Закон України “Про банкрутство”, 1991.
5. Закон України “Про оплату праці”, 1995.
6. Закон України “Про господарські товариства”, 1995.
7. Господарський Кодекс України, 2003.
8. Економіка підприємства: Підручник/ За ред. С.Ф. Покропивного – Вид. 2-ге – К.: КНЕУ, 2004 – 528 с.
9. Бойчик І. М. Економіка підприємства: Навчальний посібник. – К.: Атіка, 2004 – 408 с.
10. Сідун В.А., Пономарьова Ю.В. Економіка підприємства: Навчальний посібник – К.: Центр навчальної літератури, 2003 – 436 с.
11. Економіка підприємства: Структурно-логічний навчальний посібник/За ред. С.Ф. Покропивного – К.: КНЕУ, 2001 – 457 с.
12. Економіка підприємства: Підручник – В 2 т / За ред. С.Ф.Покропивного – К.: ”Хвиля – прес”, 1995 – 400 с.
13. Иванов В.Г., Файвишенко Л.В., Атамась П.Д. Экономика предприятия: Курс лекций – Донецк: ДИЭХП, 2000 – 265 с.
14. Экономика предприятия: Учебник / Под ред. О.И. Волкова – М.: ИНФРА – М., 2000 – 520 с.
15. Грузинов В.П., Грибов В.Д. Экономика предприятия: Учебное пособие – М.: Финансы и статистика, 1998 – 208 с.
16. Экономика предприятия: Учебник для ВУЗов / Под ред. В.Я. Горфинкеля – М.: ЮНИТИ, 1996 – 367 с.
17. Селезнёв В.В. Основы рыночной экономики Украины: Учебное пособие – К.: АСК, 2000 – 544 с.
18. Современная экономика. Общедоступный учебный курс. – Ростов-на-Дону: «ФЕНИКС», 1998. – 605 с.
19. Экономика предприятия: Задачи. Ситуации. Решения.: Учебное пособие / Под ред. С.Ф. Покропивного. – К.: Знання-прес, 2001 –343 с.
20. Продиус И. П., Филиппова С.В., Захарченко В.И. Экономика предприятия. Краткий курс. – Харьков: Одиссей, 2004. – 192 с.
|
|
|
Гальванические элементы (ГЭ) – это первичные элементы, которые допускают лишь однократное использование заключенных в них активных элементов. Им свойственен только процесс разряда. Различают ГЭ сухие (с невыливающимся электролитом) и с жидким электролитом (наливные).
ГЭ любого типа состоит из двух разнородных электродов (проводников первого рода, которые разделяются слоем электролита (проводник первого рода)). Между этими электродами возникает разность потенциалов, которая зависит от материала электродов и состава электролита.
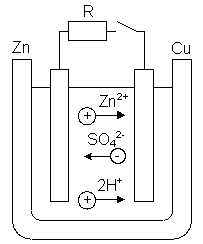 Рассмотрим сущность электрохимических процессов на гальваническом элементе Вольта.
Рассмотрим сущность электрохимических процессов на гальваническом элементе Вольта.
Элемент Вольта состоит из сосуда с раствором Н2SO4 и двух электродов – цинкового и медного. Цинковый электрод в электролите растворяется. Под действием химических сил в электролит переходят ионы цинка. Эти ионы, соединяясь с отрицательным ионом SO4, образуют молекулы цинкового купороса ZnSO4. При этом нарушается электрическая нейтральность электролита и он заряжается положительно. Свободные валентные электроны, остающиеся в цинке, заряжая цинковый электрод отрицательно. В области соприкосновения цинкового электрода с цинком образуется электрическое поле. Силы электрического поля направлены противоположно химическим силам, т.е. препятствуют растворению цинка. Если цепь разомкнута, то химические силы уравновешиваются силами электрического поля и процесс растворения цинка быстро прекращается. При этом между цинковым электродом и электролитом возникает определенная разность потенциалов, которая называется электродным потенциалом металла. Электродный потенциал цинка 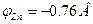 . Медный электрод нейтрализует часть ионов водорода электролита, отдавая им свободные электроны, поэтому получает положительный потенциал
. Медный электрод нейтрализует часть ионов водорода электролита, отдавая им свободные электроны, поэтому получает положительный потенциал 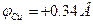 . Следовательно, ЭДС элемента Вольта составляет:
. Следовательно, ЭДС элемента Вольта составляет:
|
|
|
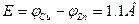 .
.
ЭДС многих ГЭ находится в пределах 0,8÷1,6В. Поэтому для получения больших напряжений ГЭ соединяют последовательно. При замыкании внешней цепи валентные электроны цинка начинают перемещаться по проводнику r. При этом ослабляется электрическое поле между цинковым электродом и электролитом. Нарушается равновесие электрических и химических сил. В связи с этим под действием последних возобновляется процесс растворения цинка, перемещение ионов цинка и водорода к медному электроду, а ионы кислотного остатка – к цинковому электроду, т.е. осуществляется процесс разрядки ГЭ.
Важной характеристикой качественной работы ГЭ является устранение т.н. явления поляризации. Во время работы ГЭ происходит непрерывный процесс растворения отрицательного электрода, а к положительному электроду из электролита подходят ионы водорода, которые разряжаются на нем. При этом молекулы водорода на положительном электроде образуют непроводящий слой. Это явление называется поляризацией. В результате этого явления увеличивается внутреннее сопротивление элемента и снижается его напряжение. Для устранения поляризации в состав элемента вводят деполяризаторы, т.е. вещества, богатые кислородом, например, перекись марганца. Деполяризаторы превращают водород в воду и освобождают положительный электрод от непроводящего слоя водорода.
Емкость и саморазряд ГЭ. Количество электричества, которое можно получить от элемента в течение разряда, называется емкостью первичного элемента. Оно измеряется в А·ч, которая вычисляется выражением:
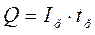 ,
,
где Ip – ток разряда (А); tp – время разряда (ч).
Емкость первичного элемента зависит от количества заложенных в него активных веществ, разрядного тока, режима разряда, температуры электролита и времени хранения. Увеличение разрядности тока ухудшает процесс деполяризации. Активные вещества, заложенные в элемент, используются не полностью. В результате снижается емкость элементов. Для улучшения условий эксплуатации ГЭ рекомендуется производить перерывы разрядного тока, что будет улучшать процесс деполяризации и способствовать увеличению емкости ГЭ. С увеличением температуры электролита химические процессы в элементах протекают более интенсивно и емкость электролита возрастает. Однако при слишком высоких температурах происходит высыхание электролита и снижение емкости.
|
|
|
Даже при отключенной нагрузке в ГЭ происходит процесс саморазряда, т.е. бесполезный расход его активных веществ. Саморазряд элемента вызывается несовершенством изоляции между электродами и образованием на отрицательном электроде местных гальванических пар в местах вкрапления в электрод посторонних примесей. Саморазряд увеличивается при установке элемента в сыром месте, при загрязнении его пылью и грязью.
Номинальная или гарантированная емкость элемента. Номинальная емкость элемента – минимально допустимая емкость, которую должен отдавать элемент в режиме работы, указанном заводом-изготовителем. Фактическая емкость обычно превосходит на 10-20% его номинальную. Номинальная емкость марганцево-цинкового элемента определяется при непрерывном разряде на R=10 Ом и t=15÷30 ºC до напряжения 0,7 В и определяется выражением:
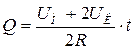 ,
,
где UН – начальное напряжение, измеренное на зажимах элемента в течение первых 10с после начала разряда; UК – конечное напряжение разряда (0,7 В); R – сопротивление разрядной цепи (10 Ом); T – время разряда.
Температура элемента существенно влияет, как ранее отмечалось, на величину отдаваемой емкости. При повышении температуры внешней цепи интенсивность электрохимических процессов возрастает, что приводит к увеличению саморазрядов элементов, а это приводит к быстрому уменьшению их емкости. Зависимость емкости элемента от температуры определяется следующим выражением:
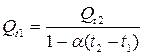 ,
,
где t1 – начальная температура; t2 – конечная температура; α – темпера-турный коэффициент емкости.
|
|
|
|
|
Дата добавления: 2014-01-20; Просмотров: 385; Нарушение авторских прав?; Мы поможем в написании вашей работы!