
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Небілкові азотисті компоненти крові
У живому організмі одночасно з процесом біосинтезу білка (асиміляція) відбувається протилежний процес – розпад білків (дисиміляція), який значно посилюється при розвитку патологічних явищ. Продуктами розпаду білка є такі речовини, як аміак, сечовина, креатин, креатинін, сечова кислота, індикан, глутамін, окремі амінокислоти, які складають фракцію так званих небілкових азотистих компонентів крові. Азот перерахованих азотовмісних речовин називається залишковим азотом крові (ЗА). Така назва зумовлена тим, що згадана фрак-ція компонентів крові належить до азотистих речовин, які залишаються в плазмі крові після додавання до неї трихлороцтової кислоти і випадання білка в осад.
Найбільш вагомою складовою частиною ЗА є азот сечовини, який у нормі становить близько 50 % усього ЗА. У здорової худоби і свиней кількість ЗА в сироватці крові становить 15–29 ммоль/л. Підвищення вмісту залишкового азоту в крові називається гіперазотемією. Залежно від причин, розрізняють ретенційну і продуктивну гіперазотемію. Ретенційна гіперазотемія буває нирковою (при нефриті і пієлонефриті), коли вміст ЗА підвищується до 107–214 ммоль/л (в основ-ному за рахунок сечовини), і позанирковою, яка спостерігається при зменшенні клубочкової фільтрації при хворобах серця та зневодненні. Наприклад, у новонароджених телят із синдромом діареї і тяжким ступенем зневоднення кількість виділюваної сечі зменшується утричі, а концентрація залишкового азоту в сироватці крові зростає.
Продуктивна гіперазотемія розвивається за рахунок азоту амінокислот унаслідок посиленого розпаду білків в організмі (злоякісні новоутворення), але функція нирок збережена.
Гіпоазотемія зустрічається значно рідше. Причиною її буває знач-не ураження печінки, унаслідок чого порушується синтез сечовини.
Сечовина є кінцевим продуктом обміну білків, основною складовою частиною ЗА крові у ссавців. Вона становить 80–90% усіх азотис-тих речовин сечі. За добу із сечею людини виділяється 25–35 г сечовини. Сечовина (NH2-CO-NH2) утворюється здебільшого в орнітиновому циклі в печінці та частково – у нирках (цикл Кребса-Генселяйта). Початковим етапом її утворення є з’єднання аміаку з вугільною кислотою, які утворилися в процесі дезамінування і декарбоксилювання, та АТФ, у результаті чого утворюється карбомоїлфос-фат, який вступає в реакцію з орнітином (рис. 10).
| Аміак + СО2 + Н2О + 2 АТФ ® карбомоїлфосфат ® ® орнітин ® цитрулін ® аргініно-бурштинова кислота ® фумарова кислота + аргінін ® орнітин + сечовина |
Рис. 10. Схема орнітинового циклу утворення сечовини
Таким чином, під час синтезу сечовини знешкоджується аміак. Необхідна для синтезу сечовини енергія АТФ забезпечуються циклом Кребса. Взаємозв’язок між цими двома циклами образно названий «двоколісним велосипедом» Кребса. Уся сечовина фільтрується в проксимальні канальці нирок, після чого близько 35 % її реабсорбується знову, решта виділяється із сечею.
Уміст сечовини в сироватці крові молодняку великої рогатої худоби становить (ммоль/л) 3,0–6,5; корів – 3,5–6,0; свині – 3,3–6,0; собаки – 3,0–8,0. Концентрація сечовини залежить від інтенсивності її синтезу та виведення. Тому визначення її є важливим діагностичним тестом як функції печінки, де вона синтезується, так і нирок, через які вона виводиться. Частіше зустрічається збільшення вмісту сечовини, що свідчить про ураження нирок. При гострій нирковій недостатності рівень сечовини в сироватці крові зростає до 50–80 ммоль/л і навіть
більше, а виділення її з сечею різко зменшується. Якщо вміст сечовини досягає 35 ммоль/л, то це вказує на середній ступінь ураження нирок. При хронічному перебігу гломерулонефриту та в азотемічній стадії нефротичного синдрому вміст сечовини підвищується до 13–15 ммоль/л, а в пізні строки хронічної ниркової недостатності – до 30–35 ммоль/л. Кількість азоту сечовини у фракції ЗА збільшується до 90 %.
Зменшення вмісту сечовини в сироватці крові спостерігається при аліментарному виснаженні (ЗА зростає за рахунок азоту амінокислот), тяжкому перебігу патології печінки, яка володіє значними функ-ціональними резервами, тому синтез сечовини зберігається навіть тоді, коли уражено 85 % її паренхіми. Оскільки вміст ЗА при цьому може залишатися в межах норми, то процентне відношення азоту сечовини до ЗА стає нижчим 45 % (якщо перерахунок робити у мг/100 мл), або 10 % – при розрахунку в ммоль/л. Якщо на фоні підвищення вміс-ту ЗА кількість сечовини починає зменшуватися, то має місце комбінована патологія нирок і печінки (гепаторенальний синдром).
Креатин надходить в організм м’ясоїдних із тваринними кормами, а в жуйних в основному синтезується з аргініну, гліцину і метіоніну. Починається синтез у нирках, а закінчується в печінці, звідки він надходить у м’язи і мозок. У м’язах креатин приєднує АТФ, утворюючи креатинфосфат (креатин +АТФ ® креатинфосфат + АДФ) – сполуку, яка багата на макроергічні зв’язки і є джерелом енергії, необхідної для скорочення м’язів. При роботі креатинфосфат вивільняє енергію і знову перетворюється в креатин (креатинфосфат – АМФ ® креатин). У нормі в сироватці крові вміст азоту креатину становить 75–115 мкмоль/л, а в сечі його немає. Якщо вміст креатину в крові перевищує 120 мкмоль/л, то тоді він починає виділятися із сечею, тобто розвивається креатинурія, яка спостерігається при міопатії (прогресуючій м’язовій дистрофії, міозиті, міотонії – м’язовій слабос-ті, міоглобінурії), а також при ураженні печінки, зменшенні синтезу креатинфосфату і особливо – при ураженні нирок унаслідок зниження ниркового порогу. Кретинурією супроводяться тонічні судоми при різних хворобах і отруєннях.
Креатинін є похідним креатину, його кінцевим продуктом метаболізму. Частина креатину не перетворюється в креатинфосфат, а віддає молекулу води і перетворюється в креатинін. Він може утворюватися також з креатинфосфату (+АДФ ® креатинін + АТФ).
 NH2
|
C=NH
| NH2
|
C=NH
|
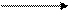 N–CH3 – Н2О
|
СН2
|
COOH
Креатин N–CH3 – Н2О
|
СН2
|
COOH
Креатин
| HN
  |
C=NH
|
N–CH3
|
CH2
| |
C=NH
|
N–CH3
|
CH2
|
 С
||
О
Креатинін С
||
О
Креатинін
|
Уміст креатиніну в сироватці крові становить 70–140 мкмоль/л (у людей – 50–115). Креатинін у клінічно здорових людей і тварин пов-ністю фільтрується клубочковим апаратом нефрону і не реабсорбується в канальцях. Тому визначення креатиніну використовують для вивчення фільтраційної функції клубочків нирок. Об’єм клубочкової фільтрації при нормальному вмісті креатиніну в сироватці крові становить 85–135 мл за 1 хв, при 200 мкмоль/л – 37 мл/хв, при 300 – 23, 400 – 17 мл/хв (функціонує від 20 до 50 % клубочків нирок). Якщо креатиніну міститься від 500 до 700 мкмоль/л, то об’єм фільтрації становить 13–8,8 мл/хв і функціонує лише 10–20 % клубочків. За вищого рівня креатиніну (700–1016 мкмоль/л) об’єм фільтрації первинної сечі менший 8 мл/хв і функціонує менше 10 % клубочків.
Визначення креатиніну широко використовують у клінічній практиці як показник кліренсу нирок, який вказує на кількість плазми або сироватки крові, яка за одиницю часу повністю очищається від введеної речовини. Кліренс нирок за вмістом креатиніну визначають за формулою:
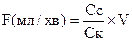 ,
,
де F – клубочкова фільтрація; Сс і Ск – концентрація креатиніну в сечі і крові; V – об’єм сечі, яка виділяється за 1 хв.
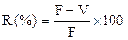 ,
,
де R – канальцева реабсорбція.
Сечова кислота – один із кінцевих продуктів обміну нуклео-протеїнів, при розпаді яких утворюються нуклеїнові кислоти, які у свою чергу гідролізуються до нуклеотидів. Подальший розпад нуклеотидів здійснюють нуклеотидази, утворюючи пуринові (аденін і гуанін) та піримідинові основи. При дезамінуванні аденіну і гуаніну утворюються гіпоксантин, а потім – ксантин, який окиснюється у печінці ксантиноксидазою з утворенням сечової кислоти. У крові вона міститься у вигляді натрієвої солі, зв’язаної з білком. Цей комплекс дуже чутливий до зміни рН сечі: при рН 5,0 розчинність сечової кислоти становить 60 мг/л, а при рН 7,0–1600 мг/л. Сечова кислота є головною азотистою частиною сечі птиці: у гусей майже 70 % азоту сечі припадає на частку сечової кислоти і лише 3–4 % – сечовини. Виділяється вона у формі солей – уратів калію та натрію; при змішуванні з фекаліями утворює на них білий наліт. Нирки птиці ефективно виводять сечову кислоту навіть при низькій концен-трації її в плазмі і володіють достатніми компенсаторними можливостями: якщо на зернових раціонах кури щодня виділяють із сечею 2 г сечової кислоти, то при згодовуванні їм тваринних білків – 8–11 г. У нормі в плазмі крові птиці міститься 0,12–0,36 ммоль/л сечової кислоти, у людей – 0,16–0,50 ммоль/л. Збільшення вмісту сечової кислоти у плазмі крові (гіперурикемія) спостерігається: а) при підвищенні її синтезу з нуклеїнових кислот, що має місце при надмір-ному згодовуванні кормів тваринного походженні та обмеженні зелених; б) при захворюваннях, які супроводжуються посиленим розпадом нуклеопротеїнів (лейкемія, злоякісні пухлини); в) уна-слідок зменшення виділення сечової кислоти із сечею при патології нирок.
Найбільш поширеним захворюванням, яке виникає при порушенні пуринового обміну, є подагра. При цьому захворюванні в суглобах, хрящах, сухожильних сумках, на серозних покривах (епікарді, парієтальному листку серозної оболонки грудочеревної порожнини), у внутрішніх органах (нирках, серці, печінці) та м’язах солі сечової кис-лоти відкладаються у вигляді кристалів, навколо яких розвивається запалення з наступним розростанням сполучної тканини. Розрізняють чотири форми подагри: вісцеральну – урати відкладаються на серозних покривах і внутрішніх органах; суглобову; змішану – вісцерально-суглобову і локальну, коли урати відкладаються в нирках і сечоводах. Вісцеральна форма сечокислого діатезу реєструється як серед молодняку, так і дорослої птиці, тоді як суглобова форма виявляється лише у дорослої птиці.
Випадіння в осад уратів часто є причиною утворення каменів у нирках і сечових шляхах. Вони можуть бути центрами кристалізації інших солей і спричиняти утворення змішаних камінців.
Аміак утворюється в організмі внаслідок дезамінування амінокис-лот, аденілової кислоти та інших азотистих сполук. Збільшується продукція амонійного азоту (аміаку) у жуйних при порушенні співвідношення в кормах раціону між легко- та важкорозчинним протеїном. Включення до раціону таких кормів, як зелена маса люцерни, конюшини, озимого жита, які містять у своєму складі багато легкорозчинних білків, спричинює різке підвищення вмісту аміаку в рубці. Другим джерелом надходження аміаку в рубець є підвищений уміст нітратів у кормах. Значна кількість амонійного азоту накопичується в сінажі та силосі при порушенні технології їх заготівлі та при зберіганні. Рівень амонійного азоту може складати у силосі з кукурудзи 30–35 %, а в сінажі злаково-бобової суміші – 50–60 % від загального азоту корму. Четвертим джерелом надходження амонійного азоту в організм тварин є використання вугле-амонійних солей, аміачної води та інших препаратів, що містять у своєму складі небілковий азот.
Аміак є досить токсичною речовиною, тому організм має кілька механізмів його знешкодження. Основним є перетворення його в сечовину в печінці та частково у нирках (цикл Кребса-Генселяйта). Час-тина аміаку виділяється із сечею у вигляді солей амонію, інша – зв’язується з глутаміновою та аспарагіновою кислотами. У крові понад 96 % аміаку міститься у вигляді NH4+ і лише близько 4 % – в неіонізованому. У нормі вміст амонійного азоту становить менше
30 мкмоль/л.
Збільшення кількості амонійного азоту в крові – гіперамоніємія – спостерігається передусім при хворобах печінки (гепатиті, гепатодис-трофії, цирозі печінки) унаслідок пригнічення синтезу сечовини.
При цьому аміак стимулює процеси гліколізу, що спричинює накопичення молочної кислоти; зв’язується з a-кетоглутаровою і щавлево-оцтовою кислотами, що зумовлює зниження інтенсивності реакцій циклу Креб-са і тканинного дихання, а також – із гемоглобіном, утворюючи лужний гематин, що зумовлює кисневе голодування тканин, порушення функціонального стану серця, нирок і центральної нервової системи. Зменшення величини рН у клітині під впливом амонійного азоту спричинює зміни трансмембранних процесів у ній, співвідношення вільних нікотинамідних коферментів та аденіннуклеотидів, активності аденілат- та гуанілатциклази, вмісту циклічних нуклеотидів – цАМР та цГМР.
У корів порушується білоксинтезувальна функція печінки: при цьому в плазмі крові знижується рівень a2-макроглобуліну, фібриногену, білків системи комплементу та преальбумінів. Молозиво в таких корів має нижчі імунобіологічні властивості, а захворюваність новонароджених телят на гострі розлади травлення є вищою.
Дія амонійного азоту на організм моногастричних тварин значно сильніша, оскільки у них відсутня гепаторумінальна система обігу азоту.
Хвороби печінки супроводжуються різким підвищенням умісту аміаку в крові: в артеріальній – до 20–129, венозній – 12–85 мкмоль/л (у здорових корів – 7,0–30,0 і 5,5–25). Аміак легко проникає через гематоенцефалічний бар’єр, і його кількість у лікворі може досягати 40–64 мкмоль/л проти 8,5 у здорових корів (Влізло В.В., 1998). У тварин розвивається печінкова енцефалопатія і печінкова кома; причому, глибина коми пропорційна рівню аміаку в крові. Йому ж належить значна роль у розвитку епілептичних судом.
Уміст аміаку в сечі значно зростає при уроциститі, пієлонефриті внаслідок розпаду сечовини під впливом бактерій та при ацидозі.
|
|
Дата добавления: 2014-01-20; Просмотров: 6442; Нарушение авторских прав?; Мы поможем в написании вашей работы!